星状硝子体症(AH)
粒子形状:球状
組成:カルシウム・リン脂質、ムコ多糖
硝子体状態:非液化、ゲル状態を保つ
静止時の挙動:元の位置に戻る
症状:通常無症状
発症背景:加齢性変性

星状硝子体症(Asteroid Hyalosis; AH)は、硝子体のコラーゲン線維にカルシウム含有リン脂質・ムコ多糖が沈着する変性疾患である。沈着物を「星状体(asteroid body; AB)」と呼び、硝子体中に黄白色の球状混濁として認められる。
1894年に Alfred Hugh Benson が初記述し、後に Luxenberg と Sime が「asteroid hyalosis」と命名した。閃輝性硝子体融解症(synchysis scintillans)とは異なる独立した疾患である(鑑別診断の項参照)。
疫学的特徴は以下の通りである。
| 研究 | 有病率 | 特記事項 |
|---|---|---|
| Beaver Dam Eye Study | 1.2% | 43-54歳 0.2% → 75-86歳 2.9% |
| Blue Mountains Eye Study | 1.0% | 49-55歳 0% → 75-97歳 2.1% |
| UCLA剖検コホート(10,801人) | 1.96% | — |
AHの有病率は約2%で、約80%が片眼性である。3) 性差として男性(1.4%)が女性(0.6%)より多く、60歳以上の高齢者に好発する。
糖尿病との合併はしばしば指摘されてきた。しかし、Beaver Dam・Blue Mountains・UCLA研究のいずれにおいても有意な関連は確認されていない。片眼性が主体であることも、全身疾患との関連に疑問を呈する根拠となっている。
古くから糖尿病との合併が指摘されてきた。しかし、Beaver Dam Eye Study、Blue Mountains Eye Study、UCLA剖検コホートの3つの大規模研究いずれも有意な関連を確認できていない。片眼性が主体であることも、全身疾患との直接的な因果関係に疑問を呈している。
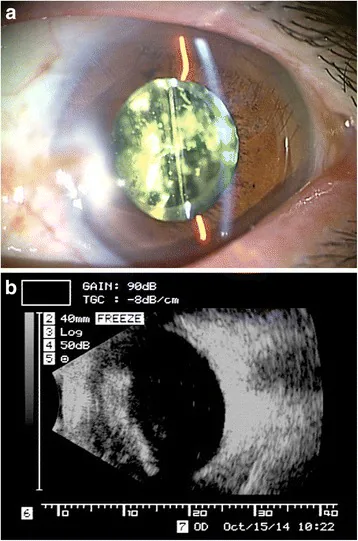
通常は無症状である。中等度の混濁があっても飛蚊症を自覚しないことが多く、視力は良好で治療不要なことが多い。
稀に後部硝子体剥離(PVD)の発生を契機として急性視力低下を生じる。机序は星状体が前方硝子体に集中し、眼の結節点(nodal point)付近の混濁密度が上昇して視軸を遮断するためである。3)
Marlow らの6眼ケースシリーズでは、全例が急性ないし亜急性の視力低下を呈した。術前矯正視力(BCVA)の平均は20/150(範囲 20/25〜20/2500)で、後部硝子体剥離進行に伴う平均低下量は logMAR 0.70 であった。3)
細隙灯顕微鏡では、黄白色で球状の粗な粒子が硝子体中に浮遊する所見を認める。眼球運動とともに可動性を呈するが、静止すると元の位置に戻る。星状体は大きな粒子であり、白血球との区別は容易である。硝子体液化はきたしていないことが多く、後部硝子体剥離を生じていない例が多い。網膜との癒着が強固で後部硝子体剥離が生じにくい特性がある。
AH眼で後部硝子体剥離が発生した場合、異常な硝子体網膜接着によりvitreoschisis(硝子体分離)を伴いやすい。3)
Marlow らの6眼中3眼で完全後部硝子体剥離が、3眼で部分後部硝子体剥離(vitreoschisis)が確認された。3)
通常は無症状だが、後部硝子体剥離(PVD)の発生を契機に急性視力低下を生じることがある。星状体が前方硝子体に集中して視軸を遮断するためである。3) Marlow らの報告では術前平均視力が20/150に低下した症例群も、PPV後3ヶ月以内に全例が基線視力に回復した。3)
加齢が最大のリスク因子である。そのほか以下の要因との関連が報告されている。
細隙灯顕微鏡検査で硝子体中の特徴的な黄白色球状混濁を確認する。眼球運動で可動性を示しながら静止で元位置に戻る所見が診断の鍵となる。カルシウム結晶由来の大きな粒子であり、診断は比較的容易である。
各検査の特性を以下に示す。
| 検査法 | 特性 | 有用な場面 |
|---|---|---|
| OCT | AHの影響少ない | 硝子体網膜界面評価 |
| FA | AH下でも撮影可 | 糖尿病網膜症合併例 |
| 超音波Bモード | 後方エコー欠損なし高輝度焦点 | 眼底透見不能時 |
星状硝子体症(AH)
粒子形状:球状
組成:カルシウム・リン脂質、ムコ多糖
硝子体状態:非液化、ゲル状態を保つ
静止時の挙動:元の位置に戻る
症状:通常無症状
発症背景:加齢性変性
閃輝性硝子体融解症(SS)
その他の鑑別疾患として、硝子体アミロイドーシス、硝子体出血、硝子体炎(ぶどう膜炎)、眼内リンパ腫などがある。
密なAHでは眼底透見が困難になることがある。しかしOCT(830nm波長)・蛍光眼底造影(FA)・眼底自発蛍光(FAF)・超音波Bモードなどの補助検査で眼底情報を得ることができる。FA検査はAH合併の糖尿病網膜症診断にも有用である。
通常は飛蚊症を自覚せず視力が良好なため、治療を要さない。混濁が強くても視力が保たれていることが多く、手術対象となることは少ない。
視力障害を生じる場合に手術適応となる。後部硝子体剥離に伴う急性視力低下例では、硝子体手術が治癒的に視力を回復させる。3)
硝子体手術の適応と成績
適応:混濁が強く視力障害を生じる場合
手術方式:23G または 25G 経結膜硝子体手術3)
視力回復経過:術後1ヶ月で2眼が基線視力に回復、3ヶ月で全眼が回復3)
最終最高矯正視力:平均 20/35(範囲 20/20〜20/200)3)
術後合併症:報告なし3)
白内障手術時の注意点
IOL度数誤差:屈折値・眼軸長の測定誤差が生じることがある
前房移動(術中):I/A操作中に星状体が前房へ移動する稀な合併症1)
前房移動(術後遅発):悪性緑内障など房水逆流によっても起こりうる2)
対処法:I/Aによる吸引・前房洗浄で除去可能1)2)
AH眼の硝子体手術では、硝子体の液化が生じにくく後部硝子体皮質と網膜の癒着が病的に強いため、慎重な操作が必要である。増殖糖尿病網膜症を合併する場合は網膜光凝固が困難となり、硝子体手術の難易度も高くなる。
Saeed らは、70歳男性の白内障手術中(I/A操作時)に黄白色球状体が前房に移動した1例を報告した。嚢破損・チン小帯損傷なし。I/Aで吸引・除去し、IOLを嚢内に挿入した。術後視力は 20/20 で4年後も良好であった。文献上AH前房移動は術後例3例のみであり、術中移動はこの症例が初報告である。1)
Desai らは、白内障手術後2ヶ月で前房内黄色結晶塊・IOP 35 mmHg・前房浅小化を呈した70歳男性を報告した。悪性緑内障によるAH前房移動と診断した。前房洗浄+硝子体生検+虹彩-チン小帯-硝子体切除術を施行し、翌日IOP は 17 mmHg に改善した。後嚢欠損やチン小帯脆弱がなくても、房水逆流でAH前房移動が起きうることを示した。2)
硝子体手術で硝子体ごと星状体を除去するため、術後の再発は報告されていない。Marlow らの6眼全例で術後3ヶ月以内に基線視力が回復し、合併症も認めなかった。3)
星状体はリン酸カルシウムが硝子体中に析出し、コラーゲン線維に付着することで形成される。電子分光イメージングではCa・P・Oが均一分布し、ヒドロキシアパタイトに構造的・元素的に類似することが示されている。免疫蛍光顕微鏡では星状体周囲にコンドロイチン-6-硫酸が検出され、レクチン金標識によりヒアルロン酸特異的炭水化物が内部マトリックスの一部を構成することが確認されている。プロテオグリカンとグリコサミノグリカン(GAG)側鎖が生体鉱物化(biomineralization)プロセスの調節に関与していると考えられている。
AH眼では硝子体液化が進みにくく、網膜との癒着が強固であるため後部硝子体剥離が起こりにくい。しかし一旦後部硝子体剥離が発生すると、異常な硝子体網膜接着によりvitreoschisis(硝子体皮質分離)を伴う異常後部硝子体剥離となりやすい。3)
Marlow らの6眼中3眼で部分後部硝子体剥離(vitreoschisis)が確認された。vitreoschisisが生じると、星状体を含む前方硝子体が眼の結節点付近に集中し視力障害が顕在化する。3)
Topilow らの病理学的解析では、AH眼の81%で硝子体ゲルが顕微鏡的に正常であり、19%で中等度の液化(syneresis)が確認された。1)
術中のAH前房移動は、硝子体液化(syneresis)とチン小帯微小間隙を介した星状体の前方移動によると考えられている。1) 術後遅発性には悪性緑内障による房水逆流が前方移動を引き起こす別機序も存在する。2) 後嚢欠損やチン小帯脆弱がない状態でもAH前房移動が生じうる点が重要である。1)2)