ドライ型(非新生血管型)
全加齢黄斑変性の80〜90%:進行は緩徐。ドルーゼン蓄積と網膜色素上皮の変性が特徴。
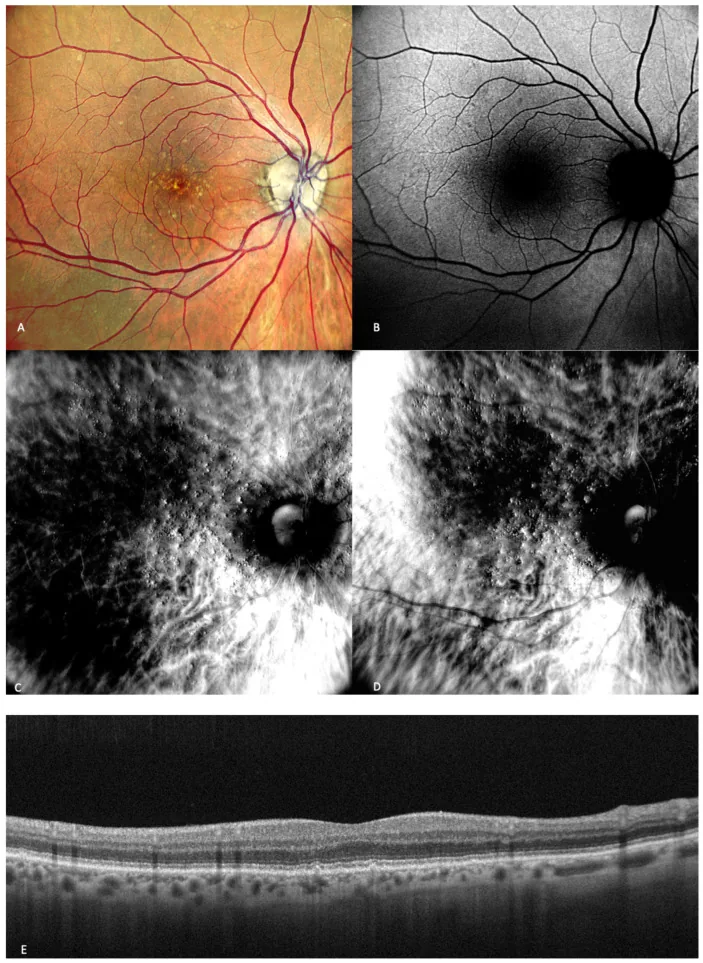
地図状萎縮:進行期の最終像。境界明瞭な網膜色素上皮の萎縮が黄斑に広がる。
FDA承認治療は限られる:2024年承認の補体阻害薬が地図状萎縮の成長抑制に用いられる。

加齢黄斑変性は、網膜の中心部である黄斑の網膜色素上皮(RPE)・Bruch膜・脈絡膜複合体が変性する後天性疾患である。**非新生血管型(ドライ型)と新生血管型(ウェット型)**に大別される。
加齢黄斑変性は世界で約2億人が罹患しており、2040年には約2億8800万人に増加すると予測される3)。後期加齢黄斑変性の有病率は50〜59歳で0.1%、80歳以上で4.3%と、年齢とともに指数関数的に上昇する7)。英国の法的失明の26%、米国の20%は地図状萎縮に起因する8)。地図状萎縮は世界で約500万人に影響を与え、米国だけで約100万人が罹患している8)。
人種差があり、白人での有病率が最も高い7)。
加齢黄斑変性の臨床病期と進行リスクの目安を以下に示す。
| 病期 | ドルーゼン径 | 進行リスク |
|---|---|---|
| 早期 | <63μm(硬性) | 低 |
| 中期 | 63〜125μm(軟性) | 中 |
| 後期 | ≥125μm/地図状萎縮/脈絡膜新生血管 | 高 |
ドライ型(非新生血管型)
全加齢黄斑変性の80〜90%:進行は緩徐。ドルーゼン蓄積と網膜色素上皮の変性が特徴。
地図状萎縮:進行期の最終像。境界明瞭な網膜色素上皮の萎縮が黄斑に広がる。
FDA承認治療は限られる:2024年承認の補体阻害薬が地図状萎縮の成長抑制に用いられる。
ウェット型(新生血管型)
全加齢黄斑変性の10〜20%:脈絡膜新生血管(黄斑新生血管)の発生により急激な視力低下を来す。
網膜下出血・漿液性網膜剥離:脈絡膜新生血管からの液体・血液の漏出が特徴。
第一選択は抗VEGF硝子体内注射:早期治療で視力を維持・改善できる。
片眼に後期加齢黄斑変性がある場合、もう一方の眼にも後期加齢黄斑変性が生じるリスクは高い。定期的な眼科検診と自己モニタリング(Amslerグリッド)が推奨される。
初期は無症状であることが多い7)。症状が出た時点で病変がある程度進行している場合も多く、定期検診による早期発見が重要である。
黄斑部のドルーゼン(脂質・タンパク質・炎症成分の細胞外沈着物)が加齢黄斑変性の初期所見である。
境界鮮明な網膜色素上皮の萎縮領域。直径250μm以上、脈絡膜中大血管が透見可能。地図状萎縮の成長速度が速いほど最高矯正視力(BCVA)低下が速く、2年間で約75%の患者が5文字以上の視力低下を来す8)。
スウェプトソース光干渉断層血管造影(SS-OCTA)により、無症状段階から非滲出型黄斑新生血管が46.67%(45眼中21眼)に検出される1)。
Amslerグリッド(方眼紙状の自己チェックシート)で変視症や暗点を自己確認できる。ただし初期は無症状であることが多く7)、定期的な眼科受診による客観的評価が不可欠である。
加齢黄斑変性は多因子疾患であり、加齢・遺伝・環境因子が複雑に関与する。
AREDS/AREDS2サプリメント(ルテイン・ゼアキサンチン・ビタミンC・E・亜鉛・銅)は、中期加齢黄斑変性が後期へ進行するリスクを低減する7)。ただし早期加齢黄斑変性や予防目的での有効性は確立されていない。なお、βカロチンは喫煙者の肺癌リスクを高めるため、喫煙者にはルテイン/ゼアキサンチン配合製品を選択する7)。
中期加齢黄斑変性から後期への進行リスクを低減する7)。βカロチンは喫煙者の肺癌リスクを高めるため、喫煙者にはルテイン/ゼアキサンチン配合を選択する7)。
ドライ型加齢黄斑変性(地図状萎縮)の進行抑制を目的に2024年にFDA承認を取得した。地図状萎縮の治療薬の比較を以下に示す。
| 薬剤 | 標的 | 投与間隔 |
|---|---|---|
| ペグセタコプラン(Syfovre) | C3(補体第3成分) | 25〜60日ごと |
| アバシンカプタドペゴル(Izervay) | C5(補体第5成分) | 28日ごと×12ヵ月 |
ペグセタコプランはOAKS/DERBY第3相試験で地図状萎縮の成長率を有意に減少させた7)。アバシンカプタドペゴルはGATHER2試験で有効性が示された7)。ただし、両薬剤とも地図状萎縮の成長率は減少したが、視力改善を事前設定評価項目とした試験では有意差が得られなかった8)。
ドライ型では、AREDS2サプリメントが中期から後期への進行リスクを低減する7)。地図状萎縮に対しては補体阻害薬(ペグセタコプラン・アバシンカプタドペゴル)がFDA承認を得ており、地図状萎縮の成長速度を抑制する7), 8)。視力の実質的な改善は現時点では困難であり、進行抑制が治療目標となる。
ラニビズマブ / ベバシズマブ
アフリベルセプト
標準用量(2mg):毎月または2ヵ月ごと投与。
高用量(8mg):PULSAR試験で最大16週間隔投与が可能。治療負担の軽減が期待される7)。
ブロルシズマブ
6mg投与:scFv構造により長期持続。HAWK/HARRIER試験で12週ごと(四半期)投与が可能6)。
特殊状況での有用性:硝子体切除眼でも有効。他の抗VEGF薬に無効の症例で20/20を回復した症例報告がある6)。
注意:眼内炎症・網膜血管閉塞リスクがある7)。
ポリープ状脈絡膜血管症では抗VEGF療法と光線力学的療法の併用が選択肢となる7)。
導入期は通常1〜3ヵ月間、毎月1回の注射を行う。その後は必要時投与またはtreat-and-extend(間隔を徐々に延長)レジメンで管理する7)。新しい薬剤(アフリベルセプト8mg・ファリシマブ)では最大16週間隔の維持が可能な症例もある。
加齢黄斑変性はBruch膜/脈絡膜複合体・網膜色素上皮・視細胞が変性する多因子疾患である。
補体経路(古典的経路・副経路・レクチン経路)の調節異常が地図状萎縮の病態の主要因である8)。CFH、C3、ARMS2の遺伝子多型が発症感受性に関与する7)。
Anegondiら(2025)はGATHER/ランパリズマブ試験データの解析で、地図状萎縮の成長率が速いほど最高矯正視力低下が速く、補体経路の持続的活性化が地図状萎縮の拡大を駆動することを示した8)。
眼内液中でIL-6、IL-8、MCP-1、VEGFが上昇する2)。脈絡膜内層の肥満細胞が脈絡膜新生血管の発症に関与し、加齢黄斑変性の脈絡膜では肥満細胞数の増加と脱顆粒の亢進が認められる2)。
Ribattiら(2024)は、脈絡膜肥満細胞が分泌するトリプターゼ・粘膜類天疱瘡-2/粘膜類天疱瘡-9によるBruch膜の分解が網膜色素上皮の死を誘発し、VEGF-A・FGF-2・IL-8・NGF・TNF等の放出が血管新生を促進すると報告した2)。
老化した網膜色素上皮細胞は細胞老化関連分泌表現型(SASP)を示し、SA-β-gal・p53・p21・p16の発現が増加する5)。この老化網膜色素上皮の表現型は、ドライ型加齢黄斑変性の患者の所見と一致する5)。
非滲出型の黄斑新生血管は無症状でも生物学的に活性であり、経時的な面積増大が持続する1)。
Wangら(2023)は45眼(中央値14.83ヵ月追跡)を対象としたスウェプトソース光干渉断層血管造影研究で、成長型の黄斑新生血管(面積50%以上増大)は滲出転化までの期間が非成長型より有意に短く(13.60ヵ月 vs 31.11ヵ月、ハザード比12.51)、喫煙歴と高トリグリセリド血症が成長と有意に相関した(P=0.021)と報告した1)。抗VEGF治療中も成長が持続することがあり、これは血管剪定と再増殖のサイクルを反映する。
また、眼内炎発症後に脈絡膜新生血管が退縮した7眼中5眼で網膜下液/網膜色素上皮剥離の消失が確認されており、眼内炎症で誘導されるGBP-1が抗血管新生状態を形成する可能性が示唆されている4)。
補体阻害薬の課題
FDA承認済み(2024年):ペグセタコプラン(C3阻害)・アバシンカプタドペゴル(C5阻害)が地図状萎縮の成長を抑制7), 8)。
今後の課題:視力アウトカムの改善。ランパリズマブ(抗補体因子D)は第3相試験で有効性を示さなかった7)。
光生物調節
赤色〜近赤外光(650〜1300nm):ミトコンドリア機能促進・抗酸化酵素活性改善・抗炎症機序3)。
Lightsite III第3相試験:ドルーゼン体積減少・視力改善が確認された3)。在宅用デバイスの開発が進む。
セノリティクス
Nutlin-3a(MDM2阻害薬):老化網膜色素上皮細胞を選択的に除去する新規アプローチ5)。
概念実証段階:ミトコンドリア特異的セノリティクスの開発が今後の課題5)。
Jiら(2025)は、光生物調節治療を受けたドライ型加齢黄斑変性の患者の症例を報告した3)。8ヵ月間で右眼のドルーゼン面積は58%減少し、左眼では100%消失した。視力は両眼とも20/30から20/20に改善した。
Anegondiら(2025)はランパリズマブ試験データの解析から、地図状萎縮の成長速度が速いほど最高矯正視力低下が速く、2年間で約75%が5文字、約50%が10文字、約25%が15文字以上の視力低下を来すことを示した8)。
CFH・ARMS2・C3などの遺伝子多型が加齢黄斑変性の発症リスクに関与する7)。現時点では遺伝子検査による治療方針の変更は標準化されていないが、家族歴がある場合の定期検診の動機づけに役立つ可能性がある。
Wang Y, Sun J, Wu J, et al. Growth of nonexudative macular neovascularization in age-related macular degeneration: an indicator of biological lesion activity. Eye (Lond). 2023;37(10):2048-2054.
Ribatti D, Dammacco R. Mast cells in human choroid and their role in age-related macular degeneration (AMD). Clin Exp Med. 2024;24(1):98.
Ji PX, Pickel L, Berger AR, Sivachandran N. Improvement in dry age-related macular degeneration with photobiomodulation. Case Rep Ophthalmol. 2025;16(1):155-162.
Kokame GT, Yannuzzi NA, Shantha JG, et al. Involution of neovascular age-related macular degeneration following endophthalmitis. Retin Cases Brief Rep. 2021;15(5):495-499.
Chung H, Kim C. Nutlin-3a for age-related macular degeneration. Aging (Albany NY). 2022;14(14):5613-5616.
Maggio E, Alfano A, Mete M, Pertile G. Intravitreal brolucizumab for neovascular age-related macular degeneration in a vitrectomized eye. Case Rep Ophthalmol. 2022;13(3):736-743.
American Academy of Ophthalmology. Age-Related Macular Degeneration Preferred Practice Pattern. San Francisco, CA: American Academy of Ophthalmology; 2024.
Anegondi N, Steffen V, Sadda SR, et al. Visual loss in geographic atrophy: learnings from the lampalizumab trials. Ophthalmology. 2025;132(4):420-430.