原因ウイルス
VZV(最多):高齢者に多く病変範囲が広い傾向
HSV-1:高率に高眼圧(平均35 mmHg)を伴う
HSV-2:若年者に多い
CMV・EBV:極めて稀

急性網膜壊死(Acute Retinal Necrosis; ARN)は、ヘルペスウイルス科のウイルスが引き起こす重篤な壊死性網膜炎である。全ぶどう膜炎(汎ぶどう膜炎)として発症し、急激な視機能障害をもたらす。
1971年、浦山晃一らが6症例を「桐沢型ぶどう膜炎」として初報告した疾患であり、日本で命名された疾患概念である。英語圏では「Acute Retinal Necrosis(ARN)」として国際的に認知されている。
主な原因ウイルスは水痘帯状疱疹ウイルス(VZV)が最多で、単純ヘルペスウイルス(HSV-1・HSV-2)がこれに続く。サイトメガロウイルス(CMV)やエプスタイン・バーウイルス(EBV)による報告は稀である。EBVによる急性網膜壊死は極めて希少な事例として報告されている10)。
疫学的には年間発症率は0.5〜0.63/100万人(英国)と報告され3)4)、まれに1/160〜200万人/年との報告もある6)8)。50〜70代の免疫正常成人に多く、小児発症は稀である。男女差・人種差に一貫した傾向はない。
発症形式は2/3が片眼性で、1/3が両眼性(Bilateral 急性網膜壊死; BARN)である8)。免疫正常者に多く発症するが、免疫抑制状態も素因となる。近年では免疫チェックポイント阻害薬(ICI)3)、natalizumab8)、ジメチルフマル酸塩(DMF)6)など免疫抑制薬との関連が報告されている。また白内障手術5)やCOVID-19感染7)がトリガーとなった事例も報告されている。
原因ウイルス
VZV(最多):高齢者に多く病変範囲が広い傾向
HSV-1:高率に高眼圧(平均35 mmHg)を伴う
HSV-2:若年者に多い
CMV・EBV:極めて稀
疫学
発症率:0.5〜0.63/100万人/年(英国)
好発年齢:50〜70代が多い
片眼/両眼:約2/3が片眼性、1/3が両眼性
免疫状態:正常者が多いが免疫抑制者にも発症
三徴
周辺部壊死性網膜炎:境界明瞭な地図状白色病変
閉塞性網膜動脈炎:血管閉塞による網膜虚血
硝子体炎:中等度〜高度の炎症細胞浸潤
同一の疾患である。1971年に日本の浦山晃一らが「桐沢型ぶどう膜炎」として報告した疾患が、後に国際的に「Acute Retinal Necrosis(ARN)」として認識された。日本ではどちらの名称も使用される。
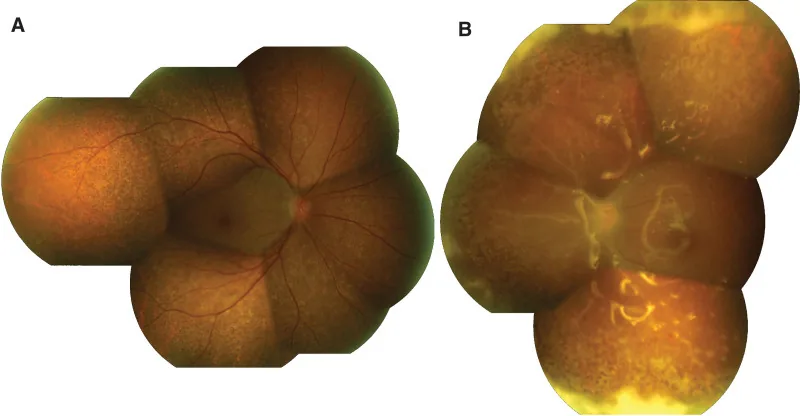
急性網膜壊死は急激な発症が特徴で、以下の症状が出現する。
蛍光眼底造影検査では閉塞性動脈炎パターンと乳頭過蛍光が確認される。OCT検査では、壊死性網膜炎部位に一致した脈絡膜肥厚(パキコロイド)が生じることが報告されており4)、新たな診断的所見として注目されている。
約1/3が両眼性(BARN)として発症する8)。片眼発症後、対側眼は数週から数年後に発症しうる。全身的な抗ウイルス薬維持療法が対側眼発症リスクを低下させると考えられており、詳細は「標準的な治療法」の項を参照。
急性網膜壊死の原因ウイルスとして以下が知られている。
既往感染の再活性化が主なリスクである。帯状疱疹の既往は30年以上前でもVZV再活性化による急性網膜壊死を引き起こすことがある5)。HSV脳炎の既往も原因となりうる9)。
免疫抑制薬との関連が近年増加しており、CD8+ T細胞やウイルス特異的T細胞免疫の低下が再活性化の鍵とされている。
natalizumab・DMF・免疫チェックポイント阻害薬・メトトレキサート(MTX)など様々な免疫抑制薬で急性網膜壊死発症が報告されている6)8)。CD8+ T細胞の減少がVZV・HSVの再活性化を促進することが主な機序と考えられており、これらの薬剤を使用中に眼症状が出現した場合は眼科の緊急受診が必要である。
急性網膜壊死は主に臨床所見に基づいて診断される。日本では高橋ら(2015)の診断基準が用いられており、以下のように分類される。
確定診断群:初期眼所見(壊死性網膜病変+前眼部炎症)+経過項目(病変の急速な拡大・閉塞性動脈炎・硝子体炎)+PCR陽性
臨床診断群:初期眼所見1a(壊死性網膜病変)+1b(前眼部炎症)+その他の初期項目2つ+経過項目1つ
2021年のSUN(Standardization of Uveitis Nomenclature)基準では、周辺部壊死性網膜炎の確認(PCR確認または典型的臨床像)が必要とされている4)。
以下の疾患との鑑別が重要である。
| 特徴 | 急性網膜壊死 | PORN | CMV網膜炎 |
|---|---|---|---|
| 免疫状態 | 正常者が多い | 高度免疫不全 | 免疫不全 |
| 硝子体炎 | 強い | 軽微 | 軽度 |
| 病変開始部 | 周辺部 | 後極部 | 血管沿い |
PORN(Progressive Outer Retinal Necrosis:進行性外側網膜壊死)はVZVによるHIV患者等の高度免疫不全者に多い病型で、硝子体炎が軽微で後極から始まる点で急性網膜壊死と異なる。
その他の鑑別疾患には、トキソプラズマ網脈絡膜炎、梅毒性網膜炎、眼内リンパ腫、転移性腫瘍などがある。転移性扁平上皮癌が急性網膜壊死に酷似した所見を呈した症例が報告されており1)、生検や全身検索が必要となる場合がある。
PCR検査(前房水または硝子体液)で原因ウイルス(VZV・HSV・CMVなど)を特定できる3)4)。初回が陰性でも臨床的に強く疑われる場合は治療を先行させ、再検することが推奨される。蛍光眼底造影やOCTで病変の範囲と活動性を評価する。
治療の基本は早期の抗ウイルス療法である。日本の教科書的な標準プロトコルを以下に示す。
| 治療 | 薬剤・用量 | 期間 |
|---|---|---|
| 抗ウイルス(初期) | ACV 10 mg/kg × 3回/日 IV | 2週間 |
| 抗ウイルス(継続) | VACV 500 mg × 6錠 分3 PO | 2週間 |
| 抗炎症(全身) | ベタメタゾン 8 mg IV | 5日→漸減 |
| 抗炎症(代替) | PSL 30 mg/日 PO | 7日間 |
| 抗血栓 | バイアスピリン 100 mg/日 PO | 4週間 |
| 局所(点眼) | ベタメタゾン 6回/日、トロピカミド 1回/日 | 適宜 |
ステロイドは抗ウイルス薬開始24〜48時間後から使用する2)。抗ウイルス薬を使用せずにステロイドのみを投与することは禁忌である2)。
各種免疫抑制関連急性網膜壊死の治療として以下が報告されている。
BARN症例(両眼性ARN)に対し、IV ACV 11 mg/kg q8h、硝子体内GCV 2 mg、経口VACV 2 g 3回/日、プレドニゾン60→40 mgの組み合わせが用いられた2)。
ICI関連急性網膜壊死では、硝子体内GCV 2.5 mg/0.1 mL(週2回×4週)+IV GCV 0.25 g bid×2週→経口VACV 0.3 g 3回/日×20週が奏効した3)。
白内障術後のVZV再活性化急性網膜壊死に対し、硝子体内GCV 2 mg/0.1 mL+IV ACV 750 mg q8h→経口ACV 14週が施行された5)。
EBV-急性網膜壊死においてアシクロビル・ガンシクロビル抵抗性を示した1例に、foscarnet 4800 mg/日 IVが奏効した10)。
抗ウイルス療法
初期静注療法:ACV 10 mg/kg IV(2週間)が基本。対側眼保護にも寄与
経口継続療法:VACV内服(2週間以上)。長期維持も考慮
硝子体内投与:GCV・foscarnetの硝子体内投与は難治例・重症例に考慮
抗炎症療法
手術療法
予防的レーザー光凝固:壊死病変境界部への施行。RD予防効果は議論あり
硝子体手術(PPV):日本ではACV灌流・眼内光凝固・輪状締結・シリコーンオイルを組み合わせる
網膜剥離時:硝子体手術+シリコーンオイル(±強膜バックル)
使用は可能だが、必ず抗ウイルス薬開始から24〜48時間後に限定する2)。抗ウイルス薬なしでのステロイド単独早期使用は禁忌であり、ウイルス増殖を助長して病態を悪化させる。適切なタイミングで使用すれば炎症抑制と網膜剥離リスクの低下に寄与する。
急性網膜壊死の発症機序は大きく急性ヘルペス期と後期瘢痕期に分けられる。
ウイルスの再活性化から始まる。HSVは三叉神経節の神経細胞に潜伏し、再活性化すると軸索流に乗って網膜に到達する。VZVは神経節外套細胞に潜伏し、病変範囲が広くなる傾向がある。
網膜内での病態は以下のように進行する。
各薬剤・病態固有の機序が明らかにされている。
ICI(PD-1/PD-L1阻害薬)による急性網膜壊死の機序として、免疫関連有害事象(IRIS類似機序)、自己寛容の障害、眼の免疫特権喪失などが示唆されている3)。
COVID-19関連急性網膜壊死では、SARS-CoV-2感染によるCD3+ CD8+ Tリンパ球の著明な減少が、潜伏HSVの再活性化を促進し対側眼急性網膜壊死の発症につながったと考えられている7)。
natalizumab関連急性網膜壊死では、白血球のCNS移行阻害作用によるCD4/CD8比低下がウイルス特異的免疫を低下させるとされている8)。
DMF(ジメチルフマル酸塩)関連急性網膜壊死では、CD8+ T細胞およびVZV特異的T細胞免疫の低下が再活性化のリスクを高める6)。
MTX(メトトレキサート)がEBVの再活性化を誘発しうることも報告されている10)。
OCTでの脈絡膜肥厚(パキコロイド)が急性網膜壊死の活動性を反映する所見として報告されている。
二次性VZV-急性網膜壊死の1例で、OCT上のパキコロイドが壊死性網膜炎部位に一致して生じ、治療後の経過観察において急性網膜壊死活動性のマーカーとして活用できる可能性が示唆された4)。また、初回PCR陰性の症例でも2回目の検体採取で陽性となった経緯も報告され、臨床的に強く疑われる場合の検査反復の重要性が示された4)。
アシクロビル・ガンシクロビルに抵抗性を示したEBV-急性網膜壊死の1例に対し、foscarnet 4800 mg/日 IVが奏効した10)。VZV・HSV以外のウイルスが原因の場合、標準的な治療が効きにくい場合があり、PCRによる原因ウイルスの同定が治療方針の決定に重要である。
免疫チェックポイント阻害薬(ICI)の普及に伴い、VZV再活性化による急性網膜壊死発症リスクへの注意が求められている3)。また、COVID-19感染後のHSV/VZV再活性化による急性網膜壊死報告が相次いでおり7)、免疫抑制療法関連の急性網膜壊死は今後も増加する可能性がある6)8)。