特発性
感染先行歴:ウイルス前駆症状(HCV、コクサッキーB型、EBV、HIV、COVID-19)、梅毒、ライム病などの感染症が先行することがある。
眼外傷:発症前の眼外傷が誘因となる場合が報告されている。
自己免疫仮説:抗ペルオキシレドキシン3(PRDX3)抗体が急性期に検出され、寛解後に消失することが示されている。RPE・視細胞タンパク質に対する自己抗体が病態に関与すると考えられる。
原因不明例:全身検査・遺伝子検査がいずれも陰性の純粋な特発性例も存在する。1)

急性滲出性多形卵黄状黄斑症(Acute Exudative Polymorphous Vitelliform Maculopathy; AEPVM)は、漿液性網膜剥離に一致する両眼性の多発性黄白色網膜下病変を特徴とする稀な網膜疾患である。1988年にGassらが初めて報告した(Trans Am Ophthalmol Soc 1988)。
発症年齢は13〜69歳と幅広く、性差は認めない。1)主に白人に発症するが、他の人種でも報告されている。文献上の特発性症例は約20例と極めて少ない。1)
AEPVMは病因により以下の2型に分類される。
本疾患はICD-10ではH35.89(その他の明示された網膜疾患)に分類される。
特発性AEPVMの文献報告は約20例にとどまり、極めて稀な疾患である。1)副腫瘍性も含めると報告例は増えてきているが、いずれの型も世界的に症例数が少ない。
両眼対称性・多発性の黄白色網膜下病変が主たる眼底所見である。病変の形態は多様であり、円形・楕円形・曲線状など様々な形態をとる。主に黄斑部に位置するが、血管弓沿いにも水疱状(bleb-like)病変が認められる場合がある。1)
病変内の卵黄状物質は重力に従って下方に沈殿し、半月状(meniscus-like)の液面形成(偽前房蓄膿;pseudohypopyon)を呈することがある。1)硝子体炎症や血管炎所見は認めず、視神経乳頭の異常も伴わない。1)
急性期と回復期では眼底所見が異なる。以下に2段階の所見を示す。
急性期と回復期の比較を以下に示す。
| 段階 | 眼底所見 | 視力 |
|---|---|---|
| 急性期 | 多発性卵黄状病変+漿液性網膜剥離 | 低下 |
| 回復期 | 漿液消失→卵黄状物質の下方沈殿 | 改善傾向 |
AEPVMは特発性と副腫瘍性の2型に分類され、それぞれ異なる原因・病態を持つ。
特発性
感染先行歴:ウイルス前駆症状(HCV、コクサッキーB型、EBV、HIV、COVID-19)、梅毒、ライム病などの感染症が先行することがある。
眼外傷:発症前の眼外傷が誘因となる場合が報告されている。
自己免疫仮説:抗ペルオキシレドキシン3(PRDX3)抗体が急性期に検出され、寛解後に消失することが示されている。RPE・視細胞タンパク質に対する自己抗体が病態に関与すると考えられる。
原因不明例:全身検査・遺伝子検査がいずれも陰性の純粋な特発性例も存在する。1)
副腫瘍性
メラノーマ:皮膚黒色腫・脈絡膜黒色腫が最も多い原因悪性腫瘍である。
その他の悪性腫瘍:肺癌・乳癌・結腸癌などとの関連が報告されている。
免疫チェックポイント阻害薬:BRAF阻害薬(ベムラフェニブ、ダブラフェニブ)やPD-1阻害薬(ペムブロリズマブ、ニボルマブ)の使用に関連して発症する場合がある。
発症機序:腫瘍抗原と網膜抗原の交差反応(分子擬態)により、RPEや視細胞に対する自己免疫反応が引き起こされると考えられている。
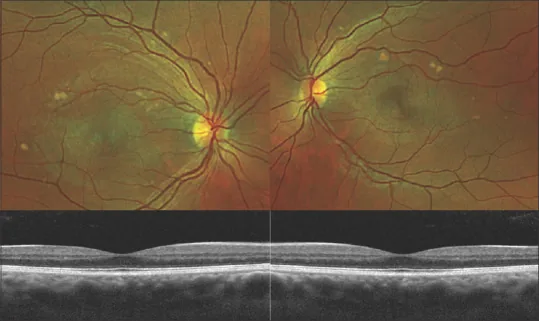
AEPVMの診断は除外診断であり、類似疾患を体系的に除外する過程が必要である。マルチモーダルイメージングの組み合わせが診断の要となる。1)
画像検査
OCT(光干渉断層計):ドーム状の神経感覚網膜剥離と、高反射または等反射の網膜下沈着物を検出する。回復期には漿液の消失とRPEの再接着が確認できる。楕円体層(ellipsoid zone)の肥厚も認められる。1)
FAF(自発蛍光検査):卵黄状物質が高自発蛍光を示す。診断において最も重要な検査である。1)リポフスチンや蛍光色素の蓄積を反映する。
FA(蛍光眼底造影):卵黄状物質は低蛍光または無蛍光を呈する。FAFとは反転したパターンを示す点が特徴的である。漏出所見は認めない。
機能・遺伝子検査
FAと自発蛍光検査(FAF)の反転パターンは本疾患の特徴的な所見である。
| 所見 | FA | FAF |
|---|---|---|
| 卵黄状物質 | 低蛍光 | 高自発蛍光 |
| 漿液部分 | 軽度高蛍光 | 蛍光なし |
AEPVMは以下の疾患との鑑別が重要である。
Best病はBEST1遺伝子の変異による遺伝性疾患であり、遺伝子検査で鑑別できる。AEPVMでは次世代シークエンシングによる遺伝子検査でBEST1・PRPH2変異が陰性となる。1)また発症経過(急性発症か緩徐か)や家族歴も鑑別の参考になる。
AEPVMには確立された薬物療法は存在しない。特発性AEPVMは自己限定性(self-limiting)疾患であり、自然経過での回復が期待できる。
特発性AEPVMは自己限定性疾患であり、多くの症例で視力の自然回復が見込まれる。Fernandes et al.の症例では、6ヶ月後に両眼の最良矯正視力が20/25まで改善し、OCTで網膜下液の完全消失が確認された。1)ただし回復の程度は症例により異なる。
AEPVMの正確な発症機序は未解明の部分が多い。現在提唱されている主な仮説は以下の通りである。
網膜色素上皮(RPE)の機能不全がリポフスチン蓄積を引き起こし、漿液性網膜剥離をもたらす。神経感覚網膜とRPEが物理的に分離されることで、視細胞外節の正常な貪食機能が障害される。脱落した視細胞外節が網膜外層・網膜下腔に蓄積するとされる(Spaide仮説)。FAFで観察される高自発蛍光は、こうしたリポフスチン・蛍光色素の蓄積を反映する。
RPE・視細胞タンパク質に対する自己抗体が病態に関与すると考えられている。推定される自己抗体の標的抗原として以下が報告されている。
副腫瘍性では、腫瘍抗原と網膜・RPEの共通抗原に対する交差免疫反応(分子擬態)が、卵黄状病変の形成を引き起こすと推測される。
カラー眼底写真・SD-OCT・FAFの組み合わせにより、侵襲的検査なしにAEPVMの臨床診断が可能になりつつある。1)各モダリティが相補的な情報を提供し、特にFAFとFAの反転パターンが診断の鍵となる。
次世代シークエンシングパネルの活用により、BEST1・PRPH2などの遺伝子変異を網羅的に検索できる。遺伝子検査の標準化は除外診断の精度向上に寄与する。1)
BRAF阻害薬(ベムラフェニブ、ダブラフェニブ)やPD-1阻害薬(ペムブロリズマブ、ニボルマブ)の普及に伴い、これら薬剤と副腫瘍性AEPVMの関連が新たな臨床課題として浮上している。免疫治療の普及とともに、副腫瘍性AEPVMの報告例が増加する可能性がある。
文献上の特発性AEPVM症例は約20例にとどまる。1)病因解明・治療法開発のためには、多施設共同による症例集積と大規模前向き研究が必要である。
Fernandes et al.(2023)は、60代男性の特発性AEPVM症例において、全身検査と次世代シークエンシングパネルによる遺伝子検査がいずれも陰性であったことを報告した。6ヶ月後に最良矯正視力は両眼20/25まで改善し、SD-OCTで網膜下液の完全消失が確認された。1)