前部RON

放射線視神経症
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. 放射線視神経症とは
Section titled “1. 放射線視神経症とは”放射線視神経症(radiation optic neuropathy: RON)は、視器(optic apparatus)への放射線照射後に生じる遅発性の虚血性変化による視神経障害である。視器は放射線感受性が高く、血管内皮障害を主体とした機序で視機能が失われる。
好発部位は視交叉またはその前後であり、前部RON(anterior RON)と後部RON(posterior RON)に分類される。前部RONは眼窩・脈絡膜・網膜腫瘍に対する陽子線治療やプラーク小線源治療から生じ、後部RONは副鼻腔や頭蓋底腫瘍の治療に起因する。
疫学と安全線量
Section titled “疫学と安全線量”発症リスクは照射線量と密接に関連する。以下に線量と発症リスクの目安を示す。
| 照射条件 | 発症リスク |
|---|---|
| 総線量5,000 cGy未満 | 稀 |
| 総線量5,000〜6,000 cGy | 10年以内に最大5% |
| 1回線量2 Gy以下・総線量50 Gy以下 | 比較的安全 |
| ガンマナイフ 800〜1,000 cGy単回(1〜3セッション) | 比較的安全 |
発症時期は照射後3か月〜数年と幅があり、ほとんどは3年以内に発症する。ピークは照射後1.5年、最も一般的な発症は治療後8〜16か月とされる。ガンマナイフの普及により、RONの発生頻度は著明に低減した。
総線量5,000 cGy(50 Gy)未満の分割照射では発症は稀である。5,000〜6,000 cGyでは10年以内に最大5%の確率で発生するとされる。1回線量2 Gy以下・総線量50 Gy以下であれば比較的安全とされており、照射計画の立案においてこれらの値が基準となる。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”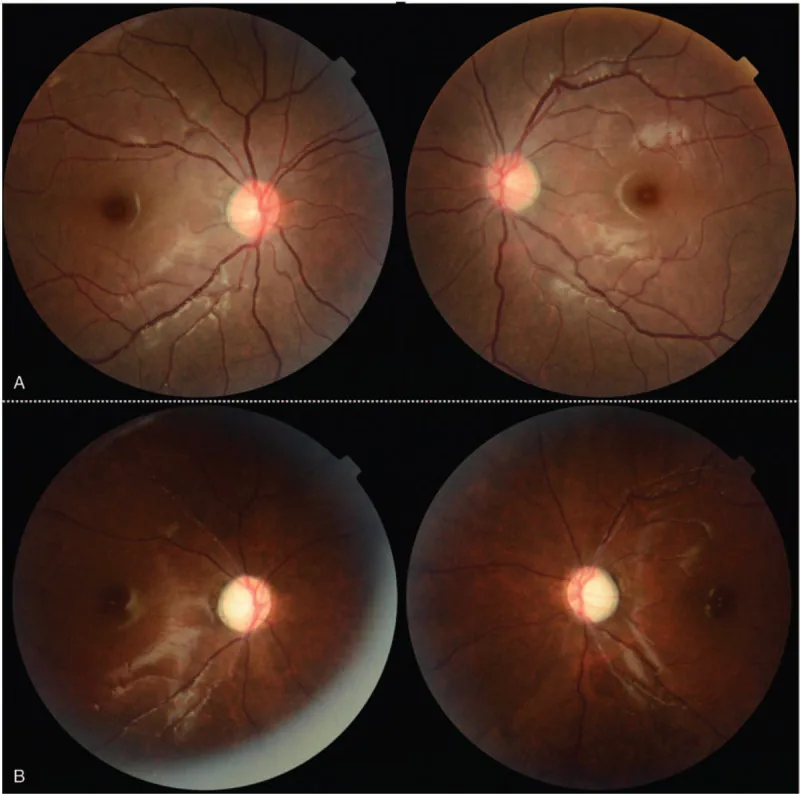
- 視力低下:数週間にわたる進行性かつ急速な視力低下として発症する。片側性または両側性に生じ、通常無痛性である。
- 色覚障害:色覚異常も一般的に認められる。
- 発症様式:急性(治療中)、早期遅発性(照射後3か月)、晩期遅発性(照射後6か月〜10年)に分類される。
- 両眼性の場合:2番目の眼の症状は数週間以内に出現することが多い。
後部RON
正常または蒼白の視神経:後部RONでは眼底所見が乏しく、視神経は正常または蒼白を呈する。
視野欠損のパターン:視交叉損傷では耳側半盲、視索損傷では対側同名半盲+帯状萎縮を呈する。
- RAPD:片側性または非対称性の損傷では相対的輸入瞳孔欠損(RAPD)を認める。
42歳女性(乳癌脳転移に対し50 Gy照射)の症例では、照射後1年で右眼に上方高度視野欠損・下方分節性視神経蒼白・RAPD陽性が認められた。最終的に右眼は光覚のみ(amaurotic pupil)の状態となった1)。
74歳女性(髄膜腫切除後54 Gy照射)の症例では、照射後22か月の時点で左眼視力20/20と無症候性であったにもかかわらず、OCTでpRNFL・GCIPL菲薄化が検出された2)。
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”放射線は分子結合の直接破壊と、フリーラジカル発生による間接障害の2経路で細胞を障害する。Bergonie-Tribondeauの法則に示されるように、細胞分裂頻度が高く未分化な細胞ほど放射線に障害されやすい。血管内皮細胞への障害が、血管透過性の亢進と毛細血管の閉塞をもたらし、最終的に虚血性視神経障害を引き起こす。
- 照射線量:総線量・1回線量・照射間隔がいずれもリスクに関与する。
- 糖尿病:虚血性血管疾患リスクが高く、RON発症リスクが上昇する。
- 高血圧・既存の血管病変:もともと血管に病変のある症例ではリスクが高まる。
- 化学療法の併用:放射線障害を増強する可能性がある。
- 患者の年齢:年齢もリスク因子の一つとされる。
糖尿病患者は虚血性血管疾患のリスクが高いため、RON発症リスクが上昇するとされる。高血圧や既存の血管病変も同様にリスク因子となる。化学療法との併用もリスクを高める可能性があり、これらの要因が重複する症例では特に慎重な照射計画と経過観察が求められる。
4. 診断と検査方法
Section titled “4. 診断と検査方法”放射線視神経症は除外診断であり、類似疾患を鑑別したうえで診断する。
主な鑑別疾患として以下が挙げられる。
- 圧迫性視神経症・腫瘍再発による視神経圧迫
- 浸潤性視神経症、癌性髄膜炎
- 化学療法に続発する中毒性視神経症
- 副腫瘍性視神経症、クモ膜炎
- 巨細胞性動脈炎(高齢者での鑑別)
腰椎穿刺による髄液検査(癌性髄膜炎の除外)や血清学的検査(副腫瘍症候群の検索)が必要となることもある。
- MRI(第一選択):視神経疾患にはMRIが第一選択であり、STIR画像とGd造影T1強調画像の冠状断が有用である。3T・3 mm以下の薄切が推奨される。罹患視神経の造影増強を認める。初期には腫瘍再発との鑑別が困難な場合もある。2)で報告された症例でも、T1造影MRIで左前交叉視神経の膨隆・造影増強が確認された。
- OCT:pRNFL・GCIPL菲薄化を検出でき、症候性になる前に変化を捉える可能性がある2)。放射線治療後のスクリーニングツールとしての有用性が示唆されている。
- OCT-A(光干渉断層血管撮影):乳頭周囲放射状毛細血管網(RPCP)の変化に基づく0〜4のグレーディングスケールが提唱されており、非侵襲的な評価法として注目される。
以下にOCT-Aグレーディングスケールの概要を示す。
| グレード | 所見 |
|---|---|
| 0 | RPCPの規則的な放射状分布 |
| 1 | RPCPの初期放射状パターン消失 |
| 2 | 2象限未満の乳頭周囲低灌流 |
| 3 | 2象限以上の低灌流 |
| 4 | 全4象限のびまん性低灌流 |
グレード1〜3には「+」サブ分類(乳頭黄斑線維束の関与)があり、視力低下と相関する。
OCTによるpRNFL・GCIPL菲薄化の検出により、自覚症状が出現する前に変化を捉えられる可能性がある2)。MRIでは罹患視神経の造影増強が確認される。放射線治療後の定期的な眼科モニタリングがRONの早期発見につながるとされており、外照射完了後10〜20か月のルーチンMRIモニタリングを提案する報告もある2)。
5. 標準的な治療法
Section titled “5. 標準的な治療法”根本的な治療法は基本的になく、予後は通常不良である。視神経萎縮が起きていない発症間もない症例には、以下の治療がある程度有用とされる。
- ステロイド全身投与:発症初期に行う。プレドニゾロン50 mg/日の投与が行われた症例が報告されている1)。プレドニゾン60 mg/日×4週間で治療された症例もある2)。ただし、ステロイドや抗凝固療法はRONに対して成功を収めていないとする報告もある。
- 抗凝固療法:ヘパリンなどの抗凝固薬が用いられることがある。
- 高圧酸素療法(HBOT):血管新生を促進し虚血性壊死の進行を抑制する目的で行われる。症状出現後できるだけ早期(約72時間以内)に2〜3気圧のほぼ100%酸素を30〜60分間施行する。副作用として気圧外傷・気管支肺毒性・発作・ドライアイ・可逆的近視化がある。費用が高く、中止後に再進行が起こる場合もある。
- 罹患眼の45%で最終視力が20/200未満〜光覚弁となる。
- 最終視力が光覚なしに至る症例は約半数である。
- 片側性または両側性の永久的失明に至る可能性がある。
根本的な治療法はなく、予後は通常不良である。罹患眼の45%で最終視力が20/200未満〜光覚弁となり、約半数が光覚なしに至る。ステロイド全身投与・高圧酸素療法・抗凝固療法が発症間もない症例に対してある程度有用とされるが、いずれも視機能回復を保証するものではない。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”RONの発症機序には、血管損傷(放射線血管炎)と視器への直接放射線損傷の両方が関与する。初期損傷が血管系に現れるか神経実質に現れるかは未解明の部分が残る。
病期別の変化
Section titled “病期別の変化”初期段階(数週間以内)
可逆的な炎症と滲出性血管障害:血管透過性の亢進が中心。この段階での変化は可逆的とされる。
進行段階(数か月〜数年)
血管閉塞・内皮細胞増殖:フリーラジカル損傷が加わる。
微小血管不全:低酸素を伴う微小血管不全が誘発される。細胞DNA・血液脳関門への直接損傷も生じる。
不可逆段階
脱髄と反応性アストロサイトーシス:周囲神経への損傷が広がり、不可逆的な視機能喪失に至る。
放射線による細胞障害は2経路で生じる。第1は分子結合の破壊による直接障害、第2はフリーラジカル発生による間接障害である。Bergonie-Tribondeauの法則に基づき、細胞分裂頻度が高く未分化な細胞ほど障害を受けやすい。血管内皮細胞への損傷が毛細血管透過性の亢進と閉塞をもたらし、局所VEGF上昇と炎症反応を介して虚血性視神経障害が完成する。
7. 最新の研究と今後の展望(研究段階の報告)
Section titled “7. 最新の研究と今後の展望(研究段階の報告)”抗VEGF療法(ベバシズマブ)
Section titled “抗VEGF療法(ベバシズマブ)”内皮細胞障害に伴う局所VEGF上昇を標的とした治療として、ベバシズマブが注目されている。全身投与(3週間ごとに1回、計4回)または硝子体内投与(6〜8週間ごとに最低2回)が報告されており、3年間にわたり視力と色覚を安定的に改善したとする報告がある。
ペントキシフィリン
Section titled “ペントキシフィリン”メチルキサンチン誘導体であるペントキシフィリン(Trental)は血液粘度を修飾し循環改善を助ける可能性が示されており、有望な結果が報告されている。実際の症例報告でもペントキシフィリン1,200 mg/日が処方されている2)。
その他の研究
Section titled “その他の研究”ACE阻害薬(ラミプリル)を放射線照射2週間後から約6か月間投与すると、炎症性サイトカインの放出が減少するとの報告がある。ただし、現時点ではラットモデルのみで示されており、ヒトへの適用は未確立である。
ビタミンEはin vitro研究において活性酸素生成の減少と線維化の阻害が示されているが、臨床的なエビデンスは限定的である。
OCT・OCT-Aによる早期検出の展望
Section titled “OCT・OCT-Aによる早期検出の展望”OCTでpRNFL・GCIPLの菲薄化を検出することで、症候性になる前に放射線視神経症を診断できる可能性がある2)。OCT-Aによるグレーディングスケールも、非侵襲的な経過観察ツールとして今後の活用が期待される。国際的なレジストリの確立により、臨床プロファイルのさらなる解明が進むと考えられる。
8. 参考文献
Section titled “8. 参考文献”- Abduraman S, Mali B, Celebi ARC. Taxane-associated retinopathy and radiation-induced optic neuropathy in a young female patient with metastatic breast cancer. GMS Ophthalmol Cases. 2025;15:Doc07.
- Grosinger A, Chen JJ, Link MJ, Bhatti MT. Detection of asymptomatic radiation induced optic neuropathy with optical coherence tomography. Neuroophthalmology. 2021;45(5):339-342.
