傍腫瘍症候群(PNS)の眼科的症状は、腫瘍の直接侵襲ではなく腫瘍抗原への自己免疫反応によって生じる。
癌関連網膜症 (CAR)の約50%では、がんの診断よりも先に眼症状が出現する。CARの主な原因は小細胞肺がん、MARの原因は悪性黒色腫のみである。
CARとMARは網膜電図 パターンで鑑別できる。CARはa波・b波ともに低下、MARはnegative 網膜電図(a波正常、b波低下)が特徴。
確立された治療法は存在せず、基礎悪性腫瘍の治療が最優先となる。
50歳以上で遺伝歴のない網膜色素変性 様所見では、本症を疑って全身精査が不可欠である。
視覚的予後は全体として不良で、多種多様な治療でも予測不可能な経過をたどる。
傍腫瘍症候群(paraneoplastic syndromes; PNS)は、がん組織やその転移による直接的症状ではなく、腫瘍関連抗原に対する宿主免疫が正常組織と交叉反応して生じる症候群の総称である。眼科領域では網膜 ・視神経 ・眼運動系など多様な部位が侵される。
眼科的PNSの主な病型は以下の通りである。
CAR(癌関連網膜症) :主に杆体視細胞 の障害を呈する。中枢神経系に特異な蛋白質が腫瘍組織に異所性発現し、自己免疫を獲得して網膜視覚系を障害する。MAR(癌関連黒色腫網膜症) :網膜双極細胞の障害を主体とし、先天停在性夜盲 に類似した表現型を示す。PON(傍腫瘍性視神経症) :視神経を標的とし、CRMP-5抗体との関連が代表的である。BDUMP(両眼びまん性ぶどう膜黒色腫細胞増殖症) :急激な視力 喪失と網膜剥離 を呈する。OMS (眼球振盪 様ミオクローヌス症候群) :眼振とミオクローヌスを特徴とする。LEMS(Lambert-Eaton筋無力症候群) :電位依存性カルシウムチャネル抗体(VGCCA)が関与する。
CARに関連する主な悪性腫瘍は小細胞肺がんが最多で、消化器系・婦人科系のがんがこれに続く。性差はない。MARの原因は悪性黒色腫のみであり、本邦でも報告がある。その他のPNSでは非小細胞肺がん、乳がん、子宮がん、甲状腺がん、リンパ腫などが関連する。
がんの種類によって発症時期が異なる。リンパ腫・肺がんでは数週〜数ヶ月で網膜症が発症するのに対し、乳がん・前立腺がんでは数年かかることもある。
Q がんと診断される前に眼症状が出ることはあるか?
A CARでは約50%の症例でがん診断より先に眼症状が出現する。原因不明の進行性視力低下をきっかけに精査を行い、悪性腫瘍が発見されることがある。
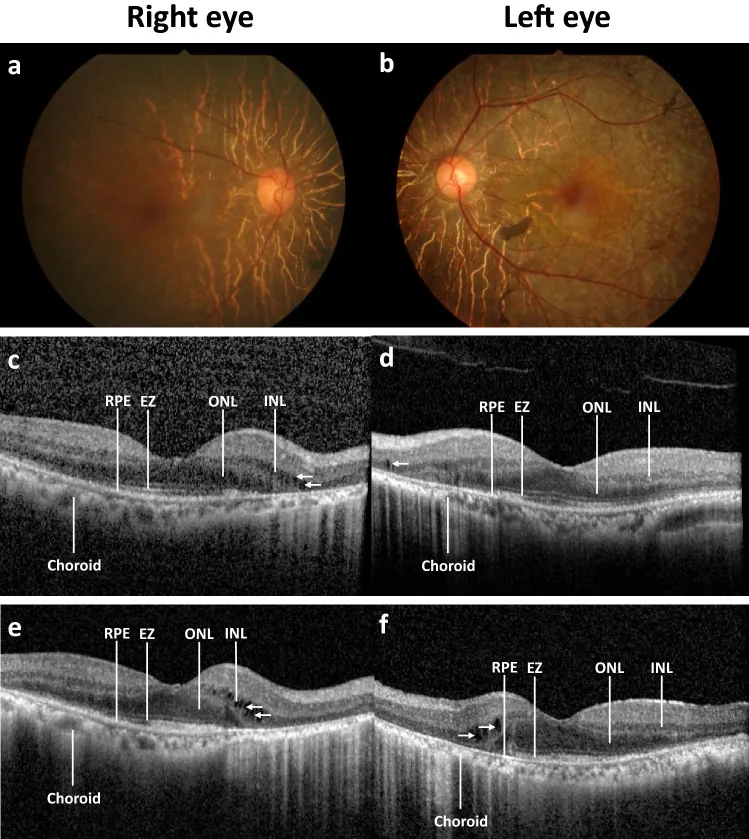
paraneoplastic autoimmune retinopathy fundus oct series Autoantibody profiles and clinical association in Thai patients with autoimmune retinopathy. Sci Rep. 2021 Jul 22; 11:15047. Figure 1. PMCID: PMC8298708. License: CC BY.
Disease progression of a patient with autoimmune retinopathy (AIR). Color fundus photography at baseline in the right (a) and left eye (b) shows normal optic disc, arteriolar attenuation, generalized retinal pigment epithelium (RPE ) atrophy with macular sparing and scattered pigment clumps. Prominent large choroidal vessels can be observed around the optic disc. Optical coherence tomography images at baseline showing RPE attenuation, loss of ellipsoid zone (EZ ) at the periphery, flattening of the outer nuclear layer (ONL), and slit cavitation in the inner nuclear layer (INL) on the nasal side, as marked by arrows, in the right (c) and left eye (d). The disease progression after five years is marked with RPE atrophy, progressive loss of EZ and ONL toward the fovea, more prominent slit cavit
CAR・MAR・PONに共通する主な自覚症状は以下の通りである。
無痛性の進行性視力低下 :両側性であることが多いが、非対称な場合もある。夜間視力の低下 :特にMARで顕著であり、先天停在性夜盲に類似する。光視症 ・光過敏症色覚識別の悪化 :色の識別が困難になる。視野異常 :CARでは輪状暗点・中心暗点 ・視野狭窄を呈する。周辺視野喪失 :MARで比較的目立つ所見。
疾患の種類によって特徴的な眼底所見および検査所見が異なる。
CAR
視神経乳頭蒼白 :萎縮を反映した蒼白化。
網膜動脈の狭小化 :血管の細小化が認められる。
色素上皮のmottling :RPEの不規則な変化。
骨小体様色素沈着 :網膜色素変性に類似した所見。
硝子体 中の軽度細胞浸潤
MAR
夜盲 の優位
光視症 :持続的な閃光感を訴えることが多い。
眼底は初期正常に近い :進行しても比較的眼底変化に乏しい場合がある。
negative 網膜電図 :a波はほぼ正常、b波が著しく低下する(双極細胞障害を反映)。
PON
視神経乳頭浮腫 :CRMP-5抗体関連に特徴的。
視神経萎縮
網膜炎・硝子体炎症細胞 :CRMP-5関連では網膜炎と硝子体の炎症細胞を伴う2) 。
BDUMP
急激な視力喪失 :急速な経過が特徴。
斑状の赤色眼底 :びまん性の眼底変化。
滲出性網膜剥離
PNSの病因は、腫瘍組織に異所性に発現した神経系抗原が免疫系に認識されることによる自己免疫機序である。腫瘍関連抗原に対する自己抗体が産生され、同じ抗原を持つ正常神経・網膜組織を攻撃する。
主な原因悪性腫瘍と関連する病型は以下の通りである。
小細胞肺がん :CAR・PON・抗Hu抗体関連症候群の最多原因。悪性黒色腫 :MARの唯一の原因。非小細胞肺がん・乳がん・子宮がん・甲状腺がん :CARおよびその他のPNSに関連。神経芽細胞腫 その他 :淡明細胞型腎細胞がん、リンパ腫、骨髄腫、大腸がん、前立腺がんなど。
自己抗体の種類と関連する病型は以下の通りである。
抗リカバリン抗体 :CARの最も代表的な自己抗体。α-エノラーゼ抗体 :CAR関連。アポトーシス を介して網膜神経節細胞 ・双極細胞を障害する。hsc70(熱ショック蛋白質) :CAR関連。TRP M1 :MARの抗原候補として報告されているが、未解明な点が多い。CRMP-5(CV2) :PONに関連し、広範な神経系表現型を示す。
診断の基本は、臨床症状・眼科的所見・原因自己抗体の同定の組み合わせによる。眼症状がCARの約50%でがん診断に先行するため、本症を迅速に認識することが癌の早期発見にも繋がる。
以下の所見が本症を疑うきっかけとなる。
50歳以上で遺伝歴がないのに、網膜色素変性様の眼底像・視野狭窄を呈する場合。
軽度のぶどう膜炎にもかかわらず、著しい視野狭窄・視感度低下を呈する場合。
網膜電図パターンによるCARとMARの鑑別が重要である。
疾患 a波 b波 パターン CAR 低下 低下 全体的な平坦化 MAR ほぼ正常 著しく低下 negative 網膜電図
Goldmann視野計では輪状暗点・中心暗点・中心視野狭窄が認められる。
免疫組織化学染色アッセイ・ウェスタンブロット・ELISAによる抗体検出が確定診断に必要である。抗リカバリン抗体の存在はCARの有力な根拠となる。MARの確定診断には、血清中の抗網膜双極細胞抗体の証明が必要である。
初回検査で抗体が検出されないことがある。少なくとも3回以上の繰り返し測定が必要である。
SD-光干渉断層計 (OCT) :網膜各層の変化を非侵襲的に評価する。FAF (眼底自発蛍光)・フルオレセイン 蛍光造影CT・MRI・PET :原発腫瘍の検索に用いる。脳脊髄液(CSF)分析 :神経系の関与を評価する。傍腫瘍性抗体の血清検査 :抗Ri・抗Hu・抗Yo・抗Ma2など、関連抗体を網羅的に検索する。
眼症状が原発巣より先行するため、本症が疑われたら呼吸器・消化管・泌尿器・婦人科の全身精査が不可欠である。
主な鑑別疾患として以下が挙げられる。
網膜色素変性症・錐体ジストロフィー(遺伝性網膜疾患)
非傍腫瘍性自己免疫性網膜症
AZOOR ・白点症候群中毒性網膜症・中毒性視神経症
LHON (レーバー遺伝性視神経症)栄養欠乏性視神経症・慢性中心性漿液性脈絡網膜症
ビタミンA欠乏症
Q CARとMARはどのように鑑別するか?
A 最も重要な鑑別点は網膜電図パターンである。CARではa波・b波ともに低下する全体的な平坦化を呈するのに対し、MARではa波はほぼ正常で、b波が著しく低下するnegative 網膜電図が特徴である。これは双極細胞の障害を反映している。
基礎疾患である悪性腫瘍の治療が最優先である。CARおよびMARに対する決定的な治療法は確立されておらず、視覚症状の改善を示した対照群のあるヒト研究は存在しない。
副腎皮質ステロイド IVI G(免疫グロブリン静注療法 )血漿交換 :有効例の症例報告があるが、確立された治療法ではない。その他の免疫抑制薬 :アザチオプリン ・シクロスポリン ・ミコフェノール酸モフェチル などが用いられることがある。生物学的製剤 リツキシマブ ・アレムツズマブが試みられることがある。
PNSに対する眼科手術の適応はない。基礎悪性腫瘍の摘出が基礎疾患の治療となる。胸腺腫に関連するPNSでは胸腺摘出術により症状改善のエビデンスがある。
Q 傍腫瘍症候群の眼症状に確立された治療法はあるか?
A 確立された治療法は存在しない。基礎悪性腫瘍の治療が最優先である。免疫抑制療法 ・IVIG・血漿交換などが試みられるが、いずれも成功事例の報告にとどまり、対照群のある研究はない。視覚的予後は全体として不良であることを患者に伝える必要がある。
悪性腫瘍が神経系に特有の蛋白質(リカバリンなど)を異所性に発現する。免疫系がこれを腫瘍抗原として認識し、特異抗体を産生する。この抗体が網膜視細胞上の同一抗原と交叉反応し、視細胞の変性・アポトーシスを引き起こす。
CARで報告されている主な自己抗体と標的は以下の通りである。
自己抗体 主な標的細胞 主な関連がん 抗リカバリン 杆体・錐体視細胞 小細胞肺がん α-エノラーゼ 網膜神経節細胞・双極細胞 小細胞肺がん 抗hsc70 視細胞 各種がん
α-エノラーゼ抗体はアポトーシスを介して網膜神経節細胞・双極細胞の死を誘導する。
CRMP-5(CV2)-IgG抗体は末梢・中枢神経系の広範な表現型を示し、典型的には傍腫瘍性で小細胞肺がんが最多である1) 。CRMP-5関連の視神経炎 では、両側性の視神経乳頭浮腫が特徴であり、網膜炎と硝子体の炎症細胞を伴う2) 。視神経炎としての最も一般的な機序は、細胞内カルシウム流入を含むカスケード依存性経路を介した視細胞アポトーシスとされている。
抗リカバリン抗体が関与する視神経炎の症例報告もある3) 。
抗Hu抗体 :脳幹・小脳・側頭葉を侵し、緊張瞳孔 ・眼筋麻痺を呈する。小細胞肺がんが典型。抗Yo抗体 :主に小脳に影響し、OMS関連所見(眼振・oscillopsia)を呈する。抗AChR・横紋筋抗体 :胸腺腫に関連した重症筋無力症 (MG)様の複視 ・眼瞼下垂 を呈する。VGCCA :LEMSに関連し、軽度のドライアイ ・眼運動異常を呈する。
Q どのような自己抗体が眼症状を引き起こすか?
A 抗リカバリン・α-エノラーゼ・hsc70などがCARに関与し、CRMP-5がPONの代表的な原因抗体である。このほかにも抗Hu・抗Yo・抗AChR・VGCCA抗体などが各病型に対応する。自己抗体の種類によって症状パターンや関連がんが異なる(詳細は「診断と検査方法」の項 参照)。
Kaushikら(2024)は、抗リカバリン抗体陽性の視神経炎に対し、化学療法・ステロイド・血漿交換の組み合わせが奏効した症例を報告した3) 。確立された標準治療ではないが、多角的な治療アプローチが有効な可能性を示す事例として注目されている。
CARのモデルラットにおいて、カルシウム拮抗薬が有効である可能性が示唆されている。視細胞アポトーシスへの細胞内カルシウム流入の関与を示す知見であり、今後の治療開発の基礎となりうる。
PNSを伴う腫瘍は、PNSを伴わない腫瘍より予後良好である可能性が指摘されている。自己免疫応答が同時に抗腫瘍免疫として機能している可能性があり、早期がん発見との関連が示唆されている。一方、視覚的予後は全体として不良であり、多種多様な治療でも予測不可能な経過をたどる点が課題である。
Wang S, Hou H, Tang Y, et al. An overview on CV2/CRMP5 antibody-associated paraneoplastic neurological syndromes. Neural Regen Res. 2023;18:2357-64.
Cross SA, Salomao DR, Parisi JE, et al. Paraneoplastic autoimmune optic neuritis with retinitis defined by CRMP-5-IgG. Ann Neurol. 2003;54:38-50.
Kaushik M, Virdee J, Giridharan S, et al. Response of Recoverin-Positive Optic Neuritis to Chemotherapy, Steroid, and Plasma Exchange. J Neuro-Ophthalmol. 2024;44:e79-e81.
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト) してください