全身性毛細血管漏出症候群(SCLS、クラークソン病)は1960年以降500例未満しか報告されていない稀疾患である。
低血圧・低アルブミン血症・血液濃縮の三徴を特徴とし、最大80%にMGUS(意義不明の単クローン性ガンマグロブリン血症)を合併する。
主な眼所見は結膜 浮腫・脈絡膜 滲出・眼圧 上昇であり、重度の結膜浮腫は露出性角膜症 のリスクとなる。
毛様体 滲出による急性閉塞隅角 は、偽水晶体 眼でも発生しうる。NAION (非動脈炎性前部虚血性視神経症)の合併例では永続的な視野欠損 が残ることがある。発作予防にはIVI Gの月次投与が有効であり、IVIG投与群の5年生存率は91%に達する。
TLN1遺伝子変異による内皮バリア破綻が家族性SCLSの発症機序として近年同定された。
全身性毛細血管漏出症候群(Systemic Capillary Leak Syndrome; SCLS)は、毛細血管から組織への一過性かつ重度の水分・大分子漏出を特徴とする稀な疾患である。1960年にClarksonが初めて報告したことから「クラークソン病」とも呼ばれる。1960年以降の報告例は500例未満であり2) 、診断時の患者の中央値は48歳、高齢男性に多い傾向がある。
特発性SCLSの最大80%にMGUS(意義不明の単クローン性ガンマグロブリン血症、主にIgG型)が合併するが、骨髄腫への進行リスクは増加しないとされる。
水分漏出はあらゆる組織で起こりうるため、眼科的合併症も多彩である。主な眼所見として結膜浮腫・脈絡膜滲出・眼圧上昇が挙げられる。急性閉塞隅角や非動脈炎性前部虚血性視神経症(非動脈炎性前部虚血性視神経症)を合併した重篤な症例も報告されている1) 。
Q SCLSはどのくらい稀な疾患か?
A 1960年以降の世界での報告は500例未満とされ、きわめて稀な疾患である2) 。診断時の年齢中央値は48歳で、高齢男性に多い。希少性ゆえに診断が遅れやすい点に注意が必要である。
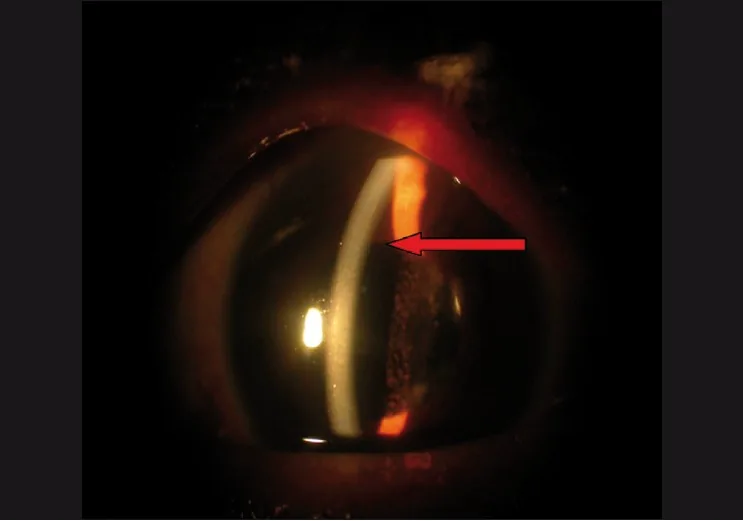
systemic capillary leak syndrome deep anterior chamber Management of complications in glaucoma surgery. Indian J Ophthalmol. 2011 Jan; 59(Suppl1):S131-S140. Figure 4. PMCID: PMC3038515. License: CC BY.
Responded to medical therapy, note the deep anterior chamber
前駆症状 :非特異的な軽度症状(呼吸器感染様)が漏出期の1〜4日前に出現する2) 。息切れ・倦怠感 :肺水腫・胸水による呼吸困難と全身的な衰弱。全身性浮腫 :末梢を中心とした急激な浮腫。
流涙・羞明 ・異物感・痒み :結膜浮腫(chemosis)による。視力 は保たれることが多い。視力低下・眼痛 :脈絡膜滲出+急性閉塞隅角を呈した症例で報告されている。上方視野欠損 :非動脈炎性前部虚血性視神経症合併例では、SCLS回復期に両側対称性の上方弓状視野欠損が明らかとなる1) 。
前眼部・外眼部
眼瞼浮腫・眼窩 周囲浮腫 :顔面の腫れを伴う。眼球突出 (眼窩充血による)を来すこともある。
結膜浮腫(chemosis) :非常に重度になることがあり、兎眼 ・露出性角膜症のリスクとなる。結膜血管の拡張・蛇行を伴う。
浅前房 ・隅角閉塞 :毛様体滲出による毛様体前方回旋が原因。瞳孔ブロック 機序ではなく、偽水晶体眼でも発生しうる。
眼圧上昇 :強膜 上静脈圧の上昇も寄与する。
後眼部・視神経
脈絡膜滲出 :血清アルブミンの急激な低下による膠質浸透圧の低下が原因。しばしば両側性。
毛様体滲出 :後眼部から毛様体への広汎な滲出。
視神経乳頭 蒼白(非動脈炎性前部虚血性視神経症例)1) 。
RNFL 菲薄化(非動脈炎性前部虚血性視神経症例)OCT で下方のRNFL菲薄化が両眼に認められる1) 。
Q SCLSで視力が永久に低下することはあるか?
A 非動脈炎性前部虚血性視神経症を合併した症例では永続的な視野欠損が残る場合がある。報告例では両側対称性の上方弓状視野欠損を呈しつつも、中心視力は両眼とも6/7.5(約0.8)に保たれた1) 。一方、結膜浮腫・脈絡膜滲出・閉塞隅角による視力低下は全身状態の改善とともに回復することが多い。
SCLSの原因は大部分が特発性(原因不明)である。特発性以外に以下の誘因が報告されている。
薬剤誘発性 :ゲムシタビン、クロファラビンなどの抗がん剤、モノクローナル抗体、治療用成長因子。デニロイキンジフチトクス(CTCL治療薬)では臨床試験で36%にSCLSが発現している9) 。ウイルス感染 :インフルエンザA・B、帯状疱疹、デング熱。非動脈炎性前部虚血性視神経症合併の症例報告ではインフルエンザBが確認されている1) 。COVID-19関連 :COVID-19感染自体に加え、AstraZeneca・Johnson & Johnson-Janssen・Pfizer-BioNTechワクチンでの発症が報告されている7) 8) 。欧州医薬品庁(EMA)はAstraZenecaワクチンをSCLS既往者に禁忌と勧告している7) 。減圧症 :潜水後の減圧症に続発したSCLSが報告されている6) 。悪性腫瘍 :びまん性大細胞型B細胞リンパ腫(DLBCL)などによる傍腫瘍症候群としてのSCLS3) 。遺伝的背景 :TLN1遺伝子のスプライス部位変異(c.7188+2T>C)が家族性SCLSで同定されている。常染色体優性・不完全浸透の形式をとる4) 。
非動脈炎性前部虚血性視神経症を合併しやすいリスク因子として、SCLSによる低血圧・血液濃縮・凝固亢進状態に加え、糖尿病・高血圧・動脈硬化・小型のcrowded discが挙げられる1) 。
SCLSの発作予防にはIVIG(静脈内免疫グロブリン)の月次投与が最も有効です。
COVID-19ワクチン(特にアデノウイルスベクター型)はSCLS既往者への接種に注意が必要です。接種前に必ず主治医に相談してください。
インフルエンザなどのウイルス感染が発作の誘因となるため、感染予防に努めましょう。
Q COVID-19ワクチンはSCLSの原因となるか?
A アデノウイルスベクター型・mRNAワクチン両方での発症例が報告されている7) 8) 。因果関係は未確立だが、EMAはAstraZenecaワクチンをSCLS既往者に禁忌と勧告している。SCLS既往者はワクチン接種前に主治医への相談が必要である。
SCLSは除外診断であり、全身性浮腫・難治性低血圧など毛細血管漏出徴候の存在と他疾患の除外に基づいて診断する。
急性期に特徴的な検査値異常として以下が認められる。
低アルブミン血症 (蛋白尿を伴わない):平均約1.7 g/dL2) 。重症例ではアルブミン16 g/L5) 、18 g/L8) の報告もある。血液濃縮 :ヘマトクリット上昇(平均約60%)。重症例ではHt 69%5) 、Ht 72.3%8) に達することがある。MGUS :血清蛋白電気泳動(SPEP)で最大80%に検出される。IgG-κ2) 5) やIgG-λ1) が多い。血栓塞栓症リスク :血液濃縮による凝固亢進状態。深部静脈血栓・下大静脈血栓8) 、肺塞栓2) の合併例あり。急性腎障害(AKI) :一部の症例で発症9) 。
99mTc-HSAシンチグラフィでは四肢皮下への24時間後のHSA集積により、血管透過性亢進を直接証明できる9) 。
細隙灯顕微鏡検査 :結膜浮腫の程度、浅前房・隅角閉塞の有無を評価する。Bモード超音波 :脈絡膜滲出の有無と程度を確認する。Humphrey視野検査 :上方弓状視野欠損(非動脈炎性前部虚血性視神経症合併例)の検出1) 。光干渉断層計(OCT) :下方網膜神経線維層の菲薄化(非動脈炎性前部虚血性視神経症合併例)の定量評価1) 。頭部・眼窩MRI :局所梗塞・腫瘤病変の除外に使用する1) 。
主な鑑別疾患は以下の通りである。
敗血症・アナフィラキシー・血管性浮腫 :最も重要な鑑別。ネフローゼ症候群 :SCLSでは高度蛋白尿を認めない点で鑑別できる。卵巣過剰刺激症候群(OHSS) :女性患者での鑑別が必要。血球貪食性リンパ組織球症(HLH) :ウイルス性出血熱、蛇毒も考慮する。遺伝性血管性浮腫 :C1エステラーゼインヒビターが正常であれば除外できる6) 。
輸液管理 :晶質液が第一選択。過剰輸液は肺水腫・コンパートメント症候群のリスクとなる。「許容的低血圧」戦略として収縮期血圧70 mmHg未満の場合にのみ高分子膨張剤を検討する6) 。昇圧剤 :ノルエピネフリン等を使用する。全身ステロイド ・IVIG(急性期) :1〜2 g/kg/日×2〜3日間のIVIG投与が行われる。血栓塞栓症予防 :血液濃縮による凝固亢進状態に対して予防的に実施する。
発作予防の主な選択肢を以下に示す。
IVIG(静脈内免疫グロブリン) :最大2 g/kg/月の定期投与。MGUS合併SCLS患者のIVIG群では5年生存率91%・10年生存率77%に対し、非IVIG群では5年47%・10年37%と有意差がある。IVIG治療下での年間発作頻度中央値は0(範囲0〜3.3)8) 。β2刺激薬(テルブタリン)+テオフィリン :cAMP上昇による内皮透過性抑制を期待して使用される。テルブタリン5 mg×3回/日、テオフィリン400〜1600 mg/日6) 。ただし治療下での年間発作頻度中央値は2.25(範囲0〜20)とIVIGより劣る8) 。メチルプレドニゾロンパルス+IVIg 併用 :mPSL 1000 mg/日×3日間+IVIg 1 g/kgの投与が報告されている8) 。
Q SCLSの発作予防に最も有効な治療法は?
A IVIG(静脈内免疫グロブリン)の月次投与が最も有効とされる。IVIG群の5年生存率91%に対し、非IVIG群では47%と大きな差がある。年間発作頻度もIVIG群では中央値0と優れた抑制効果を示している8) 。
脈絡膜・毛様体滲出 :全身および局所(点眼・眼周囲)ステロイドが使用され、一部の報告で奏効する。良好な反応が得られない症例シリーズもある。眼圧管理 :局所眼圧降下薬を使用する。結膜浮腫・露出性角膜症 :人工涙液による潤滑。重症例では一時的瞼板 縫合術が検討されるが、眼窩を圧迫して眼窩コンパートメント症候群 を惹起するリスクがある。隅角閉塞 :レーザー虹彩 切開術(LPI)や白内障 手術が検討されるが、偽水晶体眼でも毛様体滲出により隅角閉塞が持続しうるため注意を要する。脈絡膜滲出に対する手術・レーザー :通常、抵抗性を示す。SCLSに対する確立された外科的治療法は存在しない。
急性期の過剰輸液は肺水腫・コンパートメント症候群のリスクとなる。
回復期(post-leak phase)への移行を認識し、利尿薬投与開始のタイミングを逃さないようにする。
血液濃縮による血栓塞栓症(DVT・肺塞栓・脳梗塞)のリスクに留意する。
偽水晶体眼でもSCLSによる隅角閉塞が起こりうることに注意が必要である。
SCLSの最終共通経路は血管内皮機能障害である。内皮細胞間の細胞間隙が拡大し、大分子の漏出と水分の血管外漏出が生じる。
発作中には以下の変化が認められる。
単核細胞のIL-2受容体発現増加、CXCL10・CCL2・IL-1β・IL-8・IL-12の産生増加
CD8+/CD25+ T細胞濃度増加、TNF -α発現増加
VEGF-D増加5)
VEGF・アンジオポエチン2の発作中上昇5)
in vitroモデルでは、アンジオポエチン2阻害薬とIVIGが有意に内皮透過性を低下させた一方、ベバシズマブ (VEGF阻害薬 )の効果は最小限にとどまった5) 。
Elefantら(JCI Insight, 2024)は家族性SCLS患者3例でTLN1遺伝子のヘテロ接合スプライス変異(c.7188+2T>C)を同定した4) 。この変異によりエクソン54がインフレームスキップされ、talin1 R13ドメインが不安定化する。C末端アクチン結合部位(ABS3)の機能障害に伴い、VE-カドヘリンの接合部局在が著しく減少し、adherens junction(AJ)とtight junction(TJ)が断片化して内皮バリア透過性が亢進する。トロンビン刺激でSCLS変異内皮は対照の約4倍のFITC-デキストラン透過を示した。
デニロイキンジフチトクスはIL-2受容体を発現する細胞に結合し、ジフテリア毒素断片の内在化によりタンパク質合成を阻害する。SCLSは血管透過性亢進(IL-2R作用)とタンパク質合成阻害(ジフテリア毒素作用)の両方により引き起こされると考えられている9) 。
脈絡膜滲出 :血清アルブミンの急激な低下による膠質浸透圧低下が原因。毛様体滲出・閉塞隅角 :毛様体滲出 → 毛様体前方回旋 → 浅前房・隅角閉塞。瞳孔ブロック機序ではないため、偽水晶体眼でも発生しうる。眼圧上昇 :閉塞隅角に加え、強膜上静脈圧上昇も寄与する。非動脈炎性前部虚血性視神経症 :低血圧+血液凝固亢進 → 後毛様体動脈による視神経乳頭への区域性梗塞。後毛様体動脈はend arteryとwatershed zoneを形成するため、ショック時に視神経乳頭梗塞が起きやすい1) 。
Elefantら(2024)は、SCLS変異talin1を発現する内皮細胞において、スプライス切り替えアンチセンスオリゴヌクレオチドによる正常スプライシング回復が治療戦略として提案できることを示した4) 。VE-カドヘリンの接合部局在とAJの完全性が回復すれば、内皮バリア機能の修復につながる可能性がある。
SCLS患者でVEGF-D濃度上昇が記録されており、VEGFR3を介した経路が将来的な治療標的候補として挙げられている。抗VEGF療法(ベバシズマブ静脈内投与)は1症例で試みられたが臨床反応は得られなかった。一方、アンジオポエチン2阻害薬はin vitroモデルでIVIGとともに内皮透過性を有意に低下させたが、臨床報告は限定的である5) 。
mRNAワクチン・アデノウイルスベクターワクチン両方での発症が報告されているが7) 8) 、因果関係は未確立であり、さらなる研究が求められている。
Neo YN, Sobti M, Zambarakji H. Bilateral simultaneous non-arteritic ischaemic optic neuropathy: a rare complication of idiopathic systemic capillary leak syndrome (SCLS). BMJ Case Rep. 2021;14:e242847.
Correia R, Santos D, Delgado M. Idiopathic Systemic Capillary Leak Syndrome: A Clinical Case. Cureus. 2023;15(12):e50301.
Silva B, Gaspar V, Alves C, et al. Systemic Capillary Leak Syndrome as a Paraneoplastic Syndrome. Cureus. 2024;16(5):e60923.
Elefant N, Rouni G, Arapatzi C, et al. Talin1 dysfunction is genetically linked to systemic capillary leak syndrome. JCI Insight. 2024;9(24):e173664.
Bouchlarhem A, Lamzouri O, El aidouni G, et al. Consider systemic capillary leak syndrome in monoclonal gammopathy with shock. Ann Med Surg. 2021;72:103013.
Mathavan A, Mathavan A, Jones K, et al. Systemic capillary leak syndrome secondary to decompression sickness. BMJ Case Rep. 2023;16:e253045.
Yang C, Tsang MYC, Zypchen LN, et al. Pericardial effusion and systemic capillary leak syndrome late post-SARS-CoV-2 vaccination. BMJ Case Rep. 2023;16:e256527.
Inoue M, Yasue Y, Kobayashi Y, et al. Systemic capillary leak syndrome (SCLS) after receiving BNT162b2 mRNA COVID-19 (Pfizer-BioNTech) vaccine. BMJ Case Rep. 2022;15:e248927.
Horino T, Okada D, Inotani S, et al. Denileukin diftitox-induced systemic capillary leak syndrome with acute kidney injury. CEN Case Reports. 2023;12:63-67.
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト) してください