求心性障害

成人発症緩徐進行型自己免疫性糖尿病(LADA)における神経眼科学的考察
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. LADAにおける神経眼科学的考察とは
Section titled “1. LADAにおける神経眼科学的考察とは”LADA(Latent Autoimmune Diabetes in Adults)は、GAD65に対する自己抗体を有しながらT2DMの表現型を示す成人患者のサブカテゴリーとして初めて報告された疾患概念である。「1.5型糖尿病」とも呼ばれる。
**診断基準(糖尿病免疫学会IDS)**は以下の3項目からなる。
- 発症年齢30歳以上
- 少なくとも1種類の膵島自己抗体陽性
- 診断後6ヶ月間インスリン非依存
有病率は全糖尿病の2〜12%であり、T2Dとして誤診される割合は5〜10%と推定される5)。膵島細胞抗体(ICA)の発見は1974年にさかのぼり、糖尿病の分類を大きく変革した。
神経眼科学的観点からは、慢性的な高血糖による微小血管障害が糖尿病網膜症・NAION(非動脈炎性前部虚血性視神経症)・皮質脳卒中による同名半盲・眼球運動脳神経麻痺・眼振などを引き起こす。LADA患者の糖尿病網膜症有病率はT2D患者と比較して有意に低い(20.3% vs 26.4%、P < 0.001)。診断時点で網膜症を認める症例は約12%である。
LADAは自己抗体陽性でありインスリン依存へ緩やかに進行するのに対し、T2Dは自己抗体陰性でインスリン非依存が長期間続く。LADAとT2Dの両方の遺伝的・臨床的特徴を共有する「1.5型」の位置づけである。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”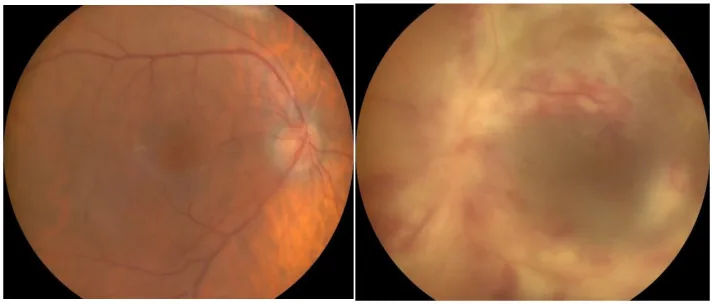
- 多尿・多食・多飲・脱水:高血糖に伴う全身症状。
- 視覚症状:糖尿病網膜症・非動脈炎性前部虚血性視神経症・皮質脳卒中による視力障害や視野欠損。
- DKA症状:ケトアシドーシスに伴う痙攣・昏睡(T1D同様の急性発症例)。
- 小繊維ニューロパチー:足から始まる痛み・灼熱感・刺痛。Aδ線維とC線維の萎縮による。
臨床所見(神経眼科学的所見)
Section titled “臨床所見(神経眼科学的所見)”遠心性障害
その他の眼所見として以下が知られる。
- 角膜異常:内皮細胞大小不同、Descemet膜皺形成。60歳以下でDescemet膜皺を認めた場合は糖尿病を疑う。
- 虹彩毛様体炎:前房に細胞を認めるだけの軽微なものが多く、ステロイド点眼で速やかに軽快する。
- 眼窩ムコール症:血糖コントロール不良患者で発症。死亡率が高く、抗真菌薬で加療する。
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”自己免疫機序
Section titled “自己免疫機序”膵島β細胞に対する自己抗体(GAD65・ICA・IA-2A・IAA)が産生され、β細胞が破壊される。インスリン欠乏へと至る過程はT1DM側とT2DM側の機序が複合している。
- T1DM共通リスク:自己免疫疾患の個人歴・家族歴、遺伝的素因(HLA-DR4-DQ8、HLA-DR3-DQ2)3)
- T2DM共通リスク:肥満・運動不足・喫煙・低出生体重・加糖飲料摂取・アルコール過剰摂取
- 合併自己免疫疾患:橋本病(甲状腺疾患有病率17.7%)5)、シェーグレン症候群4)、白斑3)、悪性貧血3)
- COVID-19関連:SARS-CoV-2がACE2受容体を介して膵β細胞への自己免疫反応を誘発する可能性がある。入院COVID-19患者の20%が入院後に新たに自己抗体を獲得したとの報告がある1)
- 肥満の促進因子:GAD65-Ab陽性でもBMIが安定であれば3年間LADA非発症の例があり、体重増加がLADA発症を促進する可能性がある4)
COVID-19後にIA2などの自己抗体が出現した症例報告がある1)。ACE2受容体を介したβ細胞傷害のメカニズムが提唱されているが、現時点では因果関係は確立されていない。
4. 診断と検査方法
Section titled “4. 診断と検査方法”自己抗体・代謝検査
Section titled “自己抗体・代謝検査”- GAD65抗体:最も感度が高い。LADA診断の主要マーカー5)
- その他の自己抗体:ICA・IA-2A・ZnT8A・テトラスパニン7
- C-peptide検査:β細胞機能の指標。C-peptide < 0.3 nmol/LはT1Dと同等のインスリン依存状態を示す
- HbA1c:反復測定による血糖コントロール評価
- CGM(持続血糖測定):血糖変動の把握2)
- 脂質プロファイル・eGFR・血清クレアチニン・シスタチンC:合併症評価
症例例として、COVID-19後LADA症例ではGAD65 < 5 nmol/L(正常)・C-peptide 2.38 ng/mL(正常)・IA2 20.6 DK units/mL(高値、正常 < 5.4)という検査値パターンが報告されている1)。
- 細隙灯顕微鏡検査:角膜異常・虹彩毛様体炎の確認
- 散瞳下眼底検査:黄斑周囲の微小血管瘤・出血・滲出物・浮腫・網膜新生血管・硝子体細胞・網膜剥離の確認
- 糖尿病乳頭症の鑑別:RAPDは陰性。水平半盲・弓状暗点を認める場合は虚血性視神経症を疑う。蛍光眼底造影で周辺部無血管域・新生血管の有無を確認する。
各糖尿病型の比較を以下に示す。
| 項目 | LADA | T1D | T2D |
|---|---|---|---|
| 発症年齢 | 30歳以上 | 35歳未満が多い | 35歳以降 |
| 自己抗体 | 陽性 | 陽性が多い | 陰性 |
| C-peptide | 正常〜低値 | 低値 | 正常〜高値 |
| インスリン依存 | 緩徐に進行 | 発症直後から | 長期間非依存 |
その他の鑑別疾患として、MODY(強い家族歴・自己抗体陰性)、LADY(若年発症緩徐進行型自己免疫性糖尿病)がある。
GAD65抗体(最も感度が高い)とC-peptide検査の組み合わせが診断に最重要である。C-peptide低値かつ自己抗体陽性でLADAを確定する。IDS分類基準(発症年齢30歳以上・自己抗体陽性・診断後6ヶ月間インスリン非依存)も診断に用いられる。
5. 標準的な治療法
Section titled “5. 標準的な治療法”全身治療(血糖コントロール)
Section titled “全身治療(血糖コントロール)”治療目標はβ細胞機能の温存と厳格な血糖コントロールである。
- C-peptide < 0.3 nmol/L:T1Dと同等のインスリンベース治療を選択する
- C-peptide高値:インスリン療法に加え、他の血糖降下薬の併用が推奨される(国際専門家パネル推奨)
- GLP-1RA(例:semaglutide)、DPP4阻害薬(例:sitagliptin)、メトホルミン
- SU薬は禁忌:β細胞の負荷を増大させ、機能悪化と血糖コントロール不良を招く5)
- SGLT2阻害薬:LADAにおける有益性は未確立
DPP4阻害薬の保護効果として、sitagliptin 100 mg/日で90歳女性のHbA1c 5.9%を1年間維持した報告がある3)。また、HbA1c 7.9→11.7%と悪化した橋本病合併LADA症例において、metformin・sitagliptin・gliclazide 120 mg/日・dapagliflozin・dulaglutideすべて無効であったが、insulin basal-bolusでHbA1c 5.7%を達成した例が報告されている5)。
網膜症治療
その他の眼合併症
糖尿病乳頭症:3〜6か月で自然寛解。特別な治療は不要。
眼筋麻痺:多くは数か月で自然治癒する。
角膜上皮欠損:術後・点眼による上皮欠損が治癒しにくい場合は、血清点眼やフィブロネクチンが奏効する。
虹彩毛様体炎:ステロイド点眼で速やかに軽快する。
SU薬はβ細胞に直接作用してインスリン分泌を強制的に促進するため、β細胞の負荷が増大し、自己免疫により消耗しつつある残存β細胞の機能をさらに悪化させる。LADAにおけるSU薬使用は血糖コントロール不良を招くことが報告されており5)、使用は禁忌とされている。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”自己抗体の種類と役割
Section titled “自己抗体の種類と役割”LADAにおける自己抗体の特徴を以下に示す。
| 抗体 | 特徴 |
|---|---|
| GAD65 | T1DM・LADA両方で最も一般的 |
| ICA | T1DM・LADA両方で陽性率高い |
| IA-2A・IAA | T1DM単独での陽性率が高い |
GAD65は膵臓膵島だけでなく、甲状腺・脳・下垂体・腎臓・肝臓・副腎・卵巣・精巣にも存在する4)。そのため高力価のGAD65抗体は甲状腺自己免疫のリスク増加と関連し、LADA患者の甲状腺疾患有病率は17.7%に達する5)。
T1DM側の機序として、遺伝的素因→免疫学的因子→自己抗体によるβ細胞アポトーシス→インスリン欠乏という経路が基本となる。T2DM側の機序として、肥満→内臓脂肪蓄積→軽度の炎症→自己免疫→β細胞機能不全が加わる。
COVID-19とβ細胞傷害の機序
Section titled “COVID-19とβ細胞傷害の機序”Lee ら(2023)は、T2DM既往の46歳男性がCOVID-19感染後にIA2抗体(20.6 DK units/mL、正常 < 5.4)が陽性となりLADAと診断された症例を報告した1)。ACE2受容体は膵外分泌腺・膵島細胞に発現しており、SARS-CoV-2のスパイクタンパクがACE2に結合してTMPRSS2によりプライミングされ、細胞内に侵入する。ACE2阻害→アンジオテンシンII上昇→NHE2持続活性化→活性酸素種増加→酸化ストレス→インスリン抵抗性・β細胞傷害という一連の機序が提唱されている。
微小血管障害と神経障害のメカニズム
Section titled “微小血管障害と神経障害のメカニズム”慢性高血糖は網膜血管を最も早期かつ高頻度に障害し、糖尿病網膜症を引き起こす。神経障害では代謝関連損傷によるAδ線維・C線維の萎縮(小繊維ニューロパチー)が足から始まる痛みや灼熱感を生じさせる。
自己免疫の連鎖(シェーグレン症候群・橋本病との関連)
Section titled “自己免疫の連鎖(シェーグレン症候群・橋本病との関連)”Wen ら(2021)は、シェーグレン症候群(SS)と橋本病(HT)を有する中年女性2例において、GAD65-AbまたはIAA-Ab陽性であっても3年間のOGTTで正常血糖が維持されたことを報告した4)。自己抗体陽性が即LADAへの進行を意味するわけではなく、肥満などの促進因子が加わって初めて発症するとされる。
7. 最新の研究と今後の展望(研究段階の報告)
Section titled “7. 最新の研究と今後の展望(研究段階の報告)”テプリズマブ(T1DM発症遅延免疫療法)
Section titled “テプリズマブ(T1DM発症遅延免疫療法)”テプリズマブは2022年11月にFDAが承認した抗CD3モノクローナル抗体である。T細胞表面のCD3に結合し、自己反応性T細胞を不活化することでT1DMの発症を遅延させる。LADAに対しては未承認・未研究であるが、自己免疫メカニズムの共通性から発症遅延の可能性が期待される。
semaglutideと非動脈炎性前部虚血性視神経症リスク
Section titled “semaglutideと非動脈炎性前部虚血性視神経症リスク”Hathaway ら(2024)は、T2DM患者においてsemaglutide使用群の非動脈炎性前部虚血性視神経症リスクがHR 4.28(95%CI 1.62-11.29、P < 0.001)と有意に高いことを報告した6)。LADAにGLP-1RAを使用する際は非動脈炎性前部虚血性視神経症の発症に注意を要する。
semaglutideと糖尿病網膜症悪化
Section titled “semaglutideと糖尿病網膜症悪化”HbA1cの急速低下時に糖尿病網膜症の悪化リスクが増加し、増殖網膜症の進行・黄斑浮腫の新規発症リスクが上昇するとされる。semaglutideを含むGLP-1RAの使用開始時には眼科的モニタリングが重要である。
DPP4阻害薬によるβ細胞保護
Section titled “DPP4阻害薬によるβ細胞保護”Marcon ら(2022)は、GAD65 > 250 U/ml陽性の90歳女性にsitagliptin 100 mg/日を投与し、1年間にわたりHbA1c 5.9%を維持した症例を報告した3)。DPP4阻害薬がLADAのβ細胞破壊を遅延させる可能性が示唆されるが、さらなるRCTが必要である。
CGMのメンタルヘルスへの影響
Section titled “CGMのメンタルヘルスへの影響”Gupta ら(2023)は、DKAで診断されたLADA患者(44歳男性)にCGMを導入した後、血糖80-408 mg/dLの変動を認め、OCD既往が悪化して自殺に至った症例を報告した2)。DM患者はうつ病リスクが約2倍とされ、CGM使用前の精神科的評価の重要性が示された。
COVID-19後自己免疫研究の課題
Section titled “COVID-19後自己免疫研究の課題”COVID-19患者における膵島自己抗体(IA2・GAD65・ICA)の発生率に関する大規模研究が必要とされている1)。また、SS・HTを有するGAD65-Ab陽性の非糖尿病患者が将来LADAへ進行するかについての長期追跡研究も求められている4)。
現時点ではT1DMのみFDA承認。LADAも同様の自己免疫機序を有するため、理論的に有効な可能性があるが、研究・承認ともに行われていない。今後の臨床試験の展開が期待される。
8. 参考文献
Section titled “8. 参考文献”- Lee N, Prabhu P, Swaminath S, et al. Development of Islet Antigen 2 (IA2) Antibodies Post-COVID-19 Infection: A Sign of Autoimmunity or Latent Autoimmune Diabetes Mellitus in Adults (LADA)? Cureus. 2023;15(6):e40971.
- Gupta R, Edupuganti S, Zamir I, et al. Latent Autoimmune Diabetes in Adults and a Continuous Glucose Monitoring Device: An Unfortunate Outcome. Cureus. 2023;15(11):e49141.
- Marcon LMR, Fanelli CG, Calafiore R. Type 1 Diabetes (T1D) and Latent Autoimmune Diabetes in Adults (LADA): The Difference Between a Honeymoon and a Holiday. Case Reports in Endocrinology. 2022;2022:9363543.
- Wen S, Jiang W, Zhou L. Islet Autoantibodies in the Patients with Sjogren’s Syndrome and Thyroid Disease and Risk of Progression to Latent Autoimmune Diabetes in Adults: A Case Series. Diabetes Metab Syndr Obes. 2021;14:1025-1033.
- Ibrahim A, Ahmed Mohmed MH, Darwish H, et al. A Case of Persistent Hyperglycemia: Autoimmune Link Between Hashimoto’s Thyroiditis and Latent Autoimmune Diabetes in Adults. Cureus. 2025;17(8):e91219.
- Hathaway JT, Shah MP, Hathaway DB, et al. Risk of Nonarteritic Anterior Ischemic Optic Neuropathy in Patients Prescribed Semaglutide. JAMA Ophthalmol. 2024.
