視神経病変
同側視力低下:侵された眼の視力障害。
視野欠損:中心暗点、周辺視野欠損など。
色覚異常:早期から生じることがある。
RAPD(相対的求心性瞳孔反応障害):視神経病変を強く示唆する所見。
光干渉断層計(OCT)変化:網膜神経線維層菲薄化・GCL障害として検出される1)。

膠芽腫(Glioblastoma multiforme; GBM)は、WHOグレード4に分類される星細胞腫であり、成人の原発性悪性脳腫瘍のなかで最も頻度が高い。米国での発生率は10万人あたり約3人で、年間10,000例以上が診断される。全脳腫瘍の12〜15%、悪性CNS腫瘍の45.2%を占める3)。診断時の平均年齢は64歳で、男女比は1.5:1である。
神経眼科的徴候は、以下の3機序のいずれかまたは複合により生じる。
視神経原発GBMはきわめて稀であり、全脳腫瘍の0.6〜1.2%、文献報告は約70例にとどまる1)。成人型視神経膠腫は悪性度が高く、中年男性に好発する。生命予後は約6か月とされており、小児型とは全く異なる経過をたどる。
視路を侵す場合の平均生存期間は約8か月で、非視路性GBMの14.6か月に比べて短い。
視神経原発GBMは全脳腫瘍の0.6〜1.2%とされ、世界的な文献報告は約70例にとどまる1)。非常に稀な病態であり、診断が遅れやすい点に注意が必要である。
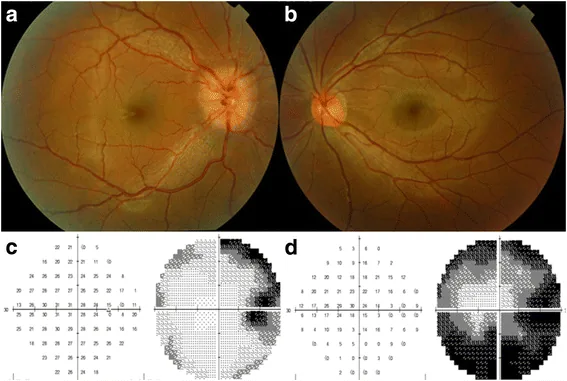
視路の侵された部位により、特徴的な神経眼科所見が得られる。
視神経病変
同側視力低下:侵された眼の視力障害。
視野欠損:中心暗点、周辺視野欠損など。
色覚異常:早期から生じることがある。
RAPD(相対的求心性瞳孔反応障害):視神経病変を強く示唆する所見。
光干渉断層計(OCT)変化:網膜神経線維層菲薄化・GCL障害として検出される1)。
視交叉・視交叉後方
両耳側半盲:視交叉の関与。接合部暗点を伴うことがある。
反対側同名半盲:視交叉後方(視索・視放線)の関与。
帯状視神経萎縮:視索関与時に反対側RAPDとともに出現。耳側中央と鼻側中央の乳頭蒼白が特徴的。
蓋性RAPD:中脳蓋病変では視力障害を伴わないRAPDが生じることがある。
頭蓋内圧亢進によるうっ血乳頭は、初期は霧視のみでMariotte盲点拡大を認める程度である。長期に持続すると視神経萎縮をきたし、視野狭窄・視力低下が進行する。
MRI撮像の方向は病変部位により異なる。視交叉前方の病変では眼窩冠状断が必須であり、後方病変では脳水平断が有用である。
視野欠損のパターンは腫瘍の位置により異なる。視神経関与では同側の中心暗点・周辺視野欠損、視交叉関与では両耳側半盲、視交叉後方(視索・視放線)の関与では反対側同名半盲を生じる。
GBMの約95%は孤発性であり、遺伝性症候群に関連するものは約5%にすぎない。発生は原発性と二次性に大別され、分子プロファイルが異なる。
原発性と二次性の主な分子変化を以下に示す。
| 種別 | 主な分子変化 |
|---|---|
| 原発性 | EGFR増幅、MDM2増幅、PTEN変異、CDKN2A欠失 |
| 二次性 | IDH1変異、p53変異、MET増幅 |
| 共通 | RAS・PI3K経路活性化 |
頭蓋外転移リスクと関連する因子として、TP53・TERT・PTEN変異、染色体+7/−10、肉腫様組織型が挙げられている6)。軟膜播種のリスク因子としては、脳室開放・反復手術・男性・上衣浸潤が報告されている3)。
確定診断には生検が必須である。評価項目はIDH1/2変異・GFAP・Ki-67である1)。
鑑別すべき疾患を部位別に示す。
| 部位 | 主な鑑別疾患 |
|---|---|
| 視神経 | 視神経鞘腫、視神経鞘髄膜腫、視神経リンパ腫 |
| 視交叉 | 下垂体腺腫、頭蓋咽頭腫、髄膜腫 |
最大限安全な範囲での切除を目標とする。視神経原発GBMでは視覚構造に隣接するため、完全切除は困難なことが多い1)。日本では腫瘍の局在・進展に応じて経過観察・手術・化学療法・放射線療法を選択する。
視交叉の圧迫解除により視力改善が得られることがある。一方で、視神経萎縮が進行した症例では圧迫解除後も視力の回復は期待しにくく、予後不良となる。
60Gy/30分割/6週間が標準的な照射プロトコールである1)。
手術+放射線+TMZのStupp protocolにより、生存中央値は約14.6か月とされている。
GBMの2〜4%(最大15〜25%)に軟膜播種が生じ、生存期間は0.2〜9.7か月と極めて短い2)。一次性LMSはきわめて稀である。標準治療は確立されておらず、髄腔内化学療法や追加放射線の効果は限定的である。
視神経原発GBMは視覚構造に隣接するため、機能温存を優先すると完全切除が困難なことが多い1)。最大限安全な切除を行った後に放射線・化学療法を追加することが一般的である。
GBMの増殖・浸潤・血管新生の中心的経路はEGFR増幅によるRAS/PI3K経路の活性化である。加えて腫瘍微小環境の免疫抑制が特徴的であり、T細胞浸潤の欠如・制御性T細胞(Treg)・骨髄由来抑制細胞(MDSC)の増加が免疫回避を促進する4)。
播種経路の主体はくも膜下腔を介した経路である3)。剖検では25%に脊髄播種が認められる。
視路への影響は以下の3機序から生じる。
LITTは46°C以上で凝固壊死を引き起こす一方、33〜43°CではBBB(血液脳関門)開放と免疫原性細胞死を誘導する4)。
Chandarら(2023)は新規診断GBMの1例にLITTを施行し、治療後にCD8+T細胞とPD-L1の著明な増加を確認した4)。同症例は9年間の無再発生存を達成した。
Longら(2025)は新規診断GBMにおいて、術前にニボルマブ+イピリムマブ+レラトリマブによる三剤ICI投与を実施した5)。治療後、腫瘍浸潤CD3+T細胞は9.8%から32.7%へ増加し、活性化T細胞は8.5倍増加した。1例で17か月間の無再発生存が確認され、現在GIANT試験が計画されている。
標準治療としての免疫療法は現時点では確立されていない。しかし術前三剤ICI投与により腫瘍内T細胞浸潤の著明な増加が確認されており5)、今後の臨床試験での検証が期待されている。
頭蓋外転移はGBMの0.4〜2.0%に発生し、転移後の生存期間は中央値1.5か月と極めて短い6)。転移例の分子的特徴としてTP53・TERT・PTEN変異が報告されており、これらが転移リスクのバイオマーカーとして研究されている6)。