RRMS
再発寛解型(Relapsing-Remitting MS):最も多いサブタイプ。再発が24時間以上持続し、発作間には完全または部分的な寛解がみられる。

多発性硬化症(Multiple Sclerosis; MS)は、中枢神経系(CNS)の白質に炎症性の脱髄性病変が発生し、多彩な神経症状が再発と寛解を繰り返す疾患である。グリオーシスによる瘢痕硬化性病変が特徴であり、通常は中枢神経のみが侵されて末梢神経系は障害されない。
米国での推定有病率は1〜1.5/1,000人である1)。世界では210万人が罹患し、北半球・南半球の高緯度地域に多く分布する。発症平均年齢は15〜45歳で、診断時の平均年齢は30歳である。日本の教科書では好発年齢は15〜50歳で女性(20歳代後半がピーク)に多く、男女比は1:2.9とされている。
MSには以下の4つの主要サブタイプがある。RRMS(再発寛解型)は25〜29歳で発症し、SPMSは40〜49歳で発症することが多い1)。
RRMS
再発寛解型(Relapsing-Remitting MS):最も多いサブタイプ。再発が24時間以上持続し、発作間には完全または部分的な寛解がみられる。
SPMS
二次性進行型(Secondary Progressive MS):RRMSから移行。寛解期にも進行性に障害が蓄積する。
PPMS
一次性進行型(Primary Progressive MS):初発から進行性に障害が蓄積する。再発なく緩徐に進行する。
CIS
臨床的孤立症候群(Clinically Isolated Syndrome):MSとなりうる初回の臨床エピソード。早期治療開始を可能にする。
MSはRRMS(再発寛解型)・SPMS(二次性進行型)・PPMS(一次性進行型)・CIS(臨床的孤立症候群)の4つのサブタイプに分類される。最も多いのはRRMSで、再発と寛解を繰り返す。SPMSはRRMSから移行し、PPMSは初発から進行性に障害が蓄積する。
患者の75%で初発症状は単独の愁訴であり、45%が運動・感覚症状、20%が視覚症状として発症する。
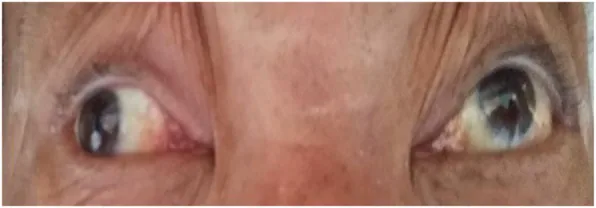
眼症状
全身神経症状
増悪は急性〜亜急性に発症し数日〜数ヶ月持続する。85%で症状改善・消失が得られるが、10〜15%では後遺症が残存する。
片眼性の痛みのある視力低下として発症することが多い。眼窩痛は92%に認められ、眼球運動で悪化するのが特徴である。また、体温上昇(入浴・運動)により症状が一時的に悪化するUhthoff現象もみられる。
MSの正確な原因は不明だが、自己免疫的な機序が発症に関わると考えられている。
遺伝的要因は関与するが、一卵性双生児でも一致率は25〜30%にとどまる。HLA多型や100以上のリスク遺伝子座が同定されているが、遺伝的素因だけでなく環境因子も発症に重要な役割を果たすと考えられている。
2017年McDonald基準(2024年改訂版)が用いられる。中枢神経の脱髄病変の時間的・空間的多発性(DIT/DIS)を証明することが基本である。2024年の改訂では視神経が5番目の地形的部位として追加された。日本では2015年の厚生労働省の多発性硬化症診断基準もある。
空間的多発性(DIS)の5つの地形的部位は以下の通り。
時間的多発性(DIT)の証明:2回以上の発作、またはMRIでの増強・非増強病変の同時存在、新規T2病変、CSFオリゴクローナルバンドで代替できる1)。
PPMSの診断には1年以上の障害進行に加え、脳T2病変・脊髄T2病変(2つ以上)・CSFオリゴクローナルバンドのうち2項目以上の所見が必要とされる1)。
脱髄プラークはT2高信号病変またはガドリニウム増強病変として検出される。
MRIが不確定な場合や疾患の進行予測に有用である1)。早期・無症候性の脱髄をMRI可視化前に検出できる。65%で潜時延長・振幅低下が認められる。
以下の疾患との鑑別が重要であり、非典型例では追加検査を実施する。
| 疾患カテゴリ | 主な鑑別疾患 |
|---|---|
| 脱髄疾患 | NMO(デビック病)、ADEM、MOGAD |
| 感染性 | サルコイドーシス、結核、梅毒、ライム病 |
| 自己免疫 | SLE、シェーグレン症候群、ベーチェット病 |
| 視神経疾患 | NAION、LHON、中毒性・代謝性視神経症 |
非典型例での追加検査:抗AQP4抗体(NMO除外)、抗MOG抗体(MOGAD除外)、血清NfL検査、梅毒血清検査(VDRL/RPR/FTA-ABS)、ANA(SLE)、ACE・リゾチーム(サルコイドーシス)。
日本の標準治療はメチルプレドニゾロン1,000mg/日の点滴静注を3日間連続で行うステロイドパルス療法である。3日間点滴後のプレドニゾロン内服(後療法)は行わない。ステロイド内服療法は再発率を高めるとされており行うべきではない。
無治療でも発症から3週間以内に約8割で視力改善が始まるが、パルス療法で改善期間が短縮される。視神経炎の9割以上で視力回復が期待できる。
ステロイドパルス療法が無効の場合は血液浄化療法(血漿交換療法)を行う。海外ではメチルプレドニゾロン500〜1,000mg/日×3〜5日間が用いられる。視神経炎治療試験(ONTT)では、高用量メチルプレドニゾロン静注は視機能・コントラスト感度・色覚の回復時間を改善したが、最終的な視力予後の改善は示されなかった。
視力低下・視野障害の改善後は、再発予防のために神経内科医との連携のもとでDMTを考慮する。
主要なDMTとその有効性を以下に示す。
| 薬剤 | 作用機序 | 投与法 | 相対リスク低下 |
|---|---|---|---|
| インターフェロンβ | T/B細胞活性・サイトカイン分泌修飾 | 自己注射 | 障害進行RR 0.71 |
| 酢酸グラチラマー | 制御性T細胞調節 | 自己注射 | 再発RR 0.82 |
| ナタリズマブ | CNSへの炎症細胞流入阻害 | 点滴 | 再発RR 0.56 |
| フィンゴリモド | S1P受容体調節 | 経口 | 新規T2病変RR 0.65 |
| テリフルノミド | ピリミジン合成阻害 | 経口 | 障害進行RR 0.76 |
| フマル酸ジメチル | 酸化ストレス・炎症軽減 | 経口 | 再発RR 0.64 |
| アレムツズマブ | 抗CD52モノクローナル抗体 | 点滴 | 障害進行RR 0.44 |
抗CD20モノクローナル抗体(オクレリズマブ、リツキシマブ、オファツムマブ)は再発型MSの標準治療として定着してきている3)。
脳病変のない視神経炎でも15年後には25%でMS発症が認められ、脳病変ありでは78%でMSへの移行がみられる。
脳MRIに病変がない場合でも15年後には25%でMSを発症し、脳病変がある場合は78%でMS移行がみられる。視神経炎を発症した患者は神経内科との連携のもと、再発予防のためのDMT適応を検討すべきである。
MSは自己免疫疾患と考えられている。Tリンパ球が髄鞘を異物として認識し、マクロファージ・サイトカイン・抗体を活性化して髄鞘・軸索を破壊する。髄鞘消失により電気インパルスの伝導が障害され、神経信号伝達が障害される。
活動性プラーク
泡沫状マクロファージ:髄鞘を貪食したマクロファージが集積する。
血管周囲浸潤(perivascular cuffing):リンパ球が血管周囲を取り巻く特徴的所見。
浮腫性の限局性脱髄病変:急性増悪期にみられる。
慢性プラーク
髄鞘消失:Luxol fast blue染色で確認できる。軸索は保存されるが再髄鞘化が不全。
NAWM病変:正常にみえる白質のびまん性グリオーシス・ミクログリア活性化・BBB破壊。限局的白質病変より臨床的障害と高い相関を示す。
オリゴデンドロサイトがCNSの再髄鞘化を担う1)。成人のオリゴデンドロサイト前駆細胞(OPC)に依存するが、既存の成熟オリゴデンドロサイトは再髄鞘化に貢献できない1)。
再髄鞘化失敗の主な原因は以下の通りである1)。
また、皮質・皮質下の灰白質障害も認められ、髄膜にB細胞濾胞様リンパ構造が形成されると、より重症の臨床経過に至ることが知られている1)。
CD40Lを阻害することで、T細胞と抗原提示細胞(B細胞含む)の共刺激を遮断する新規アプローチである。
Vermersch et al.(N Engl J Med 2024)による第2相試験では、frexalimabはMRIアウトカム(8〜12週における新規ガドリニウム増強病変)においてプラセボに対して明確な有効性を示し、神経組織障害のバイオマーカーである血清NfLの低下も確認された3)。進行型MSに対してはミクログリア・マクロファージの不活性化という効果も期待されており、プラークエッジのミクログリアへのCD40Lシグナル遮断による神経保護が理論的に可能とされる3)。
現在の高効果DMT(抗CD20薬)に対する臨床的優位性の確立が今後の課題とされる3)。
鉄依存性の細胞死であるフェロトーシスがMS神経細胞死に関与することが示された。
Tang et al.(2025)はWoo et al.(Cell, 2024)の研究を解説し、グルタミン酸興奮毒性→カルシウム過負荷→小胞体ストレス→STING1がSTIM1から解離→非典型経路活性化→オートファジー→GPX4(脂質過酸化の中和酵素)のオートファジー分解→フェロトーシスというカスケードを報告した4)。ヒトMS検体・マウスモデル双方で神経細胞におけるSTING1発現上昇が確認された。STING1阻害薬(C176、H151)は動物モデルでオートファジー依存性GPX4分解を減少させ、神経保護効果を示した4)。
研究段階では、CD40L阻害薬frexalimabによるミクログリア・マクロファージの不活性化を通じた神経保護3)と、STING1阻害によるフェロトーシス(鉄依存性細胞死)の抑制4)が有望視されている。いずれも現時点では治験・研究段階であり、標準治療ではない。