全身神経所見
運動失調性歩行:全方向性の不安定歩行。測定障害・低緊張・反復拮抗運動不全・共同運動時間障害を伴う1)。
深部腱反射消失:膝蓋腱反射・アキレス腱反射消失はHarding診断基準の必須項目。上肢反射消失も高頻度に伴う。反射亢進・痙性・はさみ脚を呈する例もある3)。
バビンスキー徴候:伸展性足底反応として出現する。
骨格変形:側弯症(初期から出現)、凹足(pes cavus)、腰椎後弯3)。
全身合併症:肥大型心筋症(最大63%)、糖尿病(5〜40%)2)。

フリードライヒ運動失調症(Friedreich Ataxia; FRDA)は、中枢・末梢神経系が侵される進行性の遺伝性疾患である。白人集団において最も頻度の高い常染色体劣性遺伝性運動失調症とされる。
1863年にニコラウス・フリードライヒが若年発症の運動失調・脊柱側弯・家族性心臓変性を報告した。後にピエール・マリーがFRDAを他の運動失調症と区別し、疾患概念が確立された。
疫学的には地域差が大きく、有病率は1:20,000〜1:750,000と報告されている。欧州人では約1:21,0001)、世界全体では1:40,0002)〜1:50,0003)と推定される。保因者頻度は約1/70とされる1)。南フランス・北スペイン・アイルランドで頻度が高く、スカンジナビアやロシアでは低い。サハラ以南のアフリカや東半球ではさらに低頻度であるが、西アフリカ(マリ共和国のトゥアレグ族近親婚家系)での遺伝学的確認例も報告されている3)。
遺伝形式は常染色体劣性であり、男女の発症率は同等である。典型的な発症年齢は平均15.5歳で、多くは25歳未満に発症する。8〜15歳での発症が多い2)。平均寿命は39歳であり、死因の主因は心筋症である2)。
白人集団で最も頻度の高い遺伝性運動失調症であり、有病率は地域差があって1:20,000〜1:750,000の範囲である。欧州では約21,000人に1人1)、世界全体では40,000〜50,000人に1人と推定される2)3)。保因者頻度は約1/70とされる1)。
運動症状の進行には個人差があるが、初発症状から平均約8年で独歩不能となり、11〜15年で車椅子が必要になる。GAA反復数が長い場合は5年で車椅子になった報告もある3)。
全身神経所見
運動失調性歩行:全方向性の不安定歩行。測定障害・低緊張・反復拮抗運動不全・共同運動時間障害を伴う1)。
深部腱反射消失:膝蓋腱反射・アキレス腱反射消失はHarding診断基準の必須項目。上肢反射消失も高頻度に伴う。反射亢進・痙性・はさみ脚を呈する例もある3)。
バビンスキー徴候:伸展性足底反応として出現する。
骨格変形:側弯症(初期から出現)、凹足(pes cavus)、腰椎後弯3)。
全身合併症:肥大型心筋症(最大63%)、糖尿病(5〜40%)2)。
神経眼科所見
眼振(nystagmus):小脳・脳幹回路の障害による。眼位依存性眼振を含む。
矩形波ジャーク(square-wave jerks):固視中に混入する不随意の衝動性眼球運動。
追従眼球運動障害:視標追跡が階段状となる(パシュート異常)。
サッケード測定障害(saccadic dysmetria):過大または過小サッケードが出現する。
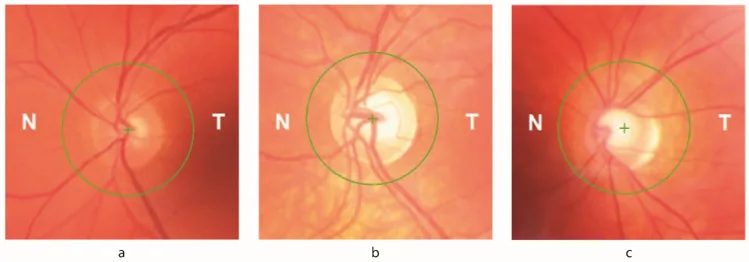
視神経萎縮:眼底検査で確認される。最大30%の患者に眼科的徴候が出現。
RNFL厚減少:OCTで検出。視力・コントラスト感度の低下と直接相関。
視野欠損:周辺部から同心円状に進行する初期視野欠損。OCTで記録されたRNFL消失と関連。
FRDAでは最大30%の患者に眼科的徴候が出現するが、多くの患者は初期に視覚的な自覚症状を欠く。視神経萎縮・RNFL厚減少・眼球運動障害は客観的検査で検出され、視力・コントラスト感度の低下と直接相関する。定期的な眼科検診が推奨される。
FRDAの原因は第9染色体上のFXN(フラタキシン)遺伝子イントロン1における GAA 3塩基反復配列の伸長である。症例の96%がbiallelic pathogenic expansionのホモ接合体である1)。残りの症例はGAA伸長と点変異、またはGAA伸長とintragenic/whole-gene deletionとの複合ヘテロ接合体である1)。
GAA反復数と疾患との関係を以下に示す。
| 分類 | GAA反復数 |
|---|---|
| 正常 | 5〜33回 |
| 中間(保因者相当) | 34〜65回 |
| 病的 | 66回以上(別報告では90回以上)1)3) |
GAA反復数が長いほど発症年齢が早く、重症化する傾向がある。アレル反復数が999/766と極めて長い症例では11歳発症・5年以内に車椅子が必要となった(一般的な10年より早い)3)。反復配列内のinterruption(中断)は発症年齢を遅延させる可能性がある1)。
Intragenic deletion + GAA expansionの複合ヘテロ接合体はbiallelic expansionより早期発症・急速進行・重症心筋症の傾向があるとされるが、典型的な経過を示した症例も報告されている1)。
近親婚は常染色体劣性遺伝の疾患特性上、発症リスクを高める2)3)。欧州系の祖先を持つ集団で頻度が高い。
PCRフラグメント解析とTP-PCRでは遺伝子内欠失を検出できないため、見かけ上のbiallelic expansionが実際にはGAA expansion + intragenic deletionである可能性がある1)。MLPA(Multiplex Ligation-dependent Probe Amplification)による追加検査と親サンプルの検査が、正確な遺伝カウンセリングには不可欠である。
臨床診断にはHardingの基準が用いられる。
| カテゴリ | 主な項目 |
|---|---|
| 必須項目 | 25歳未満発症、進行性歩行・四肢運動失調、膝蓋腱・アキレス腱反射消失、軸索変性像、構音障害(発症5年以降) |
| 追加所見(66%以上) | 側弯症、下肢錐体路性筋力低下、上肢反射消失、太い神経線維の感覚消失、心電図異常 |
| その他(50%未満) | 眼振、視神経萎縮、難聴、遠位筋萎縮、凹足、糖尿病 |
感覚神経活動電位(SNAP)消失を特徴とする感覚ニューロパチーを示す。軸索性感覚多発ニューロパチーのパターンが特徴的である3)。
眼球運動障害を主訴とした場合、以下の疾患との鑑別が必要である。
現時点では根治療法は存在せず、多職種連携による対症療法と合併症管理が治療の中心となる。
神経内科・整形外科
側弯症管理:軽度〜中等度には装具療法。重度には手術を検討。
凹足管理:腓腹筋へのボツリヌス毒素注射、アキレス腱ストレッチにより可動性を改善する。
リハビリテーション:理学療法・作業療法・言語療法による機能維持。
眼科
ロービジョンケア:視神経萎縮・網膜萎縮による視覚症状がある患者に拡大鏡・照明調整・生活指導を行う。
眼球運動障害の対症療法:眼位依存性眼振にはプリズム眼鏡(悪化する眼位方向に対し両眼に同等のプリズム度数を付加)を用いる。垂直眼振・周期性方向交代性眼振・衝動性眼球運動混入にはGABA_B作動薬を投与する。
処方例(GABA_B作動薬):ギャバロン錠(5 mg)3〜6錠、分1〜3。
FRDAに伴う糖尿病はミトコンドリア機能障害が根底にあるため、薬剤選択に注意が必要である2)。
上記レジメンを用いた症例報告では、HbA1cが13.3%から8.4%(17ヶ月後)、さらに6.9%(追加19ヶ月後)に改善し、ICARSは85から71へと14点改善した2)。
ミトコンドリア機能障害が根底にあるため、メトホルミンやチアゾリジンジオン系は避ける2)。DPP-4阻害薬(シタグリプチン等)やGLP-1アナログが推奨される。L-カルニチン・CoQ10・ビタミンEなどのミトコンドリア標的補助療法も有用な可能性がある2)。
フラタキシンはミトコンドリア内膜に局在するタンパク質である。鉄代謝(鉄貯蔵・鉄-硫黄クラスターの組み立て)に関与し、ミトコンドリア呼吸鎖の正常機能に不可欠である1)。
GAA反復配列の伸長は転写サイレンシング(transcriptional silencing)を引き起こし、FXN mRNAレベルを低下させる1)。フラタキシンが欠乏すると以下が生じる。
フラタキシン欠乏により細胞内鉄レベルが変動し、網膜神経節細胞(RGC)が酸化ストレスに対して脆弱化する。FA患者の最大30%に眼科的徴候が出現する。脳幹・小脳回路および視神経の両方が障害を受ける。RNFL厚の減少は視力・コントラスト感度の低下と直接相関し、周辺部から同心円状に進行する初期視野欠損はOCTで記録されたRNFL消失と関連する。
肥大型心筋症により心重量が増加する。心筋組織は肉眼的に「大理石様(marble-like)」外観を呈することがある。
ミトコンドリア機能障害がFRDA関連糖尿病の根本的な原因である2)。
Intragenic deletion保有者ではbiallelic expansionより早期発症・急速進行・重症心筋症の傾向がある1)。欠失によりstart codonが除去される場合はタンパク質産生が完全に消失する1)。
フラタキシン欠乏による鉄代謝異常と酸化ストレスが網膜神経節細胞を傷害する。RNFL厚の減少が視力・コントラスト感度低下と直接相関し、周辺部から同心円状に進行する視野欠損を生じる。また脳幹・小脳回路の障害により眼振・追従眼球運動障害・サッケード測定障害などの眼球運動異常も出現する。
Cooper et al.(2008)の臨床試験では、CoQ10とビタミンEの併用療法により2年間にわたるICARSスコアが有意に改善したことが報告されている2)。
Schöls et al.(2005)のランダム化プラセボ対照交差試験では、L-カルニチン投与によりミトコンドリアATP産生が有意に改善することが示された2)。
Sureshkumarら(2025)は、FA関連糖尿病を有する32歳女性に対し、インスリン療法・シタグリプチン・L-カルニチン・CoQ10・ビタミンE・ニューロトロピックビタミン・イメグリミンの組み合わせを投与した2)。HbA1cは13.3%から17ヶ月後に8.4%、さらに19ヶ月後に6.9%へ改善し、ICARSは85から71へと14点改善した(HOMA2-IR: 4.5→1.2、HOMA2-%B: 5→60、MAGE: 120→70 mg/dL、CV: 43%→34.9%)。SARAによる自然史では3年間に約2.31点の悪化が予測されるところ、約16点の正の偏差を示した。長期的な血糖安定化と運動失調改善の同時達成を初めて報告した症例とされる。
イメグリミンは呼吸鎖活性の改善・酸化ストレス軽減・ATP/NAD+合成促進を介して作用すると考えられている2)。
Aguileraら(2023)は、biallelic伸長と推定されていた患者の親サンプル検査により、FXN遺伝子の5’UTRおよびエクソン1〜2を含む新規intragenic deletionを同定した1)。これまで文献上10例の遺伝子内欠失が報告されているにとどまるが、実際にはより頻度が高い可能性が指摘されている。MLPA等を用いた補完的遺伝子解析と親サンプル検査の標準化が今後の課題とされる。
西アフリカでの初確認例の報告は、多様な民族・地理的背景での大規模コホート研究の必要性を示している3)。疾患修飾バリアントの同定が将来の治療標的となりうる。