内腔閉塞
原因:フィブリン凝塊、虹彩色素顆粒、炎症・出血の分解産物が閉塞の主要原因である2)。
対処の優先順位:隅角鏡で確認→YAGレーザー→YAGレーザー虹彩切開→ニードリング→不成功の場合は線維柱帯切除術またはチューブシャントを検討2)。
予後:一報告では4症例全例でXEN摘出と代替手術が必要であった2)。AS-OCTでフィブリン閉塞を確認し、ステロイド強化で自然消退した症例も報告されている5)。

Xenゲルステント(Xen Glaucoma Treatment System)は低侵襲緑内障手術(MIGS; Minimally Invasive Glaucoma Surgery)の一つに分類される結膜下濾過デバイスである。 前房から結膜下腔へ直接房水を誘導し、濾過胞を形成させることで眼圧(IOP)を下降させる。
Allergan社(現AbbVie)が開発した。欧州では2013年にCEマーキングを取得し、米国では2016年にFDA承認を得た。日本では2019年2月時点で未認可である。
XEN45の主要な構造的特徴を以下に示す。
XEN45とPreserFlo MicroShuntは、プレートを持たないbleb形成型シャントとして現在利用可能なデバイスである6)。従来の線維柱帯切除術とは異なり、結膜弁・強膜弁の作成を必要としない。
MIGSが普及したことにより、軽度〜中等度の緑内障に対しても、より早期からの手術介入が可能になった8)。Xenゲルステントはその中でも比較的広い適応範囲を持ち、中等度〜進行した緑内障にも使用される。
線維柱帯切除術は結膜弁・強膜弁を作成して房水の流出路を形成する従来法である。Xenゲルステントは結膜切開を最小限にとどめ、インジェクターで前房から直接ステントを留置する。手術時間・回復時間が短い一方、低目標眼圧の達成率では線維柱帯切除術が優れるとする報告がある。詳細は「有効性と臨床成績」の項を参照。
FDA承認の適応は、最大許容薬物療法に不応の以下の病型とされている6)。
欧州では薬物療法が不成功の開放隅角緑内障全般に適応が認められている。白内障手術との同時施行も可能であり6)、中等度〜進行した緑内障に対しても適応となりうる6)。
絶対禁忌は以下の通りである6)。
相対禁忌には、菲薄または不健康な結膜、過去の硝子体手術・失敗した濾過胞手術歴、強度近視、先天緑内障、続発緑内障が含まれる6)。
患者選択における主な考慮点を以下に示す。
手術自体は可能だが、抗凝固薬使用例では出血合併症リスクが約2.7倍(10.1% vs. 3.7%)高いとの報告がある4)。脈絡膜上腔出血(SCH)の症例報告もあり、担当医による個別のリスク評価と十分な説明が必要である。詳細は「合併症と対処法」の項を参照。
最も一般的な術式である。主な手順は以下の通りである。
クローズドアプローチ(結膜を前方移動させ、強膜穿刺でトンネルを作成)とオープンアプローチ(結膜を切開し、スポンジまたは注入でマイトマイシンCを適用)がある。Ab internoと比較して粘弾性物質が不要で、ステント位置の決定がより正確とされる。ニードリング率を11.8%まで低下させたとの報告もある。
結膜下にair(空気)を注入後、OVDを追注することでTenon嚢を剥離し、ステント留置のポケットを形成する手法である。マイトマイシンC毒性の観点から注意が必要であり、OVD存在下でのマイトマイシンC蓄積が角膜上皮毒性を引き起こした症例が報告されている1)。
マイトマイシンCは結膜下の線維化を抑制し、濾過胞の長期維持に不可欠である。Xenゲルステント成功の鍵とされている7)。
術後1日目のIOP > 10 mmHgは将来のニードリング必要性の予測因子とされており5)、AS-OCTによる早期評価が術後管理の質を高める。
術後ニードリングはXenゲルステントで最も頻度の高い術後処置である。
AS-OCTガイド下のニードリングはTenon嚢の圧迫が疑われる場合に有効であり、ステント開口部と周囲組織の関係を確認しながら施行できる5)。
主要な合併症とその頻度を下表に示す。
| 合併症 | 頻度 |
|---|---|
| 一過性低眼圧 | 9.59% |
| 前房出血 | 5.53% |
| 眼圧スパイク | 2.11% |
| 追加緑内障手術 | 2.4〜15.3% |
| 脈絡膜剥離 | 1.31% |
| インプラント閉塞 | 0.93% |
| 黄斑浮腫 | 0.91% |
| 位置異常 | 0.88% |
| 浅前房 | 0.88% |
| 濾過胞漏出 | 0.68% |
| 視力低下(≥2行・>1か月持続) | 0.34% |
| 角膜浮腫 | 0.29% |
| 眼内炎 | 0.15% |
内腔閉塞
原因:フィブリン凝塊、虹彩色素顆粒、炎症・出血の分解産物が閉塞の主要原因である2)。
対処の優先順位:隅角鏡で確認→YAGレーザー→YAGレーザー虹彩切開→ニードリング→不成功の場合は線維柱帯切除術またはチューブシャントを検討2)。
予後:一報告では4症例全例でXEN摘出と代替手術が必要であった2)。AS-OCTでフィブリン閉塞を確認し、ステロイド強化で自然消退した症例も報告されている5)。
脈絡膜上腔出血
特徴:稀だが重篤な合併症であり、術後低眼圧に起因する4)。
リスク因子:抗凝固薬使用が重要なリスク因子である。86歳の抗凝固薬使用患者でkissing SCHを生じ、外科的ドレナージを要した症例が報告されている4)。
臨床的意義:当該報告はXen後SCHとして文献上4例目であり、外科的ドレナージを要した初の報告とされる4)。
濾過胞が線維化・被包化して眼圧が再上昇した際に、針(通常は26〜30G)で濾過胞周囲の癒着を外来処置として剥離する手技である。12か月以内で約46%に施行が必要とされ、Xenゲルステントに特有の高頻度の術後処置として認識されている。
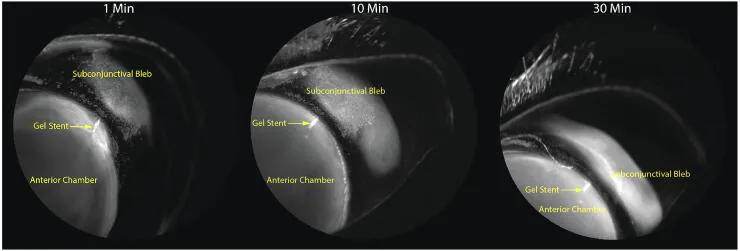
複数の研究からXenゲルステントの眼圧下降効果が報告されている。
メタ解析では、Xen術前後の平均IOP差は −7.80 mmHg、平均薬剤数差は −1.99と集計されている。全研究で薬剤数の減少が確認されている10)。
Panarelli ら(2023)によるシステマティックレビューでは、Xenゲルステントを受けた複数コホートで術前から術後にかけて一貫したIOP低下と点眼薬数減少が示された10)。
Paik ら(2025)の閉塞隅角疾患に対するMIGSの系統的レビュー・メタ解析では、Sng ら(19眼・原発閉塞隅角緑内障)で術前IOP 21.7±3.7 mmHg から1年後11.7±3.0 mmHg(薬剤数1.4→0.2)に、Gabbay ら(13眼)で術前24.6から1年後16.4 mmHg(薬剤数2.9→0.6)への改善が報告された9)。
AAO優先診療パターン(Preferred Practice Pattern)Pivotal trialでは、1年後のIOPが「10台中盤(midteens)」に達したと報告されている7)。
主要研究を下表に要約する。
| 研究(眼数) | 術前→術後IOP | 薬剤数変化 |
|---|---|---|
| Sng et al.(19眼) | 21.7→11.7 mmHg | 1.4→0.2剤 |
| Gabbay et al.(13眼) | 24.6→16.4 mmHg | 2.9→0.6剤 |
Lindland ら(2021)は、無虹彩関連緑内障(60歳男性)に対してXenゲルステントを留置し、術前IOP 30 mmHg(4剤使用)から2年後に12 mmHg(1剤)に低下した症例を報告した。ニードリングは不要であった3)。
12か月のフォローアップではIOP低下・薬剤減少に統計的有意差は認められない2)。一方で低目標IOP(≤12 mmHg)の達成においては線維柱帯切除術が優位との知見がある。XenゲルステントはMIGSの低侵襲性という優位点を有する。
Xenゲルステントは線維柱帯・シュレム管をバイパスし、前房から輪部付近の結膜下腔へ直接房水を誘導する。シュレム管が閉塞した症例においても有効な流出路を提供できる9)。
形成された濾過胞は以下の経路で房水を吸収する。
素材特性
ブタゼラチン素材:グルタルアルデヒドで架橋したブタ真皮由来ゼラチンを使用。親水性・柔軟性に優れ、組織適合性が高い。非炎症性で移動・侵食リスクが低い。
房水による軟化:房水に触れると1〜2分で軟化し、隣接組織の形状に適合する。これにより摩擦や組織損傷を低減する。
流体力学設計
Hagen-Poiseuilleの法則:チューブ内の流量は内腔半径の4乗に比例し、長さに反比例する。XEN45の45μm内腔はこの関係を利用し、定常状態でのIOP 6〜8 mmHgを実現するよう設計されている。
内腔サイズ最適化:45μmの内腔径は、低眼圧を回避しながら十分な眼圧下降を達成するために最適化されたサイズである。
ブタ真皮由来ゼラチンは親水性・柔軟性・生体適合性に優れる素材である。房水に触れると短時間で軟化し、組織形状に適合する。非炎症性であるため、異物反応によるステント周囲の線維化を抑制し、移動・侵食リスクも低い。ただしブタ由来製品アレルギーは禁忌事項であるため、術前に確認が必要である。
結膜下へのair先行注入によりTenon嚢を剥離してステント留置ポケットを形成する手法である。ニードリング率の低下が期待されているが、マイトマイシンC蓄積による角膜毒性リスクへの注意が必要であることが報告されている1)。
前眼部OCTを用いた術後管理の体系化が進んでいる。ステント開口部と周囲組織の関係を可視化し、フィブリン閉塞の特定やニードリング適応の判断を支援する5)。術後1日目のIOPが >10 mmHgであることが将来のニードリングの予測因子として同定されており、早期介入の意思決定に役立つ5)。
無虹彩関連緑内障3)やぶどう膜炎性緑内障1)など、従来の手術が困難な特殊適応でのXenゲルステント使用が症例報告レベルで蓄積されつつある。
内腔閉塞のメカニズムと対処法についての知見が集積している2)。3年以上の長期成績データが報告され始めており、長期的な有効性と安全性の評価が進んでいる9)。
前眼部OCT(AS-OCT)はステントの開口部と周囲組織の関係を断層像として可視化できる。フィブリンによる内腔閉塞か、Tenon嚢による圧迫か、濾過胞の被包化かといった流出障害の原因鑑別に有用であり、ニードリングの適応・部位の決定を支援する5)。術後早期からのAS-OCTによる評価が推奨されている。