術後早期の適応(1週〜2か月)
原因:術中のTDM剥離不全による房水流出抵抗の上昇。
隅角所見:TDMウィンドウが厚く、強膜内湖への凹みがみられない。
注意:術後4週間以内は急激な減圧や前房消失のリスクがあり、相対的禁忌である。

Nd:YAGレーザー・ゴニオパンクチャーは、非穿孔性緑内障手術(NPGS)の不可欠な構成要素である。NPGSには深層強膜切除術、管状形成術(canaloplasty)、粘弾性管形成術(viscocanalostomy)が含まれる1)2)。
NPGS後の眼圧コントロールは、線維柱帯・デスメ膜(trabeculo-Descemet’s membrane: TDM)を介した房水濾過に依存する。このTDMが術中の剥離不全や術後の線維化により肥厚すると、房水流出抵抗が上昇し眼圧が上昇する。
ゴニオパンクチャーはTDMに微小穿孔を作成し、前房から強膜内スペースへの直接的な房水流出を回復させる処置である。これにより機能不全に陥った非穿孔型の濾過が穿孔型に転換されるが、濾過胞がすでに形成された後の安全な時期に行うため、低眼圧関連合併症のリスクは大幅に低下する。
NPGSは線維柱帯切除術(trabeculectomy)と比較して低眼圧関連合併症が少ないが、長期的な眼圧降下効果は劣る1)2)。ゴニオパンクチャーはNPGSの成功率を向上させる重要な補助的処置である。
ゴニオパンクチャーは非穿孔性緑内障手術(NPGS)に特化した処置であり、線維柱帯切除術(trabeculectomy)後には適応とならない。NPGSでは線維柱帯・デスメ膜が残存する構造であるため、そこにレーザーで穿孔することで房水流出を回復させるという原理である。線維柱帯切除術ではすでに全層穿孔が行われているため、ゴニオパンクチャーの対象にはならない。
NPGS後に十分な眼圧コントロールが得られない場合にゴニオパンクチャーが検討される。
術後早期の適応(1週〜2か月)
原因:術中のTDM剥離不全による房水流出抵抗の上昇。
隅角所見:TDMウィンドウが厚く、強膜内湖への凹みがみられない。
注意:術後4週間以内は急激な減圧や前房消失のリスクがあり、相対的禁忌である。
術後晩期の適応(数か月〜数年後)
原因:TDMの線維化、色素沈着による進行性の房水流出抵抗上昇。
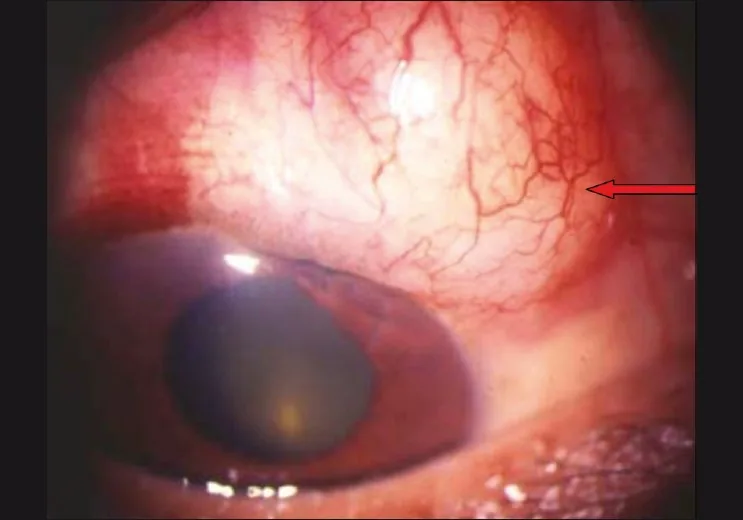
隅角所見:強膜内湖に血液・デブリ・新生血管が存在する場合は切迫した線維化の兆候である。
注意:強膜内湖が完全に線維化または虚脱する前に施行すべきである。
点眼麻酔に加え、1%アプラクロニジンとピロカルピンを点眼する。ピロカルピンによる縮瞳は虹彩嵌頓のリスクを軽減する。眼圧が高い場合は全身性炭酸脱水酵素阻害薬を併用する。
隅角鏡用コンタクトレンズを装用し、Nd:YAGレーザーのエイミングビームを半透明のTDMに合わせる。フリーランニングQスイッチモードで以下のパラメータを使用する。
照射部位は虹彩脱出や周辺虹彩前癒着形成のリスクを最小限にするため、前方(角膜側)に行う。レーザー後の虹彩嵌頓リスクを減らすため、TDMウィンドウ近傍にアルゴンレーザー虹彩成形術を併施することもある。
ステロイド点眼薬(1%酢酸プレドニゾロン)を1日3回、3日間投与する。緑内障治療薬はフォローアップ受診まで継続する。1〜3週間後に再診し、眼圧と合併症の有無を確認する。
最も重要な合併症は虹彩嵌頓であり、最大25%に発生する。以下の場合にリスクが高い。
その他の合併症として、炎症、前房出血、脈絡膜剥離を伴う低眼圧、前癒着がある。いずれも稀である。
虹彩嵌頓が生じた場合、縮瞳薬による保存的管理を試み、無効であればレーザーまたは手術による癒着解離術を検討する。
1回のゴニオパンクチャーにより、約50%の症例で少なくとも2年間、処置前と比較して20%以上の眼圧低下が得られると報告されている。NPGSの成功率向上に不可欠な処置として位置づけられており、NPGS後の眼圧上昇に対する第一選択のレーザー治療である。