FHI
炎症:慢性・低グレード。ステロイド無反応。
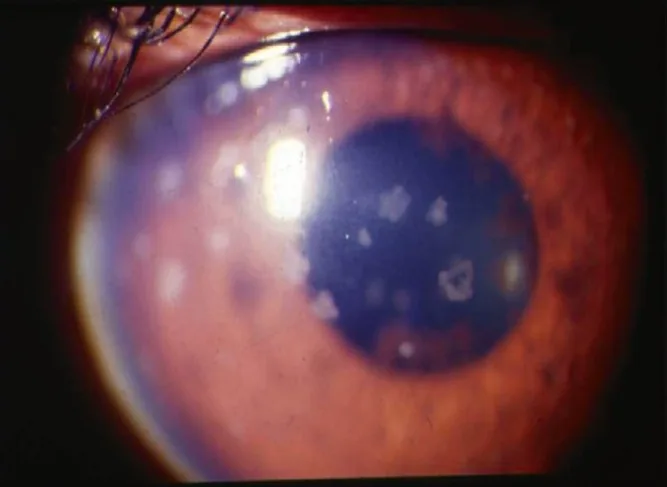
KP:星状、びまん性(角膜全面)。
虹彩異色:びまん性萎縮による。
後癒着:なし。
嚢胞様黄斑浮腫:なし。

1906年にオーストリアの眼科医Ernst Fuchsが、虹彩異色・毛様体炎・白内障を呈する38例を報告した。フックス異色性虹彩毛様体炎(Fuchs heterochromic iridocyclitis: FHI)はフックスぶどう膜炎症候群(Fuchs uveitis syndrome: FUS)とも呼ばれる。
全ぶどう膜炎の2〜11%を占める。人種や性別による偏りはなく、20〜40歳代に発症することが多い。大部分は片眼性であり、両眼性はわずか5〜10%である。無症状の患者が多いため過小診断されている可能性がある。
FHIは特発性・無痛性・慢性の低グレード虹彩毛様体炎であり、虹彩実質の萎縮による異色を特徴とする2)。典型的な発症年齢は20〜40歳で、男女ほぼ同率に罹患する2)。
FHI患者は他の前眼部ぶどう膜炎と異なり、通常は痛み・充血・羞明を伴わない。そのため受診まで長年無症状であることも少なくない。受診のきっかけとなる主訴は以下の通りである。
組織学的には、前実質脱色素、血管硝子化、細胞浸潤、Russell小体が認められる2)。
日本人は褐色虹彩であるため、虹彩異色が明らかに現れにくい。虹彩の色調変化よりも、虹彩紋理の不鮮明化やびまん性虹彩萎縮を重視して診断する必要がある。無散瞳の状態で僚眼と比較することがポイントである。
FHIの正確な病因はいまだ不明であり、多因子性と考えられている。
欧州のFHI患者63人を対象とした研究では、全症例で風疹ウイルス(RV)に対する眼内抗体産生が認められた。日本の教科書でも風疹ウイルスとの関連が注目されている。
アジアではCMV感染がFHIの16〜42%を占めると報告されている。中国の研究では35人中15人の前房水からPCRによりCMV DNAが検出された。
続発緑内障のリスクを高める因子として以下が報告されている。
FHIの診断は臨床所見の組み合わせに基づく。確定的な診断テストは存在せず、La Heyらの診断基準により、他疾患の除外後に初めて診断される。風疹抗体価の利用を提案する意見もあるが、広く普及していない。
日本人では虹彩異色が明らかでないことが多いため、以下の点が診断の鍵となる。
FHI
炎症:慢性・低グレード。ステロイド無反応。
KP:星状、びまん性(角膜全面)。
虹彩異色:びまん性萎縮による。
後癒着:なし。
嚢胞様黄斑浮腫:なし。
Posner-Schlossman症候群
炎症:再発性・急性。ステロイド反応性あり。
眼圧:40〜60 mmHgの急性上昇を繰り返す。
KP:白色・小型。
経過:発作は数日で寛解。
虹彩萎縮:進行例でびまん性に至ることあり。
その他の鑑別疾患は以下の通りである。
FHIの炎症の大部分は血液房水柵の破綻による細胞・タンパク質の漏出の結果と考えられている。副腎皮質ステロイド薬はFHIの軽度の前房反応にほとんど効果がなく、長期投与はステロイド白内障や緑内障のリスクを高めるため、積極的に使用すべきではない。
原則として炎症に対する治療は不要であり、経過観察とする。
FHIに合併する白内障は他のぶどう膜炎と比較して手術結果が良好である。水晶体乳化吸引術+後房眼内レンズ挿入術が安全かつ効果的である。他のぶどう膜炎と比べると術後炎症は比較的少なく、眼内レンズ挿入も問題となることは少ない。
ただし、重度の虹彩萎縮(透照試験陽性)、緑内障合併例、虹彩血管異常を伴う症例では術後予後をより慎重に見極める必要がある。続発緑内障に対する濾過手術が必要となる可能性がある場合には、上方結膜を温存して角膜切開で白内障手術を行う。
硝子体浮遊物が視覚的に重大な障害となる場合、硝子体茎切除術(PPV)が有効である。FHIでは他のぶどう膜炎よりも硝子体手術の結果が良好であり、これはFHIの炎症経過が比較的穏やかで嚢胞様黄斑浮腫を欠くためと考えられる。
続発緑内障の有病率はFHI患者の9〜59%に及び、長期追跡ほど高率となる2)。緑内障はFHIにおいて最も視機能を脅かし、管理が困難な合併症である。73%が最大量の薬物療法に反応せず、観血的手術が必要となることが多い。
ステロイドは緑内障の原因にもなるため、ステロイド緑内障との鑑別が重要である。
ぶどう膜炎緑内障全般では、結膜下瘢痕化の傾向から線維柱帯切除術の成功率が低い。FHIでも手術成績に関しては賛否両論がある。
| 術式 | 成績 |
|---|---|
| MMC-trab(1年) | 58〜90.9% |
| MMC-trab(4年) | 62.3% |
| AGV vs trab | 研究により結論が異なる |
緑内障ドレナージデバイス(AGV、Baerveldt、Molteno)はぶどう膜炎緑内障において一般的に優先される初期手術の選択肢であり、1年成功率は77〜94%とされている。
FHIの軽度の前房反応はステロイド点眼にほとんど反応せず、長期使用はステロイド白内障やステロイド緑内障のリスクを高める。原則としてステロイドを投与せずに経過観察する。Posner-Schlossman症候群との鑑別目的で短期間投与する場合はあるが、長期投与の適応はない。
FHIに伴う緑内障の発症には以下の機序が関与する2)。
隅角鏡検査では開放隅角と線維柱帯を横切る血管新生がみられる2)。これらの血管は軽微な外力で破綻しやすく、前房穿刺・圧平眼圧測定・眼内手術時にAmsler徴候(前房出血)を引き起こす。
虹彩蛍光造影では虹彩血管の漏出や虚血性変化が確認されることがある。
ぶどう膜炎に伴う眼圧上昇には以下の機序が関与する。
FHIでは虹彩後癒着や周辺虹彩前癒着は通常みられず、主に線維柱帯への炎症細胞浸潤と構造的変化が眼圧上昇の原因と考えられている。
Yuksel ElginとHepokur(2025)は、FUS関連緑内障に対するGATT(gonioscopy-assisted transluminal trabeculectomy)の成績を4症例で報告した1)。50歳未満の患者に対し、初回手術としてGATTを実施した。しかし全例で手術は不成功に終わり、平均6ヶ月後に3例はMMC併用線維柱帯切除術、1例はdiodeレーザー毛様体光凝固術を要した1)。
著者らは、FUS緑内障では線維柱帯が炎症性デブリで閉塞しているのではなく、後線維柱帯(post-trabecular)領域の瘢痕化が原因であり、GATTでは十分な眼圧下降が得られない可能性を指摘した1)。FHI診断からGATT手術までの期間が長いほど瘢痕化が進行し、手術成績が悪化する可能性がある1)。
低侵襲緑内障手術(MIGS)のぶどう膜炎緑内障への応用は評価段階にある。カナルプラスティや線維柱帯切開術では予備的に有望な結果が報告されている。ただし、iStentやXenなどの狭い内腔を持つインプラントデバイスは、炎症性デブリによる閉塞の懸念がある。
現時点ではFHI緑内障に対する低侵襲緑内障手術の有効性は限定的と考えられている。GATTの4症例報告では全例が不成功に終わった1)。iStentやXenなどのインプラントデバイスは炎症性デブリによる閉塞が懸念される。FHI緑内障では後線維柱帯の瘢痕化が関与する可能性があり、隅角手術のみでは十分な効果が得られない場合がある。