Stage I(ブレブ炎)
「赤の上の白(white-on-red)」:充血した結膜の上に白濁した濾過胞が特徴的。
濾過胞の混濁:黄白色に不透明化する。
軽度の前房反応:前房蓄膿を伴う場合と伴わない場合がある。

濾過胞関連感染症(bleb-related infection: BRI)は、緑内障濾過手術(線維柱帯切除術など)後に濾過胞から細菌が侵入して生じる感染性合併症である。1994年にBrownらが「ブレブ炎(blebitis)」の用語を導入して以来、臨床的に以下の2つの病態に分類される。
病期分類としては、Stage I(濾過胞の局所炎症)、Stage II(前房内の細胞・フレア・前房蓄膿)、Stage III(硝子体波及)の3段階が用いられる1)。Stage IIIはさらにIIIa(眼底透見可能)とIIIb(硝子体混濁で眼底透見不能)に細分される1)。
日本の多施設共同前向き研究では、術後5年間の濾過胞感染累積発症率は2.2%、うちブレブ関連眼内炎は1.1%と報告されている。他の内眼手術の晩期感染症と比較して発症頻度は高い。
発症時期により、術後1ヶ月以内の早期発症型と1ヶ月以降の晩期発症型に大別される1)。早期発症型は低毒性菌(コアグラーゼ陰性ブドウ球菌)が多く、晩期発症型は高毒性菌(連鎖球菌属、インフルエンザ菌)が関与し予後不良となりやすい1)。
ブレブ炎は感染が濾過胞内に限局した状態であり、適切な局所治療で良好な視力予後が期待できる。一方、濾過胞関連眼内炎(BAE)は感染が硝子体まで波及した状態であり、積極的な治療にもかかわらず94%で視力0.1以下に低下するとの報告がある。
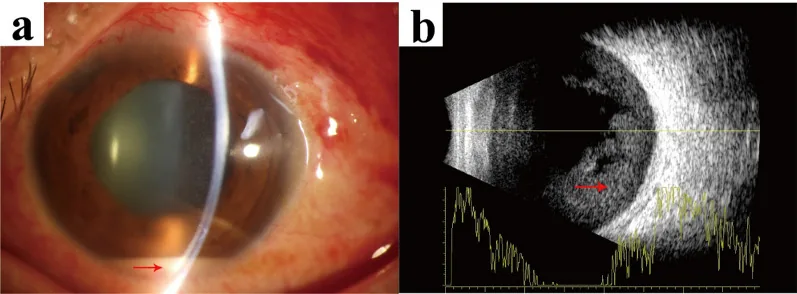
Stage I(ブレブ炎)
「赤の上の白(white-on-red)」:充血した結膜の上に白濁した濾過胞が特徴的。
濾過胞の混濁:黄白色に不透明化する。
軽度の前房反応:前房蓄膿を伴う場合と伴わない場合がある。
Stage II-III(BAE)
著明な結膜充血:Stage Iより広範かつ強い。
前房蓄膿:フィブリン析出を伴う。
硝子体混濁:Stage IIIで出現。IIIbでは眼底が透見不能となる。
前房蓄膿と明らかなブレブ感染を認めた場合、他の原因が証明されない限り眼内炎として取り扱う1)。濾過胞漏出がしばしば確認されるが、炎症性デブリが一時的に漏出部位を閉塞していることもある。
起炎菌は発症時期により異なる。100以上の起炎微生物が文献上報告されている1)。
| 発症時期 | 主な起炎菌 | 特徴 |
|---|---|---|
| 早期発症 | コアグラーゼ陰性ブドウ球菌 | 低毒性、予後比較的良好 |
| 晩期発症 | 連鎖球菌、H. influenzae | 高毒性、予後不良 |
グラム陽性球菌(ブドウ球菌属、連鎖球菌属)が最も多く、グラム陰性菌ではMoraxella属とHaemophilus属が主要である1)。まれにCapnocytophaga canimorsusなどの人獣共通感染症も報告されている2)。
濾過胞からの房水漏出が最大のリスク因子であり、感染リスクを26倍に高める1)。代謝拮抗薬の使用による濾過胞壁の菲薄化・無血管化が漏出リスクを増大させる。診察のたびにSeidel試験で漏出の有無を確認することが重要である。
ブレブの観察が基本であり、以下の5項目を確認する。
硝子体波及がない場合、積極的な局所抗菌薬治療を行う。
臨床的改善の24時間後に局所ステロイドの追加を検討するが、予後悪化の報告もあり慎重な判断を要する。
硝子体穿刺による検体採取と同時に、硝子体内抗菌薬注射を行う。
| 薬剤 | 投与量 | 備考 |
|---|---|---|
| バンコマイシン | 1mg/0.1mL | グラム陽性菌カバー |
| セフタジジム | 2.25mg/0.1mL | グラム陰性菌カバー |
| デキサメタゾン | 0.4mg/0.1mL | 補助的(炎症抑制) |
硝子体手術(PPV)は穿刺注入法よりも視力予後が優れるとの報告がある。ただし、近年のデータでは硝子体手術と硝子体内注射後の視力予後は同等との報告もある。
緑内障診療ガイドライン(第5版)では、術後早期の抗菌薬使用について以下のように推奨している4)。
濾過胞感染のリスク因子である漏出を認めた場合、適切な管理が必要である。
緑内障診療ガイドライン(第5版)では、術後1〜3ヶ月は抗菌薬の継続使用が強く推奨されている4)。その後は濾過胞漏出の有無など感染リスクに応じ、長期的にニューキノロン系眼軟膏の就寝前使用を検討する。漫然とした使用は避け、担当医と相談のうえ継続の判断を行う。
濾過胞関連感染症の病態は、緑内障濾過手術により形成された濾過胞が感染の入口(ポータル)となることに起因する。
線維柱帯切除術では、強膜弁の下から房水を結膜下に導いて濾過胞を形成させる。この濾過胞の壁が菲薄化あるいは漏出すると、涙液や眼周囲の常在菌が眼内に侵入しうる。代謝拮抗薬(MMC・5-FU)の使用は、結膜の杯細胞数を減少させてムチン産生を低下させるとともに、結膜の全般的な菲薄化と無血管化を促進する。これにより、細菌に対する物理的・免疫学的防御壁が減弱し、感染が成立しやすくなる。
起炎菌の病原性は発症時期と相関する1)。早期発症型BRIは白内障術後の眼内炎と同様の低毒性菌(コアグラーゼ陰性ブドウ球菌)が主体であり、涙液や眼瞼の常在菌叢に由来する。これらの菌は外毒素を産生せず、適切な治療で良好な予後が得られる。
一方、晩期発症型は連鎖球菌属(S. pneumoniae、S. viridans群)やHaemophilus influenzae、Serratia属などのより毒性の高い菌が関与する1)。これらの菌は外毒素産生や組織侵入性に優れ、急速な臨床経過と不良な視力予後をもたらす。
Kandarakisら(2022)は文献上報告されたBRI起炎菌を網羅的にレビューし、100以上の微生物を同定した。グラム陽性球菌ではStreptococcus属(約385分離株)とStaphylococcus属(約296分離株)が圧倒的に多く、グラム陰性菌ではMoraxella属(約79例)とHaemophilus属(約63例)が主要であった1)。
Yangら(2021)は、トラベクレクトミー10年後にCapnocytophaga canimorsusによるブレブ炎を発症した81歳男性を報告した。患者は飼い犬に日常的に顔を舐められており、犬の口腔内常在菌が濾過胞を介して感染したと考えられた。トラベクレクトミーの再建術により良好な視力予後(20/70)を得た2)。
Kandarakisら(2022)のレビューでは、従来の培養による陰性率が21〜86%と高い問題を指摘している。リアルタイムPCRは細菌検出率を47.6%から95.3%に向上させる。さらに、メタゲノミクス(高スループットDNAシーケンシング)による網羅的な微生物同定が次世代の診断手法として期待されている1)。
Paikら(2025)のレビューでは、MIGSはトラベクレクトミーやチューブシャント手術と比較してブレブ炎のリスクが低いことが示されている。MIGSデバイスは上強膜静脈圧に逆らって房水を排出する設計であるため、術後低眼圧のリスクが低く、代謝拮抗薬を使用しないことから感染リスクも軽減される3)。
Yangら(2021)のCapnocytophaga canimorsusブレブ炎の報告は、ペット動物との接触が濾過手術既往眼における新たな感染リスク因子となりうることを示した。DNAシーケンシングにより、従来培養困難であった病原体の同定が可能となっている2)。