非バルブ型
ClearPath / Baerveldt
眼圧制御:被膜の抵抗のみに依存。長期的により低い眼圧達成4)
術後早期:リガチャー・リップコードで過剰濾過を防止1)
低眼圧リスク:バルブ型よりやや高い(4.5% vs 0.4%)4)

Ahmed ClearPath(New World Medical社、カリフォルニア州ランチョクカモンガ)は、緑内障の外科的管理に用いられる非バルブ型の緑内障ドレナージデバイス(glaucoma drainage device:GDD)である。2019年に米国FDAの承認を受け、市場に導入された。
緑内障ドレナージデバイスは、眼内からチューブを通じて房水をプレートへ導出し、プレート周囲に形成される被膜(カプセル)を通じて房水を周囲組織に吸収させることで眼圧下降を得るデバイスである2)。バルブ(調圧弁)の有無により以下の2種類に大別される2)。
米国緑内障学会(AGS)の調査では、回答者の17%が非バルブ型シャントとしてAhmed ClearPathを選好していると報告されている。
Ahmed ClearPathは手術手技の簡便化と合併症リスクの軽減を目指した設計上の特徴を有する。
250 mm²モデルは直筋の分離なしに筋肉間に設置可能である。
バルブ型(Ahmed緑内障バルブ)は調圧弁により術直後から房水流出が可能で、過度の低眼圧を防ぐ仕組みを持つ。非バルブ型(ClearPath、Baerveldt)は調圧弁がないため、術後早期の過剰濾過を防ぐためにチューブの結紮(リガチャー)が必要である。非バルブ型は一般にバルブ型より良好な長期眼圧コントロールが得られるが、術後低眼圧のリスクがやや高い4)。
緑内障ドレナージデバイスは従来、線維柱帯切除術(トラベクレクトミー)が不成功に終わった症例、あるいは成功が見込めない症例に対して使用されてきた2)。具体的には以下の適応が挙げられる。
近年、緑内障ドレナージデバイスの適応は拡大傾向にある。Medicareデータでは1994年から2012年にかけてシャント手術件数が増加し、トラベクレクトミー件数は同時期に減少した2)。
日本では、Baerveldt緑内障インプラントとAhmed緑内障バルブの2種類が保険診療で使用可能である。線維柱帯切除術の成績が不良な再手術眼や、内眼手術既往のある緑内障眼が良い適応となる。
より低い眼圧を目標とする症例ではBaerveldt緑内障インプラント(非バルブ型)が選択され、術後低眼圧が危険な症例(無水晶体眼、IOL縫着眼、駆逐性出血既往、ぶどう膜炎続発緑内障など)ではAhmed緑内障バルブ(バルブ型)が選択される傾向にある。
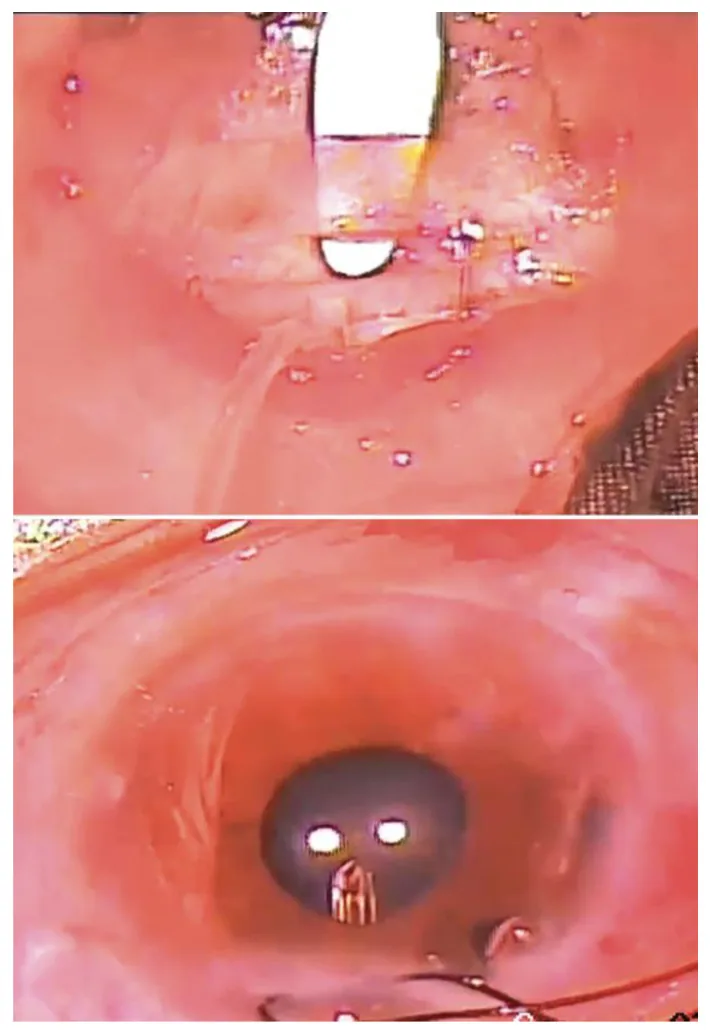
緑内障ドレナージデバイス手術の基本手技はバルブ型・非バルブ型で共通する部分が多い。
非バルブ型デバイス(ClearPath・Baerveldt)では、以下の追加手技が必要である。
Ahmed緑内障バルブ(バルブ型)では、調圧弁のプライミング(灌流液注入による弁の動作確認)が必要であるが、チューブ結紮やSherwood slitは不要である。
非バルブ型
ClearPath / Baerveldt
眼圧制御:被膜の抵抗のみに依存。長期的により低い眼圧達成4)
術後早期:リガチャー・リップコードで過剰濾過を防止1)
低眼圧リスク:バルブ型よりやや高い(4.5% vs 0.4%)4)
バルブ型
Ahmed緑内障バルブ
眼圧制御:調圧弁で理論上8 mmHg以下を防止。術直後から眼圧下降
術後早期:プライミングのみ。結紮・Sherwood slit不要
合併症:術後合併症頻度は低いが、長期眼圧コントロールは非バルブ型に劣る4)
DBACS試験(ClearPath 350 vs Baerveldt 350のRCT)では、両群で手術時間、ベンティングスリット数、ウィック数、手術象限、グラフト種類、チューブ位置に有意差は認められなかった1)。
術後は抗菌薬点眼を約2週間、ステロイド点眼を漸減しつつ約6ヶ月間行う。非バルブ型デバイスではリガチャーが溶解する4〜6週後まで眼圧が20 mmHg前後の高値で推移することが多く、降圧点眼薬を併用しながら経過観察を行う。1〜2ヶ月後に眼圧が下降してくることが多い。
緑内障ドレナージデバイス手術に共通する主な合併症を以下に示す2)。
| 合併症 | 頻度(TVT/ABC/AVB試験) |
|---|---|
| チューブ露出 | 1〜7% |
| 複視・眼球運動障害 | 6〜12.7% |
| 角膜内皮障害 | 11〜16% |
チューブ露出は下方留置で頻度が高い。角膜内皮障害はチューブが角膜に近接する場合にリスクが上昇する。
リップコードはチューブ内腔に留置する太い非吸収糸(4-0ポリプロピレン)である。チューブを部分的に閉塞し、房水流出量を制限する。リガチャー(結紮糸)が自然溶解した後、外来でスリットランプ下に抜去することで流出量を段階的に増加させ、より精密な眼圧コントロールが可能となる1)。
緑内障ドレナージデバイスはシリコン製チューブとプレートで構成される。チューブを通じて前房の房水がプレートへ導出され、プレート周囲に術後数週で形成される結合織の被膜(カプセル)を介して周囲組織に房水が吸収される2)3)。眼圧下降は主にこの被膜における流出抵抗に依存する。
非バルブ型デバイスでは流出抵抗が被膜のみに依存するため、被膜が十分に形成されるまでの術後早期にリガチャーによるチューブ閉塞が不可欠となる1)。バルブ型デバイスでは調圧弁が追加の流出抵抗を提供し、術直後からの房水排出と低眼圧予防を両立させる。
ClearPathはBaerveldtと同じ非バルブ型であるが、以下の独自設計を有する。
Langenbergらの実験室研究では、ClearPath 350とBaerveldt 350の流体抵抗および縫合アイレットの完全性は同等であったと報告されている。
プレート面積が大きいほど理論的には被膜面積が増え、流出抵抗が低下する。複数の後方視的研究で、より大きなプレート面積が低い眼圧およびより少ない降圧薬使用と関連することが示されている2)。一方、350 mm²と500 mm²のBaerveldtを比較した前向き研究では、350 mm²の方が5年時の成功率が高かったとの報告もあり、大きさが必ずしも有利とは限らない2)。
Quistら(2025)はDuke大学でClearPath 350とBaerveldt 350を比較する初のランダム化比較試験(DBACS)を実施した1)。76例が登録され(BVT群37例、ACP群39例)、70例が手術を受け、61例が12ヶ月の追跡を完了した。ベースライン眼圧は両群間で有意差なし(BVT 21.7±7.1 vs ACP 22.4±6.7 mmHg)。
DBACS試験の主要結果を以下に示す1)。
| 項目 | Baerveldt 350 | ClearPath 350 | p値 |
|---|---|---|---|
| 12ヶ月眼圧 | 14.1±4.3 mmHg | 11.4±3.9 mmHg | 0.010 |
| 眼圧低下率 | -30.7% | -44.1% | 0.038 |
ClearPath群は6週(12.1 vs 16.3 mmHg, p=0.032)、3ヶ月(12.8 vs 16.5 mmHg, p=0.026)、12ヶ月の各時点でBaerveldt群より有意に低い眼圧を達成した1)。降圧薬使用数は両群で同等であり、合併症も低頻度かつ両群間で差を認めなかった。本試験は目標症例数(304例)に対して76例と不足しているものの、主要評価項目において統計学的有意差が検出された1)。
ElhusseinyとVanderVeenは小児緑内障7眼におけるClearPathの初期成績を報告した。中央値12ヶ月のフォローアップで、平均眼圧は36±3.5 mmHgから12.4±2.8 mmHgへ有意に低下した(p<0.001)。降圧薬数も2.7±0.6剤から0.7±0.8剤へ減少した(p=0.0009)。
Groverらの多施設後方視的研究では、成人104眼(63.5%が原発開放隅角緑内障〔POAG〕)を対象にClearPathの成績を評価した。6ヶ月時点で平均眼圧は26.3±9 mmHgから13.7±4.7 mmHgへ有意に低下し(p<0.0001)、91.8%の眼で18 mmHg以下を達成した。主な合併症は前房内炎症(16.3%)、前房出血(15.4%)、早期低眼圧(6.7%)であった。
緑内障ドレナージデバイス全般の長期成績として、Tube Versus Trabeculectomy(TVT)試験の5年成績では、Baerveldt群の累積失敗率が29.8%、線維柱帯切除術群が46.9%で、線維柱帯切除術群で有意に高かった(p=0.02)4)。
Ahmed緑内障バルブとBaerveldt緑内障インプラントの5年比較(ABC/AVB試験のメタアナリシス)では、Baerveldt群でより低い眼圧が得られたが、低眼圧発生率がBaerveldt群で有意に高かった(4.5% vs 0.4%, p=0.002)4)。
DBACS試験ではClearPath 350群が12ヶ月時点でBaerveldt 350群より有意に低い眼圧を達成した1)。しかし、試験規模は小さく追跡期間も1年と短いため、長期的な安全性・有効性の評価にはさらなる研究が必要である。両デバイスの構造的差異がどのように臨床アウトカムに影響するか、今後の大規模・長期試験で検証されることが期待される。