初期(XN〜X1B)
夜盲(XN):桿体細胞のロドプシン形成不全による。血清レチノール1.0 μmol/L未満で出現し始める3)。
結膜乾燥症(X1A):結膜の光沢消失と乾燥。杯細胞の消失・ムチン分泌低下による。
Bitot斑(X1B):角質化した上皮細胞とCorynebacterium xerosisの混合堆積物。耳側球結膜に三角形の泡状白色沈着物として出現。

眼乾燥症(Xerophthalmia)は、重度のビタミンA欠乏症(VAD)によって引き起こされる一連の眼疾患の総称である。ビタミンAは角結膜上皮の正常な分化に必須の脂溶性ビタミンであり、その欠乏は結膜、角膜、および網膜に段階的な障害をもたらす。
WHO推定によれば、世界で約2億2,800万人の子供がVADに罹患しており、毎年25万〜50万人の小児が眼乾燥症により失明している3)。先進国では稀であり、米国における有病率は0.3%(2013年CDC調査)にとどまる1)。
ただし、特定の基礎疾患を有する患者ではVAD有病率が高い1)。
日本ではビタミンA欠乏をみることはほぼないが、摂食障害やアルコール依存症に伴って稀に発症することが知られている。
日本では栄養不足によるVADは極めて稀であるが、摂食障害、アルコール依存症による腸管吸収不良、あるいは胃切除後の脂溶性ビタミン吸収障害に伴い発症することがある。近年では自閉スペクトラム症の極端な偏食が原因となる報告もみられる。
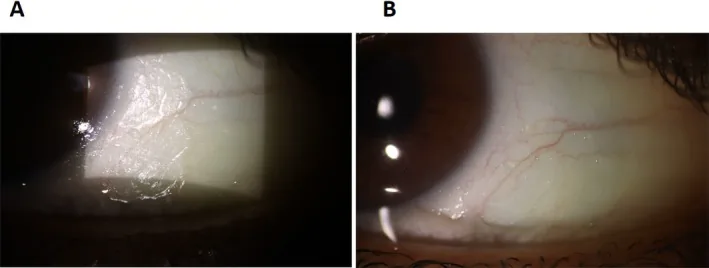
VADの進行度に応じて症状が異なる。
小児ではVADの初期徴候なしに、麻疹や下痢のあとに突然角膜潰瘍を発症することがある。暗い場所で消極的になる・怖がるなどの行動変化がVADのサインとなりうる。
WHOは眼乾燥症を以下の病期に分類している(1982年)。
| WHO分類 | 病態 | 失明リスク |
|---|---|---|
| XN | 夜盲 | なし |
| X1A / X1B | 結膜乾燥症 / Bitot斑 | なし |
| X2 | 角膜乾燥症 | あり |
| X3A / X3B | 角膜潰瘍 / 角膜軟化症 | 高い |
| XS / XF | 角膜瘢痕 / 眼底変化 | 瘢痕に依存 |
初期(XN〜X1B)
夜盲(XN):桿体細胞のロドプシン形成不全による。血清レチノール1.0 μmol/L未満で出現し始める3)。
結膜乾燥症(X1A):結膜の光沢消失と乾燥。杯細胞の消失・ムチン分泌低下による。
Bitot斑(X1B):角質化した上皮細胞とCorynebacterium xerosisの混合堆積物。耳側球結膜に三角形の泡状白色沈着物として出現。
進行期〜重症期(X2〜X3B)
角膜乾燥症(X2):角膜が光沢を失い混濁する。点状表層角膜症を呈し、急速に角膜潰瘍へ進行しうる。
角膜軟化症(X3A/B):液化壊死による角膜実質の融解。数日で角膜穿孔に至りうる最重症型。
角膜瘢痕(XS):角膜潰瘍後の瘢痕。しばしば対称性・両眼性。
進行例では不可逆的な合併症を生じる。自閉症児3例の報告では、重症VAD(血清ビタミンA ≤0.12 μmol/L)により角膜穿孔から眼球摘出に至った例や、視神経萎縮による恒久的な視力障害(最良でも手動弁〜0.01)を呈した例が報告されている2)。
Khanら(2021)は腸管切除術後24歳女性の結膜生検で、扁平上皮化生とケラチン真珠形成を確認した5)。これはVADによる眼表面変化の組織学的裏付けとなる所見である。
Bitot斑はビタミンA補充療法により約2週間以内に改善する1)。ただし夜盲の回復には4週間以上かかることがある。角膜乾燥症の段階までに治療を開始すれば視力の完全回復が期待できるが、角膜軟化症まで進行すると瘢痕が残る可能性がある。
発展途上国では日常的な栄養不足が最大の原因である。先進国では以下が問題となる。
膵臓・肝臓・腸管疾患によるビタミンA吸収障害が先進国の主因である。
自閉スペクトラム症やダウン症に伴う極端な偏食(特定の食品のみ摂取)はVADの重要なリスク因子である2)3)。偏食のある子供では血清ビタミンA値の定期的な確認が推奨される。
散瞳下の細隙灯顕微鏡検査が基本である。結膜の光沢消失・Bitot斑・角膜混濁の有無を評価する。食事歴、吸収不良の既往、アルコール摂取歴の聴取が重要である。
角膜軟化症は非常に重度のVADを示す所見であり、内科的緊急事態として扱う。
ビタミンA内服が基本である。
WHOは眼乾燥症(重度栄養不良・麻疹合併例を含む)に対し、高用量ビタミンAの経口投与を推奨している1)。
| 対象 | 1回投与量(IU) |
|---|---|
| 0〜5か月 | 50,000 |
| 6〜11か月 | 100,000 |
| 12か月以上 | 200,000 |
投与スケジュールは1日目、2日目、14日目の計3回である1)。吸収不良を伴う場合は筋肉内注射が推奨される1)4)。亜鉛欠乏を合併する場合は亜鉛の同時補充が必要である。
人工涙液・ヒアルロン酸点眼による眼表面の潤滑を行う。角膜穿孔例では全層角膜移植術が適応となる場合がある。無虹彩など輪部幹細胞不全を合併する複雑例では、高用量ビタミンA(200,000 IU)投与に加え抗緑内障薬・局所抗菌薬を併用する6)。
Sharmaら(2021)はFrey手術後の12歳女児で、ビタミンA筋注+経口投与により2週間以内に角結膜所見が完全消失し、視力が20/20に回復したと報告した4)。血清レチノールは12週で正常化した。
Bitot斑は治療開始後約2週間で改善するが、夜盲の回復には少なくとも4週間を要する1)。角膜軟化症が生じた場合は回復が困難であり、瘢痕や恒久的視力障害が残る。角膜軟化症を発症した小児の約2/3は数か月以内に死亡するとされる。
角膜乾燥症(X2)までの段階であれば、ビタミンA補充により2週間以内に眼所見が改善し、視力の完全回復が期待できる4)。Bitot斑も約2週間で改善するが、夜盲は4週間以上かかることがある1)。角膜軟化症に至った場合は不可逆的な瘢痕が残りうる。
ビタミンAはレチノール・レチナール・レチノイン酸などの総称であり、食事から既成ビタミンA(動物性食品)またはプロビタミンAカロテノイド(緑黄色野菜)として摂取される。十二指腸で吸収されたのち、肝星細胞に体内総量の80〜90%が貯蔵される。血中へはプレアルブミン(トランスサイレチン)およびレチノール結合タンパク質(RBP)と結合して放出される。
眼におけるビタミンAの主要な機能は以下の2つである。
VADが生じると、角結膜上皮でケラチノサイトトランスグルタミナーゼの過剰発現が起こり、異常な角化が進行する7)。この過程で杯細胞が消失し、ムチン分泌が低下する。
病態は以下の順序で段階的に進行する。
角膜軟化症の段階ではコラゲナーゼ活性の亢進により角膜実質が急速に融解し、わずか数日で穿孔に至ることがある。
TFOS DEWS IIIの報告では、経口ビタミンA補充がドライアイ患者の涙液の質を改善する一方、涙液量には影響しなかったとされる8)。局所ビタミンA点眼はより安定した涙膜安定性と眼表面の改善を示しており、シクロスポリンAとの併用療法も検討されている8)。
Azmiら(2023)は自閉症児3例のVADによる重篤な眼乾燥症を報告し、視神経萎縮に至った不可逆的症例の存在を強調した2)。自閉スペクトラム症やダウン症など偏食リスクの高い小児に対する定期的な血清ビタミンA値スクリーニングの重要性が提唱されている。
Roux-en-Y胃バイパスなどの肥満手術後はVADリスクが高く、術後の眼表面変化に関するモニタリングの必要性が指摘されている7)。術後6週で35%にVADが認められたという報告もあり、早期発見・早期介入の体制構築が求められている。