眼瞼型の所見
石垣状巨大乳頭:上眼瞼結膜に直径1 mmを超える扁平な乳頭が密集し、石垣状を呈する。乳頭の活動性指標は充血の程度と乳頭間の粘性分泌物である。
結膜充血:びまん性の結膜充血を認める。
乳頭頂部のフルオレセイン染色:活動性の高い乳頭は頂部がフルオレセインで染色される。

春季カタル(vernal keratoconjunctivitis: VKC)は、結膜に増殖性変化を伴うアレルギー性結膜疾患である。I型アレルギーに加え、Th2細胞主導のIV型過敏反応が病態に関与する。「vernal」は春を意味し、春季に増悪する傾向から名付けられた。
主に高温乾燥地帯(西アフリカ、地中海沿岸、中東、日本、インド)に多い。5歳から25歳の間に発症し、発症年齢のピークは10〜12歳である。男児に多いが、加齢とともに男女差は縮小する。通常は思春期以降に自然寛解するが、12%程度の患者で成人期まで症状が持続する。
VKCは臨床所見の部位により3型に分類される。
多くの患者に本人または家族のアトピー歴が認められる。一卵性双生児とその父親においてNGS(次世代シーケンシング)によるHLA解析が行われ、HLA-DQB1*05:01、HLA-DRB1*01:01:01、HLA-A*32:01:01がVKCとの関連を示した2)。ただし、直接的な遺伝子座との明確な相関は解明されていない。
VKCは10歳未満で発症し上眼瞼結膜の巨大乳頭が主体で、通常は思春期に自然寛解する。一方、AKCは20〜50代で発症し下眼瞼結膜が主に侵され、慢性経過をとり結膜の瘢痕化や角膜混濁を残しやすい。アトピー性皮膚炎に伴う春季カタルは重症化しやすく、両者の鑑別が困難な場合がある。
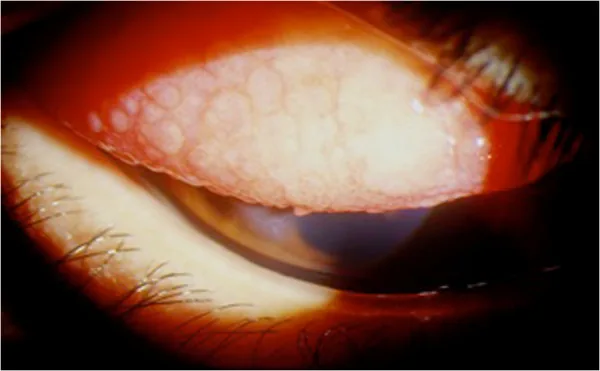
活動性の高い状態では、起床時に激しい不快感と眼瞼痙攣・粘液性分泌物のため動けなくなることがあり、「モーニング・ミザリー(morning misery)」と呼ばれる。
眼瞼型の所見
石垣状巨大乳頭:上眼瞼結膜に直径1 mmを超える扁平な乳頭が密集し、石垣状を呈する。乳頭の活動性指標は充血の程度と乳頭間の粘性分泌物である。
結膜充血:びまん性の結膜充血を認める。
乳頭頂部のフルオレセイン染色:活動性の高い乳頭は頂部がフルオレセインで染色される。
眼球型の所見
トランタス斑(Horner-Trantas dots):角膜輪部にみられる白色の斑点で、変性上皮細胞と好酸球からなる。
輪部の腫脹・肥厚:ゼラチン状に見える輪部乳頭が融合することがある。
偽老人環(pseudogerontoxon):末梢の浅層実質に灰白色の脂質沈着を認める。
角膜合併症は疾患の重症度に応じて進行する。
VKC瘢痕期の角膜組織学的検討では、上皮過形成、Bowman層の消失、間質の硝子化・血管新生が確認されている3)。免疫組織化学的にはABCG2(輪部幹細胞マーカー)が消失する一方、p63は残存しており、輪部幹細胞の部分的な機能障害が示唆されている3)。
まれな合併症として瞼板結膜の角化がある。長期罹患例で初めて両眼性の瞼板結膜角化が報告され、切除および結膜自家移植で管理された4)。強膜レンズ(PROSE)の装用により矯正視力0.8が得られた4)。
好酸球から放出されるMBP(major basic protein)やECP(eosinophil cationic protein)が角膜上皮に直接的な細胞障害を与える。これに巨大乳頭の機械的摩擦が加わり、上方角膜に楕円形の浅い潰瘍が形成される。潰瘍底にフィブリンと粘液が沈着すると角膜プラークとなり、上皮の再生が妨げられる。活動期にはMBPやECPに抗菌作用があるため感染しにくいが、寛解期のステロイド漫然投与は細菌性角膜炎のリスクを高める。
VKCは単純なIgE介在性のI型アレルギーのみでは説明できない。CD4陽性Th2細胞主導のIV型過敏反応が重要な役割を果たす。
VKCやアトピー性角結膜炎はアレルギー性角膜疾患として感染性角膜炎のリスク因子でもある6)。
正確な機序は解明されていないが、性ホルモンが結膜局所の好酸球動員に促進的に作用するという仮説がある。思春期以降に男女差が縮小し、症状も軽減することから、内分泌的な因子の関与が示唆されている。
特徴的な臨床所見(石垣状巨大乳頭、トランタス斑、シールド潰瘍)と季節性の瘙痒感から臨床的に診断する。上眼瞼の翻転による巨大乳頭の確認が重要である。
局所でI型アレルギーを証明できれば確定診断群、全身で証明できれば準確定診断群となる。
| 鑑別疾患 | 鑑別のポイント |
|---|---|
| アトピー性角結膜炎(AKC) | 20〜50代発症、下眼瞼結膜主体、慢性・瘢痕化 |
| 季節性アレルギー性結膜炎 | 増殖性変化なし、乳頭軽度 |
| 巨大乳頭結膜炎(GPC) | CL・義眼などの異物が原因 |
抗アレルギー点眼薬を基盤とし、重症度に応じて免疫抑制点眼薬・ステロイド点眼薬を組み合わせる。改善後はまずステロイドを漸減・中止し、次いで免疫抑制点眼薬を漸減する。再燃時は免疫抑制点眼薬を再開し、それでも抑制できない場合にステロイドを追加する。
抗アレルギー点眼薬
メディエーター遊離抑制薬:マスト細胞膜を安定化しヒスタミンの遊離を抑制する。クロモグリク酸ナトリウムなど。
H1受容体拮抗薬:ヒスタミンの受容体結合を競合的に阻害する。オロパタジン、エピナスチンなど。瘙痒感が強い場合に選択する。
免疫抑制点眼薬
シクロスポリン点眼液(0.1%):2006年発売。1日3回点眼。眼球型VKCにより有効とされる。
タクロリムス点眼液(0.1%):2008年発売。1日2回点眼。シクロスポリンより免疫抑制効果が強く、アトピー性皮膚炎合併例に有効とされる。
| 薬剤 | 濃度 | 点眼回数 | 特徴 |
|---|---|---|---|
| パタノール® | 0.1% | 1日4回 | H1受容体拮抗+遊離抑制 |
| フルメトロン® | 0.1% | 1日4回 | 低吸収性ステロイド |
| タリムス® | 0.1% | 1日2回 | 免疫抑制(タクロリムス) |
| パピロックミニ® | 0.1% | 1日3回 | 免疫抑制(シクロスポリン) |
| リンデロン® | 0.1% | 1日4回 | 高力価ステロイド |
VKCは若年者に多い疾患であり、若年者ほどステロイドレスポンダー(ステロイド緑内障)の割合が高い。定期的な眼圧測定が必須である。ステロイドの長期不適切使用は緑内障や白内障のリスクとなる。
免疫抑制点眼薬とステロイド点眼薬でコントロールできない場合は、ステロイド内服、ステロイド瞼板下注射、巨大乳頭切除術を考慮する。小児へのステロイド内服は成長障害の問題があり、できるだけ短期間の処方とし小児科との連携が必要である。巨大乳頭切除術は炎症細胞の減量が目的であり完全切除は不要だが、術後も免疫抑制点眼薬・ステロイド点眼薬の継続が必須である。ただし、免疫抑制点眼薬の進歩により外科的治療が必要となる頻度は大幅に減少している。
タクロリムスはシクロスポリンより免疫抑制効果が強く、重症例やシクロスポリンに反応しない例に選択される。シクロスポリンは眼球型VKCにより有効、タクロリムスはアトピー性皮膚炎を合併する症例により有効とされる。治療指針ではパターン1〜4の重症度分類に基づき、軽症例ではシクロスポリンから開始し、効果不十分であればタクロリムスに変更する。タクロリムスによるプロアクティブ療法(寛解後も低頻度で継続)は再燃予防に有効である。
VKCの病態はI型アレルギー(即時型)とIV型過敏反応(遅延型)の両方が関与する複合的な免疫反応である。
I型アレルギーでは、涙液中に飛入した抗原がIgEを介してマスト細胞の脱顆粒を引き起こす。即時相ではヒスタミンが遊離され充血と瘙痒を生じ、遅発相ではロイコトリエンなどの新規合成メディエーターが炎症を増幅する。
IV型過敏反応では、Th2細胞がIL-4、IL-5、IL-13を産生し好酸球の動員・活性化を促進する。活性化した好酸球はMBP、ECPなどの細胞障害性蛋白を放出し、角膜上皮への直接的な障害を引き起こす。
近年、Th2サイトカインのシグナル伝達にJAK/STAT経路が重要な役割を果たすことが注目されている。JAK1はIL-4、IL-5、IL-13、IL-31およびTSLP(thymic stromal lymphopoietin)のシグナル伝達を媒介し、アレルギー性炎症の中心的な経路となっている1)。
乳頭の基本病態は血管新生反応である。結膜上皮の肥厚と上皮下の炎症細胞増殖を伴い、線維性組織が乳頭状に隆起する。中心に血管があり、その周囲にリンパ球や形質細胞を主体とした細胞浸潤を認める。硬い瞼板の上で生じるため上眼瞼結膜に好発する。
VKC瘢痕期の角膜ボタンの組織学的検討では、上皮過形成、Bowman層の消失、間質の硝子化および血管新生が確認された3)。免疫組織化学ではABCG2(輪部幹細胞マーカー)が消失する一方、基底細胞マーカーのp63は保持されていた3)。この結果はVKCによる輪部幹細胞障害が完全な幹細胞不全ではなく部分的な機能障害であることを示唆しており、角膜移植(DALKやPKP)後の予後評価に重要な知見である3)。
重症VKCとアトピー性皮膚炎を合併した18歳女性において、JAK1選択的阻害薬であるウパダシチニブの内服開始後2か月で巨大乳頭の著明な平坦化が得られた1)。血清IgE 8973 IU/mLと著しい高値を示す難治例であったが、タクロリムス点眼との併用で良好な経過をたどった1)。
JAK1はTh2サイトカイン(IL-4、IL-5、IL-13、IL-31)およびTSLPのシグナル伝達を媒介する1)。ウパダシチニブによるJAK1阻害はこれらのサイトカインを包括的に抑制し、従来の免疫抑制点眼薬に抵抗する重症例への新たな治療選択肢となる可能性がある1)。
一卵性双生児とその父親のVKC家系においてNGS(次世代シーケンシング)によるHLA解析が行われ、HLA-DQB1*05:01、HLA-DRB1*01:01:01、HLA-A*32:01:01がVKCとの関連を示した2)。VKCにおけるNGSベースのHLA解析としては初の報告である2)。
VKC瘢痕期の角膜組織を免疫組織化学的に検討した研究では、3例4眼(DALKまたは全層角膜移植施行例)において上皮過形成、Bowman層消失、間質硝子化、血管新生が確認された3)。ABCG2陰性・p63陽性の所見から部分的な輪部幹細胞機能障害と結論された3)。
長期罹患(小児期発症から20年以上)のVKC患者で両眼性の瞼板結膜角化が報告された4)。これはVKCにおける瞼板結膜角化の初めての症例報告である4)。病変切除と結膜自家移植で管理され、4年間再発なく経過した4)。強膜レンズ(PROSE)装用により矯正視力0.8(20/25)が達成された4)。
VKC患者における成長ホルモン欠損(GHD)の有病率上昇が報告されている5)。11歳男児のVKC症例でGHDの合併が確認され、タクロリムス点眼とフルオロメトロン点眼への変更後6週間で著明な改善を得た5)。GH療法がCRPやIL-6などの炎症マーカーを低下させるとの報告もあり、VKCの病態へのGHDの関与が注目されている5)。
生物学的製剤として、抗IgEモノクローナル抗体であるオマリズマブの有効例が報告されている。また、抗IL-4受容体α抗体であるデュピルマブについてアトピー性角結膜炎を対象とした臨床試験が進行中であり、VKCへの応用も期待される。
ウパダシチニブ(JAK1選択的阻害薬)が難治性VKCに有効であったとする症例報告がある1)。JAK1はTh2サイトカインのシグナル伝達を包括的に媒介するため、理論的にはVKCの病態に合致した作用機序を持つ。ただし、現時点ではVKCに対する適応承認はなく、症例報告の段階にとどまる。今後、安全性と有効性を検証する臨床試験が待たれる。