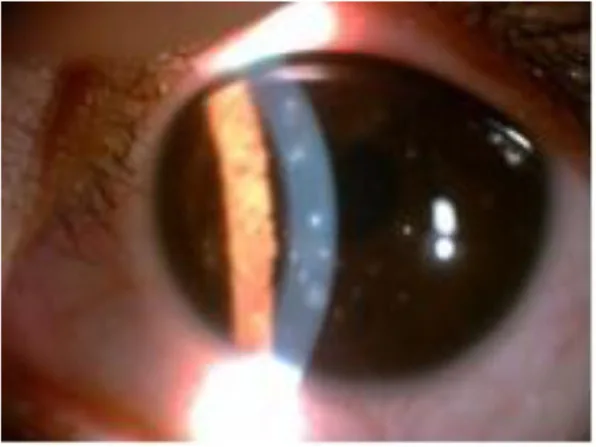
細隙灯顕微鏡検査
角膜所見:わずかに隆起した灰白色で類円形の点状混濁が角膜中央部に散在する。各病巣は顆粒状変化の集合体であり、角膜表面からわずかに隆起している。
フルオレセイン染色:混濁の中心部が点状に染色される。急性期の病変はフルオレセインでわずかに染色されるが、生体染色(ローズベンガル、リサミングリーン)では染色される場合とされない場合がある。
結膜所見:結膜は静穏であり、充血や炎症反応を欠く点が特徴的である。

Thygeson点状表層角膜炎(Thygeson superficial punctate keratitis: TSPK)は、1950年にPhillips Thygesonが報告した特異な表層角膜炎である。結膜や角膜実質に炎症を伴わず、角膜上皮から実質ごく浅層に限局した再発性・多発性の点状病変を呈する。
男女差はなく各年齢層でみられるが、一部の研究では女性優位の報告がある。発症年齢の中央値は29歳で、2歳半から70歳まで幅広い年齢層での報告がある。有病率および分布は過小評価されている可能性がある。
増悪と寛解を繰り返す経過が特徴的である。1回のエピソードは1〜2ヶ月持続し、寛解までに6週間を要する。4年経過するとほとんどの症例で再発しなくなるとの報告がある一方、20年以上持続する症例もあり、最長41年の記録がある。最終的には臨床的後遺症を残さず消退する傾向にある。
両者はいずれも角膜上皮〜上皮下に多発性の点状〜斑状混濁を呈するが、臨床的に異なる。アデノウイルス角膜炎後の多発性上皮下浸潤(multiple subepithelial infiltration)は先行するウイルス性結膜炎の既往があり、結膜炎症を伴うことが多い。一方、TSPKでは先行するウイルス感染の既往がなく、結膜は静穏である。また、TSPKの各病巣はより小さな点状病巣の集合体であるのに対し、上皮下浸潤は比較的均一な混濁を呈する。1つ1つの病巣が大きく斑状の場合は銭形角膜炎(dimmer nummular keratitis)を考慮する。
病因は不明であるが、ウイルス性および免疫学的機序の2つの仮説がある。
ウイルス説では、1974年にLempらがTSPK患者の角膜表面から水痘帯状疱疹ウイルス(VZV)を分離した1例が報告されている。しかし、PCR検査を用いた研究では水痘帯状疱疹ウイルスは検出されず、ウイルス病因説は否定的である。
免疫学的機序として、HLA-DR3との有意な関連が報告されている1)。HLA-DR3は複数の自己免疫疾患(グルテン腸症、アジソン病、シェーグレン症候群、全身性エリテマトーデス)にも関連するクラスII MHC分子である。シクロスポリンAやタクロリムスなどの免疫抑制薬が有効であることから、T細胞介在性の免疫機序が示唆されている。
セリアック病はHLA-DQ2およびHLA-DQ8と強く関連する自己免疫疾患であり、90%以上の患者がHLA-DR3アレルを保有する。Tagmoutiらは4年間のセリアック病歴を有する20歳女性にTSPKが発症した症例を報告し、HLA-DR3の共有がTSPKとセリアック病の免疫遺伝学的関連を示唆するとした1)。
HLA-DR3はクラスII主要組織適合遺伝子複合体(MHC)分子であり、免疫応答の調節に関与する。DarrellらはTSPK患者においてHLA-DR3の保有率が有意に高いことを報告した。HLA-DR3はセリアック病、アジソン病、シェーグレン症候群など複数の自己免疫疾患にも関連している。TSPKでは上皮内の抗原(おそらくウイルス抗原)に対するT細胞介在性の過敏反応が推定されており、HLA-DR3がこの免疫応答の感受性を高めていると考えられている1)。
細隙灯顕微鏡検査
角膜所見:わずかに隆起した灰白色で類円形の点状混濁が角膜中央部に散在する。各病巣は顆粒状変化の集合体であり、角膜表面からわずかに隆起している。
フルオレセイン染色:混濁の中心部が点状に染色される。急性期の病変はフルオレセインでわずかに染色されるが、生体染色(ローズベンガル、リサミングリーン)では染色される場合とされない場合がある。
結膜所見:結膜は静穏であり、充血や炎症反応を欠く点が特徴的である。
共焦点顕微鏡検査
星芒状高反射性堆積物:表層および基底上皮細胞層に星芒状(starburst-like)の高反射性堆積物の集合体を認める。
ランゲルハンス細胞の侵入:基底上皮層へのランゲルハンス細胞の侵入が認められ、免疫学的機序の関与を示唆する。
前部実質混濁:疾患の持続期間が長い眼ほど変化が重度である。
| 鑑別疾患 | TSPKとの鑑別点 |
|---|---|
| 上皮型角膜ヘルペス | 片眼性、角膜知覚低下、樹枝状潰瘍 |
| アデノウイルス角膜炎 | 先行結膜炎、結膜充血あり |
| ブドウ球菌性上皮性角膜炎 | 眼瞼炎合併、周辺部に多い |
そのほか、乾性角結膜炎、神経麻痺性角膜炎、再発性角膜びらん、春季カタル、薬剤毒性角膜症との鑑別を要する。角膜中央部の点状表層角膜症を認めた場合、TSPKと神経麻痺性角膜症を鑑別に挙げる。
薬物治療
ステロイド点眼:TSPKの主要治療である。0.1%フルオロメトロン点眼1日4回で速やかに病変は消退する。再燃が多いため、症状消退後もステロイド点眼を数ヶ月かけて漸減する。可能な限り最小用量・最低濃度で維持する。
シクロスポリン点眼:ステロイドの代替として有効である。Tagmoutiらは2%シクロスポリンA点眼1日3回を6ヶ月漸減投与し、完全寛解を達成した。3年間の経過観察で再発を認めなかった1)。
タクロリムス:点眼薬および軟膏として使用され、一定の効果が報告されている。
その他の治療
人工涙液:臨床症状の部分的な緩和に用いる。自覚症状が軽ければ経過観察のみでよい。
治療用ソフトコンタクトレンズ:重症例に使用する。隆起した角膜病変を覆い、瞬目時の眼瞼結膜との摩擦を軽減する。微生物性角膜炎のリスクに注意を要する。
無効な治療:抗菌薬は無効である。イドクスウリジンは前部実質のゴースト混濁や瘢痕を引き起こすため禁忌である。PTKは部分的改善にとどまり再発率が高く推奨されない。
TSPKでは増悪を繰り返すため、ステロイド点眼を長期間使用することがある。その際、眼圧上昇(ステロイド緑内障)と白内障形成に注意が必要である。治療目標は症状をコントロールする最小用量・最低濃度での投与である。0.1%フルオロメトロンから開始し、症状消退後は数ヶ月かけて漸減する。ステロイドの副作用が懸念される場合や忍容性が低い場合には、シクロスポリン点眼やタクロリムスへの切り替えを考慮する。
TSPKの点状混濁はリンパ球を主体とする単核球の上皮内浸潤により形成される。上皮内の抗原(おそらくウイルス抗原)に対する過敏反応と考えられており、低濃度ステロイド点眼によく反応する。
角膜上皮レベルでの細胞内および細胞間浮腫を認める。上皮下神経叢、ボーマン膜、前部実質にも変化が及ぶ。これらの変化はTSPKの持続期間が長い眼ほど重度となる。
小林らは共焦点顕微鏡を用いてTSPK患者に一貫して認められる3つの所見を報告した。第一に、表層および基底上皮細胞層における星芒状の高反射性堆積物の集合体である。第二に、基底上皮層へのランゲルハンス細胞の侵入であり、抗原提示細胞の関与を示唆する。第三に、前部実質の混濁である。これらの変化は上皮内病変の直下だけでなく、病変が存在しない領域にも認められることがあり、疾患の広範な免疫学的影響を示している。
末期には上皮下線維化や前部実質瘢痕が認められることがある。ただし一般的には病変消退後に瘢痕形成はみられず、角膜上皮内に限局した病変であるため視力予後は良好である。
通常、TSPKの各病変は4〜6週間の経過で痕跡を残さず消退する。角膜上皮内に病変が限局しているため、病変消退後の瘢痕形成はみられない。ただし、長期持続例では淡い上皮下混濁や前部実質の瘢痕を生じることがある。共焦点顕微鏡では、罹患期間が長い眼ほど前部実質の変化が顕著であることが報告されている。全体として視力予後は良好である。
Tagmoutiらは、4年間のセリアック病歴を有する20歳女性にTSPKが発症した症例を報告した1)。セリアック病はHLA-DQ2およびHLA-DQ8と強く関連し、90%以上の患者がHLA-DR3アレルを保有する。TSPKにおいてもHLA-DR3との関連が報告されており、両疾患の免疫遺伝学的関連が示唆されている1)。
Tagmoutiらは「TSPKの症例では、共通の遺伝的素因を考慮してセリアック病のスクリーニングを検討すべきである」と述べている1)。
この症例ではシクロスポリンA 2%点眼1日3回の6ヶ月漸減投与により完全寛解が達成され、3年間の追跡で再発を認めなかった1)。免疫調節療法としてのシクロスポリンの有効性が改めて確認されるとともに、TSPKと自己免疫疾患の関連を探る今後の研究の重要性が示されている1)。
本記事は日本の眼科診療ガイドラインおよび標準的な眼疾患教科書に基づいて作成されています。