診断基準
SJS診断基準(厚労省研究班2005):(1) 皮膚粘膜移行部の重篤な粘膜病変、(2) びらんまたは水疱が体表面積の10%未満、(3) 38℃以上の発熱。主要3項目をすべて満たす場合SJSと診断する。
TEN診断基準:体表面積の10%を超える水疱・表皮剥離・びらんを認め、高熱と粘膜疹を伴う。Nikolsky sign陽性で確認する3)。
SJS/TEN全体における重篤な眼合併症(偽膜と角結膜上皮欠損の両方)は約40%に生じる。

Stevens-Johnson症候群(SJS)は、突然の高熱、結膜炎、皮膚の発疹に続いて全身の皮膚・粘膜にびらんと水疱を生じる急性の皮膚粘膜疾患である。中毒性表皮壊死症(toxic epidermal necrolysis; TEN)はSJSの重症型を含んだ病型である。
| 分類 | 皮膚病変の面積 |
|---|---|
| SJS | 体表面積の10%未満 |
| SJS/TEN overlap | 体表面積の10〜30% |
| TEN | 体表面積の30%超 |
SJSとTENの眼所見は類似しており、眼所見のみで両者を鑑別することは困難である。このため眼科ではSJSとTENを包括して広義のSJSと呼ぶことが多い。
発症率はSJSが年間百万人あたり8〜9例、TENが1〜2例と大変まれな疾患であるが、小児を含めあらゆる年齢に性差なく発症する3)。米国では年間百万人あたり12.35例の発症率が報告されている8)。致死率はSJS 4.8%、TEN 14.8%と高い3)。TENでは最大30%に達するとの報告もある1)。
SJS/TENにおける眼合併症の頻度は70%程度とされ、成人では53〜88%に生じる8)。致死率が高いため発症時は全身管理が主体となるが、後遺症として最も多いものが眼障害であり、高度の角膜混濁による視力障害とドライアイが生涯にわたって持続する。
SJSとTENは同一スペクトラムの疾患であり、皮膚病変の面積で分類される。体表面積の10%未満がSJS、10〜30%がSJS/TEN overlap、30%超がTENである。眼所見は両者で類似し鑑別は困難であるため、眼科では合わせて広義のSJSと呼称する。致死率はSJS 4.8%、TEN 14.8%である3)。
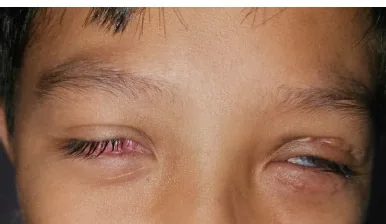
急性期(発症時)
皮疹に気づく前に眼科を受診した場合、ウイルス性結膜炎と誤診されることがある。
慢性期(瘢痕期)
眼合併症の重症度は皮膚病変の範囲と必ずしも相関しない。点眼薬を投与していない眼に対側よりも重篤な障害が生じた症例も報告されており、SJS/TENは根本的に全身性の免疫疾患であることを示している1)。
SJS/TENは薬剤の投与が誘因となって発症することが多い。小児ではマイコプラズマ感染が先行することが多い。発症に先立ち倦怠感や咽頭痛などの感冒様症状を自覚していることが多く、何らかのウイルス感染が契機になると考えられている。
| 原因 | 代表的薬剤・因子 |
|---|---|
| 抗菌薬 | サルファ薬が最多 |
| 抗てんかん薬 | カルバマゼピン、フェニトイン、ラモトリギン |
| NSAIDs | 非ステロイド性抗炎症薬 |
| その他 | アロプリノール |
抗てんかん薬による症例が多数報告されている。カルバマゼピンとフェニトインの併用で35日後に発症した症例3)、ラモトリギンへの切り替え後にTENを発症した症例7)が報告されている。
近年では免疫チェックポイント阻害薬(ICI)によるSJS/TENも報告されている。Tislelizumabの市販後調査では3,795件の有害事象中3例のTENが同定された5)。ICI誘発SJS/TENの発症中央値は32日であり、305例の追跡で69例が死亡したとの報告がある4)。
点眼薬でもSJS/TENを誘発しうる。スルホンアミド系炭酸脱水酵素阻害薬であるブリンゾラミド点眼薬により、全身性のSJS/TEN overlap(体表面積99%)を発症した症例が報告されている1)。
COVID-19ワクチン接種後のSJS/TENも報告されている2)。ワクチン誘発SJS/TENは薬剤誘発性(2〜3週間)より短い1〜8日で発症する傾向がある2)。
HLA遺伝子型がSJS/TEN感受性に強く関連する。アロプリノール投与前にはHLA-B58:01、カルバマゼピン投与前にはHLA-B15:02の検査が推奨されている8)。重篤な眼合併症を伴う日本人SJS/TENではHLA-A*02:06が強い関連を示す。
最も一般的な原因薬剤はサルファ薬(抗菌薬)と抗てんかん薬(カルバマゼピン、フェニトイン、ラモトリギン)であり、NSAIDsとアロプリノールがこれに続く。近年ではICI(免疫チェックポイント阻害薬)による報告も増加している5)6)。点眼薬(ブリンゾラミド)でも全身性SJS/TENを誘発しうる1)。COVID-19ワクチン接種後の発症も報告されている2)。
診断基準
SJS診断基準(厚労省研究班2005):(1) 皮膚粘膜移行部の重篤な粘膜病変、(2) びらんまたは水疱が体表面積の10%未満、(3) 38℃以上の発熱。主要3項目をすべて満たす場合SJSと診断する。
TEN診断基準:体表面積の10%を超える水疱・表皮剥離・びらんを認め、高熱と粘膜疹を伴う。Nikolsky sign陽性で確認する3)。
SJS/TEN全体における重篤な眼合併症(偽膜と角結膜上皮欠損の両方)は約40%に生じる。
眼合併症のグレーディング
Grade 0:眼病変なし。予防的人工涙液を推奨する。
Grade 1:結膜充血のみで角膜病変なし。抗菌薬点眼3回/日、ステロイド点眼6回/日を推奨する8)。
Grade 2:角膜病変あり、偽膜なし。上記に加えProkeraまたはAMTを推奨する8)。
Grade 3:偽膜を伴う角膜病変。AMTを含む積極的治療を推奨する8)。
急性期の治療
全身治療:ステロイドパルス療法(メチルプレドニゾロン500〜1,000mg/日×3日間×1〜2クール)。重症例ではIVIG療法や血漿交換療法を追加する。
眼局所治療:ベタメタゾン点眼または軟膏を1日6〜10回点入し瞼球癒着を防ぐ。感染予防のため抗菌薬の点眼を併用する。
早期羊膜移植(AMT):Grade 2以上で推奨される8)。極めて重症の10例中9例でBCVA 20/20が達成されたとの報告がある8)。感染性角膜炎も35%に生じるため追加の抗菌薬予防が必要である8)。
慢性期の治療
ドライアイ管理:防腐剤なし人工涙液の頻回点眼、ヒアルロン酸点眼、レバミピド(ムコスタ)点眼、涙点プラグを併用する。
睫毛乱生管理:定期的に抜去する。睫毛根切除の眼形成手術も開発されている。
炎症管理:低濃度ステロイド点眼で慢性炎症を抑制し瘢痕性変化の進行を抑制する。MRSA/MRSEの保菌に注意する。
視力回復手術:培養粘膜上皮移植術、輪部支持型ハードコンタクトレンズが視力改善に用いられる。
角膜への結膜組織侵入による高度の視力障害に対しては、培養粘膜上皮移植や輪部幹細胞移植が行われる。角膜瘢痕に対しては全層角膜移植(PKP)が検討されるが、予後は限定的である。ブリンゾラミド誘発SJS/TEN症例では瞼球癒着と角膜瘢痕に対しPKPを施行し、視力0.05に改善した1)。
白内障手術など眼科手術を契機に眼表面炎症が再燃するため、軽症例でも手術後にステロイド内服による十分な消炎が必要である。
急性期の眼表面の十分な消炎が最も重要である。全身的なステロイドパルス療法に加えて眼局所のステロイド点眼薬の頻回投与が必要である。急性期に角膜上皮幹細胞を温存できれば角膜の透明性は維持できる可能性が高い。早期のAMT介入により重症例でも良好な視力予後が期待できる8)。
SJS/TENはIV型(遅延型)過敏反応として分類される。CD8+細胞傷害性Tリンパ球が中心的役割を果たす5)。活性化したCD8+ T細胞はTNF-αとIFN-γを分泌し、ケラチノサイトに一酸化窒素(NO)を産生させる。このNOがFas/Fas ligand経路を介してケラチノサイトの死を促進する5)。
グラニュリシンがSJS/TENにおけるケラチノサイト死の主要メディエーターとして同定されている5)。NK細胞もCD94/NKG2C受容体がケラチノサイト上のHLA-E分子に結合することでケラチノサイト死を媒介する5)。TNF-αは表皮の粘膜類天疱瘡-9発現を上方制御し、最終的に表皮剥離をもたらす5)。
眼では免疫細胞の浸潤前から上皮剥離とヘミデスモソームの喪失が生じうる8)。初期のケラチノサイトには免疫細胞が存在しないにもかかわらず基底部の空胞化が認められ、免疫浸潤前のサイトカイン調節異常が示唆される8)。
後期にはCD8+細胞傷害性Tリンパ球が浸潤しケラチノサイトを標的とする8)。慢性期には結膜組織に好中球が持続的に存在し、免疫調節異常を駆動して輪部幹細胞の障害につながる可能性が示唆されている8)。
角膜上皮幹細胞は輪部上皮の基底細胞に存在し、その割合は1%以下とされる。急性期に広範囲の角結膜上皮欠損により輪部幹細胞が消失すると、角膜表面は結膜組織で被覆され不透明となる。
PD-1阻害薬誘発SJS/TENでは、正常皮膚で通常検出されないPD-L1の発現がリンパ球とケラチノサイトで有意に上方制御される5)。この結果、活性化CD8+ T細胞によるケラチノサイト死が引き起こされる5)。
急性期に角膜上皮幹細胞(輪部上皮の基底細胞に存在)が消失すると、角膜上皮の再生が不可能となる。角膜表面は血管と結合織を伴った結膜組織で被覆され、不透明で凹凸不整となる。慢性期には好中球の持続的存在が免疫調節異常を駆動し幹細胞障害を維持する8)。涙腺導管の閉塞による涙液分泌不全も加わり、障害は生涯持続する。
ICIの使用拡大に伴いSJS/TEN報告が増加している。Tislelizumab誘発SJS/TENの13例(中国)の検討では、9名が男性、平均年齢73.15±7.13歳であった5)。治療レジメンはステロイド単独、ステロイド+IVIG、ステロイド+IVIG+シクロスポリンなど多様であり、12名が改善した5)。
ステロイドとIVIGによる初期治療で改善しなかったtislelizumab誘発SJS/TEN症例に対し、TNF-α阻害薬(組換えヒトTNF受容体II-抗体融合蛋白)と血液浄化を併用し改善が得られた5)。TNF-α阻害薬のSJS/TEN治療への応用は新たな治療戦略として注目されている。
スルホンアミド系点眼薬でも全身性SJS/TENが生じうることが報告された。ブリンゾラミド点眼開始6日後に体表面積99%の全身性反応を発症した1)。結膜・鼻粘膜からの吸収経路が遺伝的に感受性の高い個体では全身性免疫応答を誘発しうる1)。
SJS/TENが劇症1型糖尿病を合併した症例が報告されている3)。全身性の免疫応答が膵β細胞を破壊する機序が推定されている3)。SJS/TEN管理中の血糖モニタリングの重要性が示された。