Salzmann結節状角膜変性(SND)はBowman膜上に青灰色の上皮下結節が形成される非炎症性の角膜 変性である。
有病率は約2420人に1人で、50代と80代に二峰性の発症ピークがある1) 。
女性に多く(72〜88%)、両側性が58〜67%を占める1) 。
慢性瞼縁炎・ドライアイ ・コンタクトレンズ装用などの慢性眼表面疾患に続発するが、特発性のものもある。
無症候性のことも多いが、中心部に及ぶと視力 低下や不正乱視 を生じる。
治療は保存的治療(人工涙液・ステロイド )から外科的治療(表層角膜切除・PTK )まで段階的に行う。
Salzmann結節状角膜変性(Salzmann nodular degeneration; SND)は、Bowman膜上の上皮下領域に青灰色〜灰白色の結節が形成される非炎症性の角膜変性疾患である1) 。1925年にMaximilian Salzmannにより初めて報告された。結節はヒアリン様物質と線維性組織で構成される1) 。
有病率は約2420人に1人と推定される1) 。発症年齢は二峰性で、50代と80代にピークがある1) 。女性に多く、報告により72〜88%を占める1) 。両側性は58〜67%とされる1) 。
結節は中間周辺部の角膜に好発する1) 。多くの場合、慢性眼表面疾患に続発するが、先行する眼疾患を伴わない特発性の症例もある。
Q 片眼だけに起こることもあるか?
A 両側性が58〜67%と過半数を占めるが、片眼性の症例も約3分の1に認められる。片眼性・両側性いずれの場合も臨床的特徴や治療方針に大きな差はない。
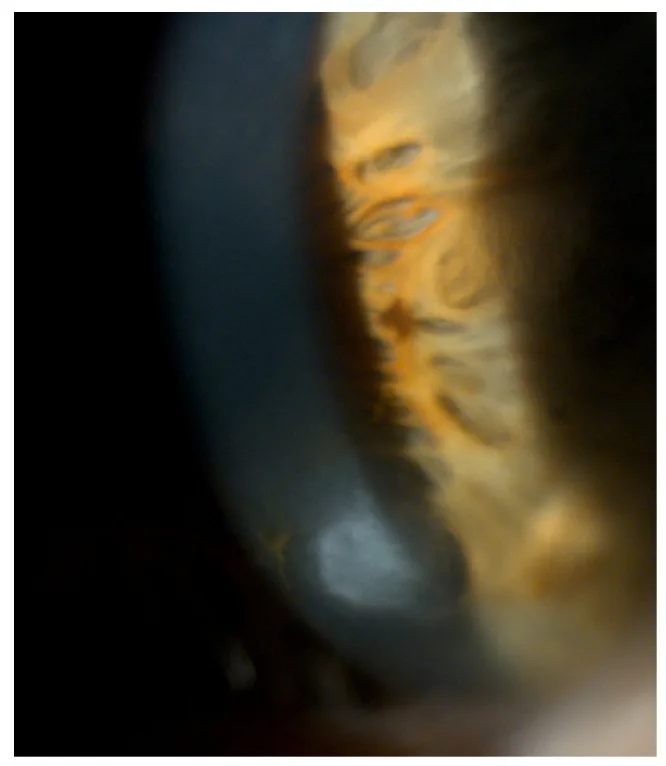
Salzmann結節変性の細隙灯写真 Roszkowska AM, Azzaro C, Calderone A, et al. Salzmann Nodular Degeneration in Ocular and Systemic Diseases. Journal of Clinical Medicine. 2024 Aug 20; 13(4900):$2. Figure 1. PMCID: PMC11355337. License: CC BY.
角膜周辺から前方へ隆起する青白い結節を細隙灯で示している。Salzmann結節の立体感と表層性病変であることが直感的に分かる。
無症候性 :結節が周辺部に限局する場合は自覚症状を欠くことが多い1) 。視力低下 :結節が角膜中心部に及ぶか、表面不整による不正乱視が生じると視力が低下する1) 。異物感 :結節の隆起により異物感を訴えることがある。眩輝(グレア) :角膜表面の不整により光の散乱が生じる場合がある1) 。
上皮下結節 :青灰色〜灰白色の隆起性結節が角膜上皮 下に認められる1) 。直径は通常1〜3mm程度で、単発または多発する3) 。結節の分布 :中間周辺部の角膜に好発し、しばしば輪部 に沿って弧状に配列する1) 。上皮菲薄化 :結節上の角膜上皮は菲薄化している1) 。角膜表面不整 :結節による表面の隆起と周囲の平坦化が角膜形状解析 で捉えられる1) 。
組織学的には、Bowman膜の断裂・消失と、その上に沈着したヒアリン化コラーゲンが特徴的である。結節内部は細胞成分に乏しく、不規則に配列したコラーゲン線維と基底膜様物質で構成される1) 。
SNDは多くの場合、慢性眼表面疾患に続発する。主なリスク要因を以下に示す1) 。
慢性瞼縁炎・マイボーム腺機能不全 (MGD) :最も高頻度に関連する眼表面疾患である1) 。ドライアイ :慢性的な眼表面の炎症がBowman膜の変性を促進する1) 。コンタクトレンズ装用 :長期装用による慢性的な機械的刺激が関連する1) 。フリクテン性角結膜炎 1) 2) 。翼状片 2) 。角膜手術後 :LASIK 後やPRK後の発症が報告されている1) 。外傷 :鈍的外傷後の発症例がある2) 。
結合組織疾患
Ehlers-Danlos症候群 :結合組織の脆弱性を共有する可能性が指摘されている1) 。
Dermatopathia pigmentosa reticularis :皮膚色素異常を伴う遺伝性疾患との合併が報告されている1) 。
炎症性・遺伝性疾患
Crohn病 :消化管の慢性炎症性疾患との合併報告がある1) 。
Kabuki症候群 :先天性の多発奇形症候群との関連が報告されている1) 。
Kartagener症候群 :繊毛運動障害を伴う症候群との合併例がある1) 。
甲状腺眼症 1) 。
遺伝的要因として、一部の家族性症例で常染色体優性遺伝 パターンが報告されている1) 。また、角膜ジストロフィ に関連するTGFBI遺伝子の変異が検出された報告がある1) 。
Q コンタクトレンズ装用は関連するか?
A コンタクトレンズの長期装用は慢性的な機械的刺激と眼表面の炎症を引き起こし、SNDのリスク要因の一つとされている。装用者は定期的な眼科検診が推奨される。
SNDの診断は主に細隙灯顕微鏡所見に基づく。画像検査は病変の範囲と深達度の評価に有用である1) 。
検査法 所見 特徴 細隙灯顕微鏡 上皮下青灰色結節 確定診断の基本 角膜形状解析 表面不整・不正乱視 Placidoリング異常1) 前眼部OCT 上皮下高反射沈着物 深達度評価に有用1)
細隙灯顕微鏡検査 :青灰色〜灰白色の上皮下結節を直接観察する。結節の数・大きさ・分布・角膜中心部への波及を評価する1) 。角膜形状解析(トポグラフィ) :Placidoディスクベースの角膜形状解析で、結節による表面不整と不正乱視を定量的に評価する1) 。結節上では角膜が平坦化し、結節間では急峻化するパターンを示す。前眼部OCT(AS-OCT) :上皮下の高反射性沈着物として結節を描出する1) 3) 。Bowman膜との関係や深達度を非侵襲的に評価できる。生体共焦点顕微鏡 (IVCM) :結節内部の微細構造を細胞レベルで観察できる1) 。不規則な線維性構造と角膜実質 細胞の消失が特徴的である。
SNDと鑑別すべき角膜病変を以下に示す2) 。
PHSCD(pericentral hypertrophic subepithelial corneal degeneration) :上皮下結節を生じるが、より周辺部に位置し形態が異なる。帯状角膜変性 球状角膜 変性(spheroidal degeneration)角膜上皮内腫瘍(OSSN ) :角膜表面の上皮性腫瘤であり、臨床的に鑑別を要する場合がある。
無症候性または軽症例では保存的治療が第一選択となる1) 。
人工涙液 :眼表面の潤滑により症状の緩和と進行抑制を図る。眼瞼衛生 :背景にある瞼縁炎・MGDの管理が重要である1) 。ステロイド点眼 :眼表面の炎症制御に用いる。シクロスポリン 点眼1) 。
視力障害を伴う症例やコンタクトレンズ装用が困難な症例では外科的介入が検討される1) 4) 。
結節切除・表層角膜切除
方法 :結節を鑷子で把持し、Bowman膜レベルで鈍的に剥離・除去する1) 。
成功率 :約90%の症例で視力改善が得られる。
羊膜移植 1) 。
PTK(治療的エキシマレーザー角膜切除)
方法 :エキシマレーザーで結節を含む表層組織を切除する1) 4) 。
利点 :均一で平滑な角膜表面が得られる。
MMC併用 :マイトマイシンC(MMC)を併用し、術後の角膜混濁(haze)を抑制する場合がある1) 。
上皮下線維症に対する層別外科的アプローチとして、SNDにはepithelial debridement(ED)、表層角膜切除(SK)、PTKが推奨されている4) 。
進行例でまれに層状角膜移植 (DALK )や全層角膜移植 (PKP)が必要となることがある1) 。角膜輪部幹細胞疲弊を伴う高度例では輪部幹細胞 移植が考慮される場合もある。
再発は外科的治療後の課題であり、61ヵ月の経過観察で約22%に再発が報告されている。背景にある眼表面疾患の管理が再発予防に重要である1) 。
Q 手術後に再発するか?
A 再発は外科的治療後の重要な課題であり、約22%に再発が報告されている。背景にある瞼縁炎やドライアイなどの眼表面疾患を適切に管理することが再発予防に重要である。
SNDの病態は、Bowman膜と上皮基底膜の破綻に始まる一連の線維化プロセスとして理解される1) 。
Bowman膜の破綻 :慢性炎症や機械的刺激によりBowman膜と上皮基底膜に断裂が生じる1) 。角膜実質細胞の遊走 :破綻部位を通じて角膜実質の角膜細胞(keratocyte)が上皮下領域へ遊走する1) 。筋線維芽細胞への分化 :遊走した角膜細胞は筋線維芽細胞に分化する1) 。線維性細胞外マトリックス(ECM)の沈着 :筋線維芽細胞がヒアリン化コラーゲンを主体とする線維性ECMを産生・沈着させ、結節が形成される1) 。
SNDの病態形成にはマトリックスメタロプロテアーゼ-2(MMP-2)、血小板由来成長因子(PDGF)、トランスフォーミング成長因子β1(TGF-β1)が関与している1) 。
粘膜類天疱瘡-2 :Bowman膜と基底膜の分解に関与する1) 。PDGF :角膜細胞の遊走と増殖を促進する1) 。TGF-β1 :角膜細胞から筋線維芽細胞への分化を誘導し、ECM産生を亢進させる1) 。
結節上の角膜上皮ではCK19陽性のtransit amplifying cell(一過性増幅細胞)が認められ、上皮の分化異常が示唆されている1) 。
一部の家族性SND症例で常染色体優性遺伝パターンが報告されている1) 。角膜ジストロフィの原因遺伝子として知られるTGFBI遺伝子の変異がSND患者で検出されており、遺伝的素因の関与が示唆されている1) 。今後、ゲノム解析の進展により、SNDの遺伝的基盤がさらに明らかになることが期待される。
近年、Ehlers-Danlos症候群、Crohn病、Kabuki症候群、Kartagener症候群、甲状腺眼症など多様な全身疾患との合併が報告されている1) 。これらの関連性は、共通する炎症経路や結合組織の脆弱性など、SNDの病態に新たな視点を提供している。
円錐角膜 とSNDの合併が報告されている3) 。両疾患は眼表面の炎症や機械的刺激といった共通のリスク要因を持つ可能性がある3) 。この合併症例の蓄積により、角膜変性と角膜拡張症 の関連性の理解が深まることが期待される。
Q 遺伝的な要因はあるか?
A 一部の家族で常染色体優性遺伝パターンが報告されており、角膜ジストロフィに関連するTGFBI遺伝子の変異がSND患者で検出されている。ただし、大部分のSNDは慢性眼表面疾患に続発する後天性の変性であり、遺伝が主因となる症例はまれである。
Roszkowska AM, Azzaro C, Calderone A, et al. Salzmann Nodular Degeneration in Ocular and Systemic Diseases. J Clin Med. 2024;13:4900.
Kuan HC, Ling JL, Chua KH, et al. Corneal Nodules and Possible Pathologies: A Case Series. Cureus. 2021;13:e20822.
Das D, Lomi N, Sasi A, et al. Layers of Rarity: An Unusual Concurrence of Keratoconus, Salzmann’s Nodular Degeneration, Ptosis, and Congenital Retinal Macrovessel. Cureus. 2025;17:e92115.
American Academy of Ophthalmology. Corneal Edema and Opacification Preferred Practice Pattern. Ophthalmology. 2024.
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト) してください