角膜所見
角膜実質浮腫:角膜のすりガラス状混濁を呈する。角膜厚が著しく増大する
Descemet膜皺襞:内皮機能不全に伴い角膜後面に皺襞が形成される
上皮下水疱(bullae):進行例ではgiant bullaeの形成もみられ、破裂により上皮欠損を生じる
実質瘢痕・血管侵入:慢性化すると角膜周辺部から血管侵入と瘢痕性混濁が生じる

偽水晶体眼性水疱性角膜症(pseudophakic bullous keratopathy: PBK)は、白内障手術および眼内レンズ(IOL)挿入後に発生する不可逆的な角膜浮腫である1)。角膜内皮細胞の障害により内皮ポンプ機能が破綻し、角膜実質・上皮の浮腫と上皮下水疱形成を特徴とする。
白内障手術を受ける患者の1〜2%に発症するとされ、術後8か月から7年の間に顕在化する1)。PBKはFuchs角膜内皮ジストロフィに次いで角膜移植の主要適応疾患であるが、白内障手術技術の進歩に伴い発症率は減少傾向にある6)。
本邦の調査では、水疱性角膜症963眼のうち428眼(約45%)が白内障手術後の偽水晶体性/無水晶体性水疱性角膜症であり、角膜移植の主因であった。超音波乳化吸引術(PEA)の普及以前の術式の術後例も多く含まれている。
いいえ、白内障手術後に水疱性角膜症になる確率は1〜2%程度です。現代の手術技術は角膜内皮への侵襲が少なく、大半の方は問題なく経過します。ただし、術前から角膜内皮細胞密度が低い方や、手術が難航した場合にはリスクが高くなります。術前検査で内皮細胞の状態を把握し、リスクに応じた手術計画を立てることが重要です。
初期には朝方の霧視が特徴的である。就寝時の閉瞼により角膜浮腫が増悪し、起床直後に最も視力が低下する。開瞼後は角膜の乾燥と酸素供給の回復により浮腫が軽減し、日中は症状が改善する。
進行すると角膜浮腫は不可逆性となり、持続的な視力低下を呈する。上皮下水疱の破裂により急性の眼痛が生じる。羞明や流涙、異物感も伴う。
角膜所見
角膜実質浮腫:角膜のすりガラス状混濁を呈する。角膜厚が著しく増大する
Descemet膜皺襞:内皮機能不全に伴い角膜後面に皺襞が形成される
上皮下水疱(bullae):進行例ではgiant bullaeの形成もみられ、破裂により上皮欠損を生じる
実質瘢痕・血管侵入:慢性化すると角膜周辺部から血管侵入と瘢痕性混濁が生じる
前眼部所見
スペキュラーマイクロスコピーでは内皮細胞密度の著明な低下がみられるが、進行例では角膜浮腫のため撮影不能となることがある2)。
角膜内皮細胞は生体内で分裂・増殖しない。局所的な障害は隣接細胞の拡大と移動により修復されるが、一定密度以下に減少すると不可逆的なポンプ機能不全に陥る。PBKはこの内皮代償不全が白内障手術後に生じた状態である1)。
| 時期 | リスク因子 |
|---|---|
| 術前 | 低内皮細胞密度・高齢・Fuchs角膜内皮ジストロフィ・浅前房 |
| 術中 | 超音波過多・器具接触・後嚢破損・硝子体脱出8) |
| 術後 | 炎症遷延・IOL偏位・核残存・緑内障 |
前房型IOL(ACIOL)は14%でPBKを合併するとの報告があり、後房型IOLより高リスクである3)。合併症のない白内障手術後にも原因不明でPBKを発症する症例がある1)。
中毒性前眼部症候群(TASS)による化学的内皮障害もPBKの原因となる。術中の灌流液毒性や前房内薬物誤注入なども報告されている。
術前の中心角膜厚が600μm近くに増大している場合は、すでに角膜浮腫が始まっている可能性があり、手術により水疱性角膜症に至るリスクが高い。
はい、スペキュラーマイクロスコピーで角膜内皮細胞密度を測定することで、ある程度リスクを評価できます。ただし、内皮細胞密度だけでは発症を正確に予測できません。中心角膜厚(パキメトリー)の測定も併用することが推奨されており、角膜厚が600μm以上の場合はすでに内皮機能が低下している可能性があります。術前に主治医とリスクについて相談してください。
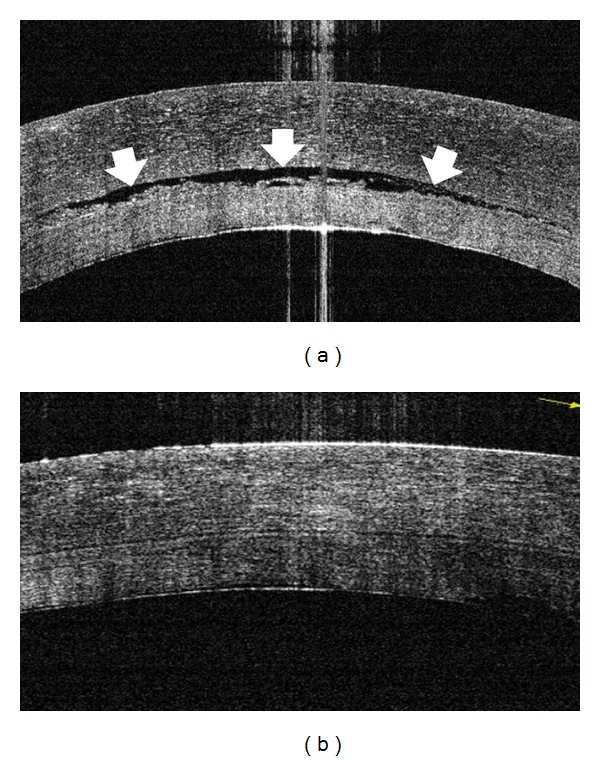
PBKの診断は臨床所見に基づく。白内障手術の既往と進行性の角膜浮腫が診断の基本となる。
細隙灯顕微鏡検査:角膜実質浮腫、Descemet膜皺襞、上皮微小嚢胞、上皮下水疱を観察する。IOLの位置と種類も確認する。
スペキュラーマイクロスコピー:内皮細胞密度の低下、多形性(polymegethism)、不同性(pleomorphism)を評価する。進行例では撮影困難なことがある2)。
角膜厚測定(パキメトリー):角膜浮腫の程度を定量的に評価する。中心角膜厚 640μm以上は白内障手術後の不可逆的浮腫のリスクが高い1)。
前眼部光干渉断層計(OCT):角膜各層の状態を高解像度で可視化でき、上皮下水疱の範囲、実質肥厚の程度、Descemet膜の異常を詳細に評価できる7)。
Fuchs角膜内皮ジストロフィ(滴状角膜の有無で鑑別)、後部多形性角膜ジストロフィ(PPMD)、虹彩角膜内皮症候群(ICE)、ヘルペス性角膜内皮炎(角膜後面沈着物のパターンで鑑別)などが挙げられる。対側眼の内皮検査が鑑別に重要である。
初期のPBKでは保存的治療が第一選択となる。
高張食塩水:5%塩化ナトリウム点眼液および6%塩化ナトリウム眼軟膏が用いられる。涙液層を高張にして角膜から水分を引き出す7)。効果は限定的であり、一時的な対症療法にとどまる。
治療用コンタクトレンズ:上皮下水疱の破裂に伴う疼痛緩和のために用いられる。
角膜移植は内皮細胞の構造と機能を回復させる根治的治療である7)。
角膜内皮移植術
角膜内皮移植術(DSAEK):ドナー角膜の内皮細胞層と約50〜100μmの後部実質を移植する。無縫合で惹起乱視が少なく、外傷にも強い7)
デスメ膜内皮角膜移植術(DMEK):Descemet膜と内皮細胞層のみを移植する。角膜内皮移植術より視力回復が早く良好で、拒絶反応もほとんど生じない7)
適応:偽水晶体眼であることが原則。無虹彩や広範な虹彩前癒着眼では適応に制限がある
全層角膜移植術(PK)
適応:実質瘢痕や血管侵入が高度な進行例で選択される7)
特徴:術後の拒絶反応リスクが内皮移植より高く、ステロイド点眼の長期使用が必要となる
注意点:術後の角膜強度が低下し、鈍的外傷で創離開を起こしやすい
| PK | DSAEK | DMEK | |
|---|---|---|---|
| 移植片脱落率 | 0% | 14.5〜15% | 5.9〜27.4%7) |
| 5年拒絶反応率 | 22.2% | 22.0% | 2.8%7) |
| 5年グラフト不全率 | PBK 27% | PBK 24% | 0〜12.5%7) |
小角膜やACIOL残存例などの複雑眼でもDSEKは実施可能であり、IOL交換なしで良好な視力回復が得られた報告がある3)。
術後6か月経過しても浮腫が改善しない場合は内皮代償不全と判断し、角膜内皮移植の適応となる。
角膜移植を待つ間の疼痛緩和として、角膜コラーゲンクロスリンキング(CXL)、羊膜移植、前実質穿刺(ASP)、治療的レーザー角膜切除術(PTK)などが選択肢となる。
軽症〜中等症のPBKでは、ROCK阻害薬(リパスジル)の点眼により角膜浮腫が改善し、手術を遅延または回避できた症例が報告されています。ただし、内皮細胞が高度に減少した進行例では効果が限定的です。現時点ではROCK阻害薬は標準治療としてまだ確立されておらず、角膜移植が根治的治療の柱です。主治医と相談のうえ、個々の病状に適した治療法を選択してください。
角膜内皮細胞は、Na⁺/K⁺-ATPaseポンプを介して角膜実質から房水側へ液体を能動的に汲み出す。このポンプ機能により角膜実質の含水量が一定に保たれ、角膜の透明性が維持される。角膜内皮細胞密度がおおよそ500〜800 cells/mm²以下に低下すると、ポンプ機能が代償できなくなり角膜浮腫が生じる1)。
白内障手術後の角膜内皮細胞減少は複数の機序で生じる。
機械的損傷:術中の器具やIOLの接触、超音波エネルギーによる直接的な内皮障害が主因である8)。高吸引流量、高い超音波パワー、長い手術時間はいずれもリスク因子とされる。
炎症性損傷:術中の虹彩損傷は前房内の炎症性サイトカイン濃度を上昇させ、長期にわたる角膜内皮細胞減少を加速させる。
術後の慢性減少:正常成人の角膜内皮細胞は年間0.6%の自然減少を示すが、白内障手術後は年間2.5%と約4倍の減少率となる。術後5年以内では術前比11.0%、10年以上では18.7%の減少が報告されている。
IOLの存在下に角膜浮腫が生じた場合、たとえ角膜内皮のguttaeが存在してもPBKと定義される6)。Fuchs角膜内皮ジストロフィとは異なり、PBKでは角膜浮腫が周辺部から始まり中心に進行する傾向がある6)。
初期は実質浮腫のみであるが、内皮障害が高度になると上皮浮腫も加わり、上皮下水疱が形成される。水疱の破裂は急性の疼痛と上皮欠損を生じ、二次感染のリスクとなる。最終的に角膜周辺部からの血管侵入と実質の瘢痕性混濁へと進行する。
Rho関連コイルドコイル形成キナーゼ(ROCK)阻害薬は、角膜内皮細胞の増殖・遊走・接着を促進し、アポトーシスを抑制する薬剤である。PBKに対する3つの応用が研究されている1)。
(1)局所点眼療法
Erdinestらは、通常の保存的治療に反応しなかったPBK 3症例にリパスジル0.4%点眼(1日3回)を3〜11か月間投与した。全例で中心角膜厚の減少と矯正視力の改善が得られ、角膜移植を回避できた2)。症例3では11か月の投与で実質混濁が完全に消失し、中心角膜厚が582μmから540μmに、視力が0.3 logMARから0.04 logMARに改善した2)。
(2)周術期予防投与
リパスジルの周術期投与が白内障手術後の内皮細胞減少を軽減する可能性が報告されている。術後12か月の内皮細胞減少率はリパスジル群4.5%に対しコントロール群12.8%であった1)。高リスク眼における予防的使用が期待される。
(3)培養内皮細胞注入療法
Kinoshitaらは培養ヒト角膜内皮細胞をROCK阻害薬Y-27632とともに前房内に注入する画期的な治療法を開発した。水疱性角膜症11眼のうち10眼で5年後も角膜透明性が維持され、平均内皮細胞密度は1257 cells/mm²であった1)。
この治療法は日本で第II/III相臨床試験を経て2022年に製造販売承認を取得し、ネナデンドセルとして商品化された1)。角膜移植に依存しない再生医療として国際的な注目を集めている。
EndoArtは角膜後面の湾曲に合致する薄い人工バリアデバイスであり、病的な内皮に代わって角膜への水分流入を制限する。複雑眼(無虹彩・硝子体手術後・チューブ挿入眼)における難治性PBKに対し、pull-through挿入法により留置に成功し、中心角膜厚が911μmから691μmに改善した報告がある4)。ドナー角膜不足を補う選択肢として開発が進められている。
はい、2022年に日本で世界初の培養角膜内皮細胞注入療法(ネナデンドセル)が製造販売承認を取得しました。ただし、実施可能な施設は限られており、対象となる病態や適応基準があります。すべてのPBK患者に適応されるわけではなく、主治医と相談のうえ治療の可否を判断する必要があります。