ゼラチン状
半透明の隆起性腫瘤:最も一般的な形態。結膜血管がヘアピン状の走行を示す。
栄養血管:異常に拡張・蛇行した栄養動脈が悪性増殖を示唆する1)。

1995年にLeeらが提唱した用語であり、角膜・結膜・輪部に生じる非複合型の扁平上皮性腫瘍を包括する1)。眼表面の非色素性腫瘍として最も頻度が高く、単一施設の研究では771例の非メラノサイト性結膜腫瘍のうち23%(179例)をOSSNが占めた1)。
OSSNは以下の病変を含む。
発生率は地理的差異が大きい。高緯度地域では0.02/10万であるのに対し、赤道近くの低緯度地域では3.5/10万に達する1)。全世界の年齢標準化発生率は0.26/10万/年であり、増加傾向にある1)。アフリカが最も高率(3.4/10万/年)で、HIV・HPV感染の高頻度が寄与する1)。
西半球では60歳以上の白人男性に好発するが、アフリカやアジアの一部ではHIV感染を背景に若年者にも発症し、より侵襲的な経過をとる1)。
AJCC第8版では、原発腫瘍(T)、所属リンパ節(N)、遠隔転移(M)に基づきOSSNを分類する1)。
| 分類 | 定義 |
|---|---|
| Tis | 上皮内癌(上皮内に限局) |
| T1 | 結膜に限局、隣接構造への浸潤なし |
| T2 | 隣接眼構造(角膜・円蓋・涙丘・強膜・眼球)に浸潤 |
| T3 | 眼窩・副鼻腔・眼瞼に浸潤 |
| T4 | 中枢神経系・遠隔部位への浸潤 |
未治療のSCCは眼窩浸潤(約10%)、所属リンパ節転移、稀に遠隔転移を生じ、死亡率は8〜24%と報告される1)。
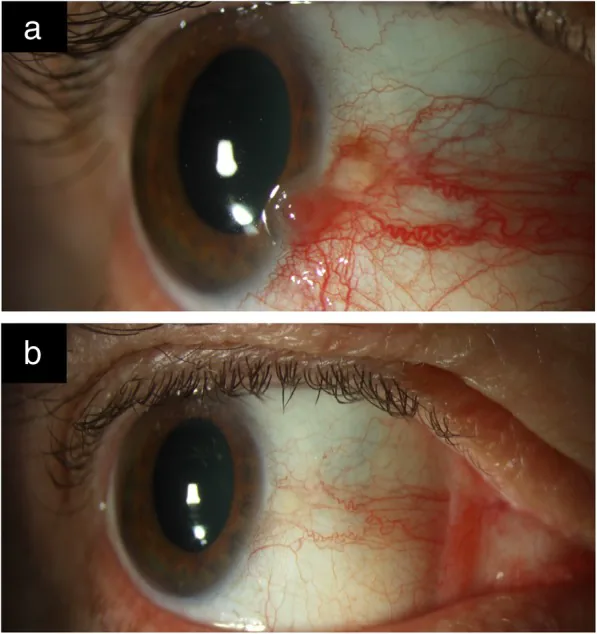
OSSN病変は無症状で偶然発見されることが多い。症状がある場合は、充血・異物感・眼刺激症状が主体である2)。痛みを伴うこともある。視力低下は腫瘍が角膜に波及した場合や眼内浸潤例でみられる。
片側性の血管を伴う腫瘤が最も一般的であり、瞼裂間(鼻側または耳側)の輪部近傍に好発する1)。角膜および球結膜に多く、眼瞼結膜の発症は稀である1)。白人では黄ピンク色、有色人種では色素沈着を伴うことがある1)3)。
ゼラチン状
半透明の隆起性腫瘤:最も一般的な形態。結膜血管がヘアピン状の走行を示す。
栄養血管:異常に拡張・蛇行した栄養動脈が悪性増殖を示唆する1)。
白板状
表面の白色化・肥厚:過角化による腫瘍表面の角化。
乾燥した外観:ゼラチン状とは対照的に不透明な白色調を呈する。
乳頭状
乳頭状増殖:HPV関連の形態として知られる4)。
結節状の表面:いぼ状の外観を呈することがある。
結節潰瘍型
稀だが侵襲的:浸潤性新生物を強く示唆する形態1)。
潰瘍形成:他の形態より予後不良。
角膜への波及では、半透明で灰色がかったすりガラス状の外観を呈し、房状(fimbriated)または偽足状の進展形態をとる。
眼内浸潤は稀であるが、前房内の白色腫瘤・前房炎症・続発緑内障として現れることがある2)。
ある。特にHIV陽性の有色人種では、CINが色素性病変を模倣することが報告されている3)。典型的なOSSN所見が乏しい場合でも、HIV陽性者の結膜色素性病変はOSSNを鑑別に含める必要がある。
OSSNの病因は多因子性である。主要なリスク因子を以下に挙げる1)。
HIV感染による免疫抑制が腫瘍免疫監視機構を低下させるためである。HIV陽性者ではOSSNリスクが10〜13倍に増加し3)、若年でも発症する。アフリカではHIV・HPVの重複感染が疾患増加の一因とされる1)。
OSSNの確定診断は切除生検または切開生検による組織学的検査である(ゴールドスタンダード)1)。4時間未満の小さな腫瘍は切除生検、4時間以上の大きな腫瘍は切開生検が適応となる。
診断補助にローズベンガル、リサミングリーン、メチレンブルー、トルイジンブルーなどの特殊染色が用いられる1)。ローズベンガルはアポトーシスや代謝不活性な上皮細胞を鮮明なピンク色に染色し、腫瘍の輪郭を明瞭化する1)。
主な診断モダリティを以下にまとめる。
| 検査法 | 特徴 |
|---|---|
| 生検(組織検査) | ゴールドスタンダード。浸潤深度も評価可能 |
| HR-OCT | 非侵襲的。上皮肥厚・高反射が特徴 |
| IVCM | 細胞レベルの評価。操作が煩雑 |
| 印象細胞診 | 非侵襲的だが表面組織のみ評価 |
OSSNは翼状片・瞼裂斑との鑑別が特に重要である1)。併存することもあり診断が困難となる場合がある。そのほか、角膜パンヌス、日光角化症、化膿性肉芽腫、結膜母斑、悪性黒色腫などが鑑別に挙がる。
臨床所見のみでは鑑別が困難な場合がある。HR-OCTでの上皮肥厚・高反射所見、ローズベンガルやメチレンブルーによる特殊染色が鑑別の手がかりとなる1)。確定診断には生検が必要である。
OSSNの治療は腫瘍のサイズ・浸潤度・患者因子に基づいて個別化する1)。外科的切除と局所化学療法の有効性は同等と報告されている1)。
ノータッチ・テクニック+凍結療法がゴールドスタンダードである1)。
切除断端陽性の場合は術後補助化学療法が推奨される1)2)。凍結療法なし・術後化学療法なしの条件下では眼内浸潤のリスクが高まる2)。
Pikeら(2023)は、切除後に凍結療法・化学療法を行わなかったOSSN症例で、全層輪部欠損を介した眼内播種(前房内腫瘤形成)が生じ、眼球摘出に至った例を報告した2)。ノータッチ・テクニックと凍結療法、および術後化学療法の重要性を強調している。
局所化学療法は単独療法としても術後補助療法としても使用される1)。
マイトマイシンC
マイトマイシンC:0.02〜0.04%点眼。DNA架橋により腫瘍細胞を死滅させる。
有効率:80〜100%。消失までの時間がIFNより短い傾向がある1)。
副作用:眼痛、輪部幹細胞消失、涙点狭窄のリスク。
5-FU
5-フルオロウラシル:S期のDNA・RNA合成を阻害するピリミジンアナログ1)。
有効率:高い。再発率は最大20%。マイトマイシンCやIFNより安価である。
投与法:1%点眼を1週間投与・3週間休薬のサイクルで使用。
IFNα-2b
インターフェロンα-2b:抗増殖・抗ウイルス・免疫調節作用を持つ1)。
有効率:80〜100%。結膜下注射(100万IU/mL)または点眼で投与。
特徴:副作用が少ないが高価で冷所保存が必要。
その他の薬物療法として、抗VEGF薬(ベバシズマブ・ラニビズマブ)は結膜病変に有望な結果を示すが角膜病変への効果は不明確であり、大規模試験が必要である1)。HPV関連患者にはシドフォビルが使用されることがある1)。
AJCC第8版に基づく治療アプローチを以下に示す1)。
再発には以下の因子が関与する1)。
化学療法単独(MMC・5-FU・IFNα-2b)の有効性は手術と同等であることが報告されている1)。腫瘍のサイズや浸潤度、患者の全身状態・アドヒアランスに応じて選択する。4時間以上の大きな病変や多発・再発例では局所化学療法が有利な場合がある。
OSSNは輪部幹細胞から発生すると考えられている1)。大部分の原発性結膜悪性腫瘍は、幹細胞分裂が活発な瞼裂間の輪部近傍に出現する1)。
組織学的に、浸潤性SCCでは悪性扁平上皮細胞が基底膜を貫通し間質内に増殖する1)。CIN I〜IIIは上皮内における異形成の範囲で分類される。上皮全層に及ぶ異形成(CIN III)は上皮内癌と同義である1)。
眼内浸潤は稀であるが以下の経路で生じる2)。
Pikeら(2023)の症例では、切除生検後に全層輪部欠損が形成され、そこを経路として腫瘍細胞が前房内に播種し、角膜後面・隅角・虹彩・毛様体・水晶体にまで拡散した2)。病理学的には上皮内増殖(epithelial downgrowth)の悪性型に類似した所見であった。
粘表皮癌ではムチン染色で異形成扁平上皮細胞と悪性杯細胞が確認される。ムチン成分が優位な場合は臨床的侵襲性が比較的低いとされる。
放射線療法はOSSNおよびSCCの治療選択肢として検討されている1)。
バーテポルフィンとレーザーを組み合わせた治療法である1)。パイロット研究では結膜SCCの100%で腫瘍消失が得られ、観察期間中の再発はなかった1)。しかし高コスト・施設の限定・専門的訓練の必要性が普及の障壁となっている。
Zeinら(2024)は、2度の切除後に再発した乳頭状OSSN(HPV陽性・p16陽性)に対し、9価HPVワクチン(Gardasil-9)の筋注を6週間間隔で4回投与した4)。3回目投与後に劇的な腫瘍縮小がみられ、HR-OCTでも上皮肥厚・高反射の改善が確認された。ただし根治には至らず、追加の5-FU・マイトマイシンC点眼が施行された。
HPVワクチンのOSSN治療への応用は世界初の報告であり4)、今後の治療選択肢として研究が進められている。ワクチンの治療機序としては、HPV特異的E6/E7癌蛋白の抑制が推測されている4)。