炎症性病変
前部ぶどう膜炎:最も多い眼合併症の一つ。毛様充血・前房内炎症細胞を呈する
後部ぶどう膜炎:硝子体混濁や網膜血管炎を伴うことがある
強膜炎・上強膜炎:強膜の炎症性充血。上強膜炎が最も強い関連を示すとの報告もある
実質性角膜炎:角膜実質の炎症。重症例では視力低下に至る

化膿性汗腺炎(hidradenitis suppurativa: HS)は、アポクリン汗腺が存在する部位に好発する慢性炎症性皮膚疾患である。痛みを伴う結節・膿瘍・瘻孔を特徴とし、腋窩・鼠径部・臀部・乳房下などに生じる。世界的な推定有病率は0.00033〜4.1%であり、欧州および米国では0.7〜1.2%と報告されている。
HSは皮膚疾患であるが、全身性の炎症が眼にも波及しうる。約13.89%のHS患者に何らかの眼科的所見が認められるとされる。最も一般的な眼合併症はぶどう膜炎であり、強膜炎・角膜炎がこれに続く。別の研究では上強膜炎が最も強い関連を示したとの報告もある。
HSの病態には毛包脂腺系単位の閉塞が中心的に関与する2)。その後の毛包破裂と免疫反応が炎症カスケードを惹起し、TNF・IL-1・IL-17・IL-23などの炎症性サイトカインが全身性に上昇する2)。これらのサイトカインはぶどう膜炎やドライアイの病態にも深く関与しており1)、HSにおける眼合併症の発症機序を説明する一因と考えられている。
HSは乾癬・クローン病・潰瘍性大腸炎などの脊椎関節炎関連免疫疾患や、ベーチェット症候群・全身性エリテマトーデスなどの血管炎と免疫学的メカニズムを一部共有する。これらの疾患でも眼合併症は周知されており、HSにおいても同様のリスクが存在する。
化膿性汗腺炎(HS)は全身性の炎症を伴うため、眼科的な合併症が生じる可能性があります。症状がなくても、定期的な眼科スクリーニングが推奨されています。特に充血・痛み・かすみ目・光過敏(羞明)などの症状が出現した場合は、速やかに眼科を受診してください。皮膚科医と眼科医の連携が重要です。
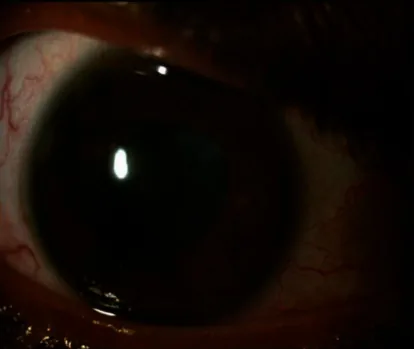
HSに伴う眼症状として以下が報告されている。
症状の強さは環境要因・ストレス・併存疾患によるフレア(再燃)に基づき変動する。
炎症性病変
前部ぶどう膜炎:最も多い眼合併症の一つ。毛様充血・前房内炎症細胞を呈する
後部ぶどう膜炎:硝子体混濁や網膜血管炎を伴うことがある
強膜炎・上強膜炎:強膜の炎症性充血。上強膜炎が最も強い関連を示すとの報告もある
実質性角膜炎:角膜実質の炎症。重症例では視力低下に至る
眼表面・網膜所見
眼瞼角結膜炎:両側性の角膜新生血管形成と下方角膜菲薄化を呈する症例が報告されている
マイボーム腺機能不全:腺機能不全によるドライアイを生じうる
網膜血管変化:OCTA上、中心窩VD・VLD低下および網膜深層毛細血管叢のVD低下が報告されている
眼窩周囲病変:まれだが、顔面・眼瞼にHS病変が出現することがある
OCTAを用いた研究では、臨床的な眼疾患がないHS患者においても網膜微小血管の異常が検出されている。これは糖尿病網膜症で見られる所見と類似しており、HSと2型糖尿病の併存リスクを反映するものと考えられている。
約13.89%のHS患者に眼科的所見が認められるとの報告があります。ぶどう膜炎が最も多く、次いで強膜炎・上強膜炎・角膜炎の順です。ただし、これらの眼合併症を調べた研究には他の自己免疫疾患を持つ患者も含まれていたため、HS単独での正確な頻度はまだ確立されていません。
HSの病態における主要な欠陥は、毛包脂腺系単位の毛包閉塞である2)。組織学的には早期に漏斗部棘細胞症・角化亢進・毛包周囲の免疫細胞浸潤が検出される2)。毛包の破裂に続く免疫反応が炎症カスケードを惹起し、結節・膿瘍・瘻孔の形成に至る。
FitzsimmonsとGilbertの研究では23家族中14家族でHSの集積が観察され、患者の30%に強い家族歴が認められた。Notchシグナル経路の異常が関与しており、PSENEN・KRT5・POFUT1・POGLUT1遺伝子の変異が報告されている3)。Notch経路はメラノサイトの恒常性や毛包の分化制御にも関わるため、その異常は皮膚のみならず多臓器に影響を及ぼす可能性がある3)。
皮膚および血清レベルでTNF・IL-1・IL-17・IL-23が上昇する2)。これらのサイトカインのうち、TNF-αとIL-6はぶどう膜炎の病態にも深く関与し、ドライアイの眼痛とも相関する1)。上皮細胞からはTNF-α・IL-1・IL-6・IL-8が放出され、免疫応答を増幅して炎症細胞を誘引する1)。
| リスク要因 | 影響 |
|---|---|
| 喫煙 | 表皮過形成と毛包閉塞を促進 |
| 肥満 | 重症化と関連 |
| 薬剤(リチウム等) | HS誘発の報告あり |
リチウムは毛包角化細胞に直接作用し、好中球遊走・貪食促進を介してHSを誘発しうる4)。リチウム中止により皮膚症状は改善する4)。
HSは臨床診断が基本であり、以下の3基準に基づく2)。
Hurley分類により重症度を3段階に分類する2)。
| Hurley分類 | 特徴 |
|---|---|
| Stage I | 孤立性膿瘍。瘻管・瘢痕なし |
| Stage II | 再発性膿瘍。瘻管形成あり |
| Stage III | 広範囲の連結性瘻管・膿瘍 |
大多数はStage I(68%)またはStage II(28%)であり、Stage IIIは4%にとどまる2)。
症状の有無にかかわらず、HS患者には以下の眼科検査が推奨される。
HSの眼症状は以下の疾患との鑑別が必要である。
特にクローン病との鑑別は重要である。HSとクローン病は17〜40%の患者で共存し2)、類似の免疫調節不全を共有する。治療反応が診断の手がかりとなることもある。HS特有のサイトカインを標的とした全身療法後に眼症状が改善すれば、診断を裏付ける。
HSの治療は重症度に応じた段階的アプローチをとる。
第1段階(軽症):局所または経口抗生物質(ドキシサイクリン、クリンダマイシン等)
第2段階(中等症):経口または注射によるステロイドの追加
第3段階(重症・難治性):生物学的製剤の導入
現在HSに対して承認されている生物学的製剤は以下の2剤である。
Sayginらの研究では、眼科的併存疾患を持つHS患者は皮膚科的な局所治療にはほとんど反応せず、抗TNF-α療法によく反応した。TNF-αはぶどう膜炎の早期病態にも関与しており1)、抗TNF-α療法はHSの皮膚症状と眼症状の両方を同時に治療できる利点がある。
生物学的製剤使用者は非使用者と比較して結膜炎リスクが低いとのエビデンスもある。
はい、抗TNF-α療法(アダリムマブ・インフリキシマブ)は、皮膚症状だけでなく眼の炎症にも有効であることが報告されています。TNF-αはぶどう膜炎やドライアイの病態にも関与しているため、HSの皮膚と眼の両方を同時に治療できる利点があります。眼科的併存疾患を持つHS患者では、皮膚の局所治療のみでは効果が乏しく、全身的な抗TNF-α療法が必要となることが多いとされています。
HSの病態は毛包脂腺系単位の閉塞に始まる2)。初期の組織学的変化として漏斗部棘細胞症・角化亢進が生じ、毛包周囲にリンパ組織球性の免疫細胞浸潤が出現する。毛包の破裂によりケラチンが周囲組織に漏出し、強い炎症反応を惹起する2)。
この炎症過程で皮膚および血清中のTNF・IL-1・IL-17・IL-23が上昇する。上昇したサイトカインは毛包周囲の炎症を拡大させ、膿瘍・結節の形成から排膿性瘻管へと進行する。
HSで上昇するサイトカインの多くは、眼炎症の病態にも関与する。TNF-αはケモカインや接着分子の発現を誘導し、ぶどう膜炎の炎症を長期化させる1)。IL-6は複数のタイプのぶどう膜炎における眼内免疫応答に関与し、ドライアイの眼痛とも相関する1)。
Rojas-Carabaliらのレビューでは、上皮細胞がTNF-α・IL-1・IL-6・IL-8を産生・放出し、免疫応答を増幅してドライアイにおける炎症細胞の誘引を促進することが示されている1)。
さらにIP-10/CXCL10は、白血球・好中球・好酸球・単球・間質細胞からIFN-γに応答して放出されるケモカインであり、眼内炎症にも関与する1)。
HSとクローン病はIL-1・IL-6・IL-17・IL-23・TNFの有意な増加を共有する2)。両疾患ともリンパ濾胞や肉芽腫を組織学的に特徴とし、17〜40%の患者で共存する2)。クローン病を含む炎症性腸疾患では眼合併症が周知の事実であり、HSも同様の全身性炎症調節不全により眼に影響を及ぼすと考えられている。
HSの遺伝的背景としてNotchシグナル経路の異常が注目されている。γセクレターゼ複合体のサブユニットであるPSENENの変異は、Notch受容体の細胞内切断を阻害する3)。Notch経路の障害は毛包の増殖・分化異常を引き起こし、表皮の角化亢進と毛包閉塞をもたらす。この機序はDowling-Degos病とHSの併存を説明する3)。
近年のOCTAを用いた研究では、臨床的な眼疾患がないHS患者においても網膜微小血管に異常が検出されている。中心窩血管密度(VD)・血管長密度(VLD)の低下、および網膜深層毛細血管叢におけるVD低下が報告されており、HSが潜在的な網膜血管合併症を引き起こしうることを示唆している。
抗TNF-α療法はHSの皮膚症状と眼症状の両方に有効性を示しており、今後も治療の中心的役割を担うと考えられる。新規生物学的製剤やJAK阻害薬などの開発が進むなか、これらの薬剤のHS眼合併症に対する有効性の検証が期待される。
HS患者における眼合併症の正確な有病率と発症機序の解明はまだ十分ではない。大規模な前向き研究によるHS特異的な眼症状の頻度・リスク因子の同定、および最適なスクリーニングプロトコルの確立が求められる。