LSCD の臨床所見
渦状上皮症(whorl-like epitheliopathy):フルオレセイン染色で渦巻状の上皮障害パターンを認める。軽度LSCDの初期所見である1)
palisades of Vogt(POV)の消失:輪部の柵状構造が消失する。LSCDの臨床診断の根拠となる
結膜化(conjunctivalization):角膜上皮が結膜上皮に置換される。杯細胞の角膜上への出現で確認できる1)
角膜新生血管:中等度以降で表層性新生血管とパンヌスが出現する1)

生体血縁者間結膜輪部同種移植術(living-related conjunctival limbal allograft: lr-CLAL)は、輪部幹細胞欠損症(limbal stem cell deficiency: LSCD)に対する眼表面幹細胞移植術(OSST)の一種である。適合する生存血縁者から杯細胞を含む結膜・輪部組織を採取し、患者の眼表面に移植する。
角膜上皮の幹細胞は輪部に存在し、求心的に移動しながら基底上皮細胞に分化・増殖し、表層へと移行する1)。LSCDではこの幹細胞が障害され、角膜上皮が結膜上皮に置換される。その結果、角膜の透明性が失われ視力低下を来す1)。角膜移植単独ではLSCDの眼表面を再建できず、上皮治癒不全と移植片不全に至る2)。輪部幹細胞移植(LSCT)により正常な上皮表現型を回復させ、安定した角膜表面を再建することが可能となる2)。
片眼性LSCDでは健側眼から自家移植(CLAu)が可能であるが、両眼性LSCDでは同種移植が必要となる。CLALはKLAL(死体ドナー由来)と比較して組織適合性が高く、手術成績に優れる3)。KenyonとRapozaが1995年に最初のlr-CLALを報告して以来、ドナー選定プロトコルの改良とともに術式が発展してきた。
lr-CLALの主な適応は以下の通りである。
lr-CLALは生体血縁者から輪部および結膜組織を移植する方法であり、KLALは死体ドナーから角膜輪部組織を移植する方法です。lr-CLALは組織適合性が高く、移植片拒絶率が低い点で優れています。また、lr-CLALは新鮮な結膜も同時に提供できるため、結膜疾患を伴うLSCD症例により適しています。一方、KLALは適合する生存血縁者がいない場合に選択されます。
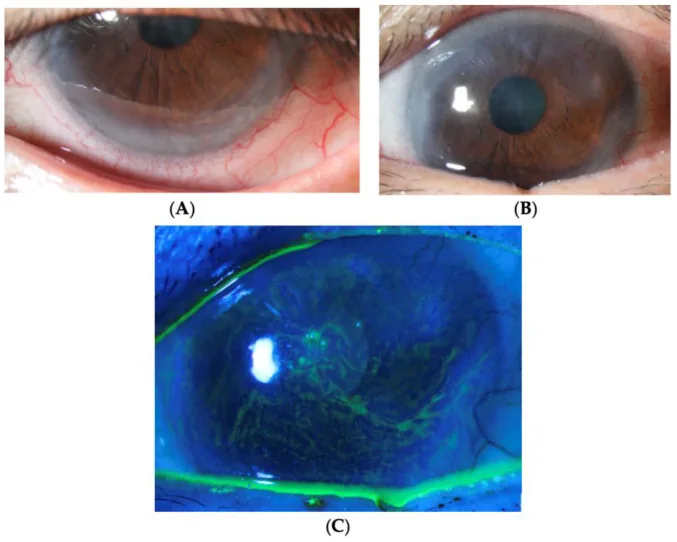
lr-CLALの対象となるLSCD患者は、眼痛・羞明・流涙・視力低下を訴える3)。結膜化の進行に伴い視力障害が増悪する。片眼性の場合は患側の視力低下が主訴となる。
LSCD の臨床所見
渦状上皮症(whorl-like epitheliopathy):フルオレセイン染色で渦巻状の上皮障害パターンを認める。軽度LSCDの初期所見である1)
palisades of Vogt(POV)の消失:輪部の柵状構造が消失する。LSCDの臨床診断の根拠となる
結膜化(conjunctivalization):角膜上皮が結膜上皮に置換される。杯細胞の角膜上への出現で確認できる1)
角膜新生血管:中等度以降で表層性新生血管とパンヌスが出現する1)
重症度分類
部分的LSCD:角膜の一部が結膜化した状態。輪部幹細胞の残存がある1)
全LSCD:角膜全面が結膜化した状態。輪部幹細胞が完全に消失している1)
Limbal Stem Cell Working Groupによるstaging:Stage 1(中央5mm透明)、Stage 2(中央5mm関与)、Stage 3(全角膜面関与)に分類される3)
輪部関与の亜分類:A(50%以下)、B(50%超〜100%未満)、C(100%)でさらに細分される3)
lr-CLALの適応となるLSCDの原因は多岐にわたる。
| 原因カテゴリ | 代表的疾患 |
|---|---|
| 外傷性 | 化学外傷、CL使用 |
| 免疫介在性 | SJS、GVHD、粘膜類天疱瘡 |
| 遺伝性 | 無虹彩症 |
単一施設の738眼の検討では、無虹彩症が30.9%、化学・熱外傷が20.6%、CL関連が16.8%、SJSが10.4%と報告されている1)。片眼性LSCDでは化学外傷が最多原因である1)。
その他の原因として、緑内障手術(マイトマイシンC・5-FU併用)1)、放射線照射1)、感染性角膜炎1)、春季カタル1)なども報告されている。
lr-CLALの相対的禁忌としては、顕著な結膜炎症・瘢痕、ムチン著減、水層涙液減少、眼表面の角化がある。これらの状態ではOSSTの予後が不良である。全身免疫抑制に対する医学的禁忌も相対的禁忌となる。
LSCDの診断は臨床所見と画像検査の組み合わせに基づく1)。
臨床診断の要点:
| 検査法 | 利点 |
|---|---|
| 印象細胞診 | 杯細胞の同定が可能1) |
| 共焦点顕微鏡 | 全層の細胞評価が可能1) |
| 前眼部光干渉断層計(OCT) | 非接触・迅速な評価1) |
印象細胞診では結膜杯細胞の存在が結膜化を示す1)。サイトケラチン3(角膜上皮マーカー)とサイトケラチン19(結膜上皮マーカー)の免疫組織化学染色が鑑別に用いられる1)。
lr-CLALの成功にはドナー選定が極めて重要である。シンシナティ・ドナー選定プロトコルでは以下の手順で評価を行う。
理想的なドナーは、ABO血液型が適合し、HLA適合性が高い第一度近親者です。ドナー眼に長期のコンタクトレンズ装用歴や手術歴がなく、眼表面疾患のないことが条件です。シンシナティプロトコルに従い、血液型・抗体検査・HLAタイピング・感染症スクリーニングを段階的に行い、最も適合するドナーを選定します。
lr-CLALの手術は、ドナーセグメントの採取とレシピエント眼への移植の2段階で行われる。
ドナーセグメント採取:12時と6時の位置から各約2時計時間の結膜・輪部セグメントを採取する。合計採取量は6時計時間未満とし、ドナー眼のLSCD誘発を防止する。BSS注入で結膜を挙上し、輪部を越えて角膜上1mmまで鈍的剥離を行い幹細胞を含める。
レシピエント眼の準備:360度の結膜切開を行い、結膜を2〜3mm後退させる。肥厚したテノン嚢を切除し、異常角膜上皮と線維血管性パンヌスを除去する。上皮化促進と炎症抑制のために羊膜を併用することがある。
ドナー組織の配置:採取したセグメントを12時と6時の位置に10-0ナイロン縫合で固定する。組織接着剤で基部を強膜に接着し、大口径バンデージコンタクトレンズを装用させる。
同時手術として瘢痕解離(最多)、羊膜移植、全層角膜移植が行われることがある3)。CLAL後の角膜移植は炎症リスクを考慮し、術後12か月以上待つことが推奨される3)。
lr-CLAL後の長期移植片生存には全身免疫抑制が不可欠である。
シンシナティOSST免疫抑制プロトコル:
眼表面安定後、タクロリムスは術後12〜18か月から、MMFは術後3年から漸減を開始する。拒絶反応の既往がある場合は低用量免疫抑制を無期限に継続する。シクロスポリンAとMMFは長期使用でも忍容性が良好であると報告されている3)。
術後局所治療:モキシフロキサシン0.5%、ロテプレドノール1%、シクロスポリンA 1%点眼、および防腐剤無添加人工涙液が使用される3)。
複合的OSST手技
シンシナティ法(KLAL/lr-CLAL):重度の瘢痕性結膜疾患と全輪部欠損を伴う両眼性症例に適応される。lr-CLALセグメントを12時・6時に配置し、3時・9時にKLAL組織を追加してほぼ360度の輪部再建を行う
lr-CLAL/CLAu併用:重度片眼性LSCD+輪部・結膜併発疾患に適応される。抗原負荷を最小限に抑えつつ健康な輪部幹細胞と結膜量を最大化する
合併症と対応
急性拒絶反応:10〜40%に発症する。疼痛・充血・移植片腫脹・上皮拒絶線を呈する。局所・全身ステロイドの増量で治療する
慢性拒絶反応:緩徐な表面不全と移植片菲薄化を来す。全身免疫抑制薬の増量が有効である
続発緑内障:長期ステロイド使用や原疾患に伴い発症しうる3)。点眼治療が無効な場合は線維柱帯切除術やチューブシャント手術が適応となる3)
眼表面が十分に安定した場合、タクロリムスは術後12〜18か月から、MMFは術後3年から漸減を開始します。ただし、移植片拒絶反応の既往がある場合は低用量の免疫抑制を無期限に続ける必要があります。免疫抑制薬の管理は臓器移植の専門医と連携して行い、定期的な血液検査で副作用をモニタリングします。
ドナー眼からの採取量を結膜・輪部セグメントあたり2〜2.5時計時間、合計5時計時間未満に抑えることで、ドナー眼にLSCDが誘発されるリスクは低いとされています。術後は抗菌薬点眼を1週間程度使用します。ドナー眼に重大な合併症が発生する可能性は低いですが、術前に十分な説明と同意が必要です。
lr-CLALの対象疾患であるLSCDの病態の本質は、輪部幹細胞の機能不全による角膜上皮恒常性の破綻である。
角膜上皮は重層扁平上皮であり、絶えず再生を続ける1)。1921年にVogtが記載した柵状構造(palisades of Vogt: POV)は輪部に位置し、動脈・静脈成分を有する放射状の構造物である1)。輪部幹細胞はこのPOV基底層に存在し、角膜上皮の再生源として機能する1)。
LSCDが生じると角膜上皮が結膜上皮に置換され、杯細胞が角膜上に出現する1)。結膜化により角膜の透明性が失われ、視力低下を来す2)。角膜幹細胞が7%残存していれば、現代の外科手技により角膜上皮の再生が可能であるとされる1)。
lr-CLALの治療原理は、ドナーから移植された健常な輪部幹細胞がレシピエントの角膜上に正常な上皮表現型を回復させることにある2)。移植された幹細胞は輪部に生着し、求心的に移動しながら角膜上皮を再生する。lr-CLALでは結膜も同時に移植されるため、結膜欠損の補填と杯細胞の供給も行われる。
LSCDの原因により病態の重症度は異なる。化学外傷では輪部だけでなく結膜・角膜実質も広範に障害されるため、より侵襲的な治療が必要となる3)。無虹彩症ではPAX6遺伝子変異による先天的な輪部幹細胞機能不全が原因であり、慢性進行性の経過をたどる。
lr-CLALに関する臨床データの蓄積が進んでいる。
Kasikciらは19眼のCLAL症例を解析し、術後1年の成功率は52.6%であったと報告した3)。術前LSCD stageが低いほど成功率が有意に高く(p=0.04)、化学外傷例では受傷から手術までの期間が長いほど成績が良好であった(p=0.001)3)。化学外傷の重症度と手術成功率は負の相関を示した(p=0.001)3)。ドナー・レシピエント間の近親度(第一度・第二度)は成功率に有意差を与えなかった3)。
Shanbhagらの系統的レビューでは、CLETにおける平均2.9年追跡での眼表面安定化率は61.4%(581眼中357眼)であり、2段階以上のBCVA改善は51.5%(425眼中219眼)に認められた2)。化学外傷がLSCDの原因の90%を占めていた2)。
LSCDの診断技術の進歩:前眼部OCTが非接触での角膜上皮厚測定に基づくLSCD診断法として研究されている1)。印象細胞診や共焦点顕微鏡と比較し、迅速かつ低侵襲な点で優位性がある1)。
今後の課題:
- Hu JCW, Trief D. A narrative review of limbal stem cell deficiency & severe ocular surface disease. Ann Eye Sci. 2023;8:13.
- Shanbhag SS, Nikpoor N, Rao Donthineni P, Singh V, Chodosh J, Basu S. Autologous limbal stem cell transplantation: a systematic review of clinical outcomes with different surgical techniques. Br J Ophthalmol. 2020;104:247-53.
- Kasikci M, Korkmaz I, Palamar M, Egrilmez S, Yagci A, Barut Selver O. Evaluation of the factors that influence surgical outcome in conjunctival-limbal allograft transplantation. Eye. 2023;37:2192-2196.