後天性(外傷・医原性・薬剤性)
化学熱傷:片眼性LSCDの最多原因である。アルカリ損傷が特に重篤になりやすい
コンタクトレンズ:CL装用者の2〜5%にLSCDが認められる1)。機械的刺激・低酸素環境が輪部幹細胞を障害する
薬剤誘発性:デュピルマブ3)、デュルバルマブ5)、マイトマイシンC・5-FU(緑内障手術併用時)などが報告されている
手術・放射線:翼状片手術、緑内障手術、冷凍凝固術、外照射放射線治療

角膜上皮は重層扁平上皮であり、3〜10日ごとに完全に更新される。この持続的な再生を支える幹細胞は、角膜と結膜の境界にある輪部に存在する。1921年にVogtが記載した輪部の柵状組織(palisades of Vogt: POV)がその幹細胞のニッチ(微小環境)である1)。
輪部幹細胞欠乏症(LSCD)は、これらの幹細胞が先天的または後天的に消失・機能不全に陥った状態である。角膜上皮の自己修復能が失われると、結膜上皮が角膜上に侵入する「結膜化」が生じる。結膜化に伴い表層新生血管・角膜混濁が進行し、視力障害をきたす。
輪部は結膜からの角膜への血管侵入を防ぐバリアとしても機能する。このバリアが破綻すると、角膜の透明性が失われる。LSCDは部分的(不完全な結膜化)から全周性(完全な結膜化)まで様々な重症度を呈する1)。わずか7%の輪部幹細胞が残存していれば、現代の手術技術で角膜上皮の再建が可能とされる1)。
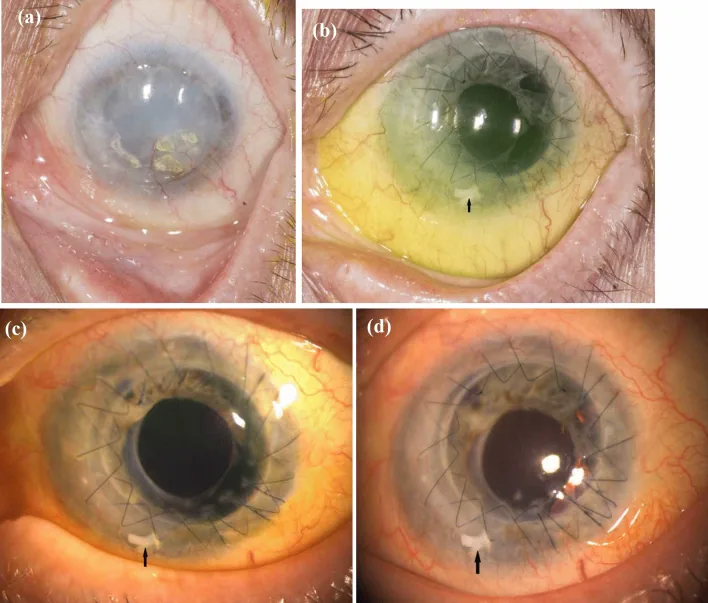
再発性上皮びらんによる眼痛と視力低下が主訴となる。異物感、コンタクトレンズ不耐症、羞明、流涙も一般的である。上皮バリアの破綻により感染性角膜炎を合併しやすい。
細隙灯顕微鏡検査で以下の所見を段階的に認める1)。
Cornea Societyが2019年に発表したグローバルコンセンサスでは、輪部の障害範囲・角膜表面の罹患範囲・視軸への影響度に基づく臨床的ステージング分類が提唱されている1)。
POVは正常では輪部全周(特に上方・下方で観察しやすい)に存在する。LSCDではPOVが消失する。ただし、10歳以下や70歳以上では正常でもPOVが観察しにくいことがある。
LSCDの原因は遺伝性・後天性・特発性に分類される1)。
後天性(外傷・医原性・薬剤性)
化学熱傷:片眼性LSCDの最多原因である。アルカリ損傷が特に重篤になりやすい
コンタクトレンズ:CL装用者の2〜5%にLSCDが認められる1)。機械的刺激・低酸素環境が輪部幹細胞を障害する
薬剤誘発性:デュピルマブ3)、デュルバルマブ5)、マイトマイシンC・5-FU(緑内障手術併用時)などが報告されている
手術・放射線:翼状片手術、緑内障手術、冷凍凝固術、外照射放射線治療
炎症性・感染性・遺伝性
ある三次施設の738眼・14年間の疫学調査では、原因の内訳は無虹彩症30.9%、化学・熱傷20.6%、CL 16.8%、スティーブンス・ジョンソン症候群 10.4%であった1)。
Mehtaらは56歳男性がデュピルマブ投与開始57か月後に両眼性のLSCDと広範な瞼球癒着を発症した症例を報告した。IL-4/IL-13シグナル阻害による杯細胞減少が眼表面炎症を惹起し、慢性炎症が輪部幹細胞を疲弊させたと考えられた。3)
Schumaierらは65歳男性が非小細胞肺癌に対するデュルバルマブ投与開始2か月後に両眼性のLSCD様所見と左眼角膜穿孔を発症した症例を報告した。角膜はPD-L1を高発現しており、PD-1/PD-L1経路の阻害が自己免疫性角膜炎を惹起した可能性がある。デュルバルマブ中止後に結膜炎症は消退した。5)
長期のコンタクトレンズ装用はLSCDの原因となりえます。特にソフトCLで多く、CL装用者の約2〜5%にLSCDが認められるとの報告があります。LSCD発症までの平均装用期間は14〜17年です。機械的刺激、低酸素環境、レンズ液の保存剤が輪部幹細胞を障害すると考えられています。
LSCDの診断は臨床所見を基本とし、各種検査を補助的に用いる1)。
| 診断法 | 長所 | 短所 |
|---|---|---|
| 印象細胞診 | 杯細胞検出で結膜化を確認 | 標本品質に依存 |
| 共焦点顕微鏡 | 全層の細胞を定量評価可能 | 5〜15分の検査協力が必要 |
| 前眼部OCT | 非接触で短時間 | 共焦点より解像度が低い |
診断の流れ:
鑑別診断として、翼状片(通常は鼻側限局)、眼表面扁平上皮腫瘍(OSSN)、周辺部感染性角膜炎を考慮する。
治療は保存的管理から段階的に進め、外科的介入を検討する。角膜移植単独はLSCDでは適応外である2)。
保存的治療
外科的治療
結膜輪部自家移植(CLAu):片眼性LSCDで健眼から輪部組織を採取する。成功率77〜100%2)
培養輪部上皮移植(CLET):小さな輪部組織片をラボで拡大培養し移植する
SLET(簡易輪部上皮移植):羊膜上にドナー幹細胞を直接播種する。ラボ不要
培養口腔粘膜上皮移植(COMET):両眼性LSCDに対し、自家口腔粘膜で代替する4)
角膜人工装具(KPro):重度の全周性LSCDに対する最終手段
培養角膜上皮移植(日本発の再生医療)や羊膜移植の併用も行われる。SJSなど炎症の強い症例ではマイトマイシンCによる線維芽細胞抑制を併用する場合がある。
Booranapongらはタイで化学熱傷3例とスティーブンス・ジョンソン症候群 3例に培養口腔粘膜上皮シート移植を施行した。化学熱傷の2例は1年後にexcellent評価を達成したが、スティーブンス・ジョンソン症候群症例は口腔粘膜自体も障害されており細胞生存率が低く、結果は不良であった。4)
角膜移植単独ではLSCDは治りません。角膜移植で提供されるのは角膜実質と内皮であり、角膜上皮の幹細胞は含まれていません。移植後も幹細胞が不足した状態は変わらず、再び結膜化と角膜混濁が進行して移植片は失敗します。まず輪部幹細胞を補充する手術を行い、角膜表面を安定させた上で、必要に応じて二期的に角膜移植を行います。
角膜上皮の幹細胞はPOV内の基底細胞層に位置する。POVの色素沈着は紫外線から幹細胞を保護する。幹細胞は基底細胞として求心的に角膜中央方向へ移動し、分化しながら表層へ向かい、最終的に脱落する1)。
幹細胞のニッチ環境:輪部幹細胞は角膜外の基質血管系からの栄養供給を必要とするため、血管に近い周辺部に位置する。角膜は透明性維持のために無血管であり、幹細胞はこの移行領域に存在する。
LSCDの発症機序:
輪部幹細胞は角膜上皮の再集団化だけでなく、結膜からの血管侵入を防ぐバリアとしても機能している。このバリア機能が失われると結膜化と新生血管が生じ、角膜の透明性は不可逆的に損なわれる。
部分的LSCDでは残存する健常輪部から角膜上皮が供給されるため、障害範囲が限局的であれば予後は比較的良好である。全周性LSCDでは外科的介入が不可欠となる。
新規薬剤によるLSCDの報告:免疫チェックポイント阻害薬やデュピルマブなどの新規生物学的製剤によるLSCDが報告されている3)5)。デュピルマブはIL-4/IL-13阻害を介して杯細胞を減少させ、慢性眼表面炎症からLSCDに至る機序が提唱されている3)。デュルバルマブはPD-L1阻害により角膜の免疫特権を破壊し、自己免疫性角膜炎を惹起する可能性がある5)。
新たな原因の報告:Elmansouriらは水痘後にLSCDを発症した10歳小児の初の症例を報告した6)。ウイルス感染によるLSCDの認識が広がりつつある。
口腔粘膜上皮を用いた再生医療:培養口腔粘膜上皮シート移植(COMET)やSOMETは、両眼性LSCDで輪部ドナーが得られない場合の有望な選択肢である4)。自家組織であるため免疫抑制が不要であり、細胞培養インフラが不要なSOMETは資源が限られた環境でも実施可能である。
iPS細胞を用いた角膜上皮再生:ドナー不足と拒絶反応の課題を解決する手段としてiPS細胞(人工多能性幹細胞)の利用が期待されている。自家iPS細胞のほか、免疫原性の低い特殊なHLA型を有する他家iPS細胞バンクの利用も検討されている。ヒトiPS細胞から角膜上皮細胞への分化誘導と細胞シート作製が報告されており、両眼性LSCDに対する新たな治療選択肢としての臨床応用に向けた研究が進んでいる。
遺伝子治療との融合:培養輪部上皮移植(CLET)は体外培養の過程で遺伝子導入が可能である。表皮水疱症などの先天性LSCDに対し、遺伝子治療との併用が検討されている。CLAuやSLETでは不可能な治療戦略であり、CLETの独自の臨床的意義とされている。
画像診断の進歩:共焦点顕微鏡や前眼部OCTの技術向上により、LSCDの早期診断・治療効果のモニタリングがより精緻になりつつある1)。
遺伝子解析の応用:無虹彩症などの遺伝性LSCDでは、遺伝子配列解析が予後予測や治療方針の決定に活用される可能性がある1)。
はい。免疫チェックポイント阻害薬はまれに眼の副作用を引き起こします。ぶどう膜炎やドライアイが比較的多いですが、重症例ではLSCDや角膜穿孔に至った報告もあります。がん治療開始後に眼の症状(充血・痛み・視力低下)が出現した場合は、速やかに眼科を受診することが重要です。