渦状角膜(cornea verticillata)
頻度:患者の50〜80%に出現
発症時期:6歳頃から認められる
部位:角膜上皮基底膜レベル
所見:灰色がかった淡い色素沈着が渦を巻くように角膜全体に広がる
保因者:女性ヘテロ保因者にも高頻度に観察される
ファブリー病は、ライソゾーム加水分解酵素であるα-ガラクトシダーゼA(α-Gal A)の欠損により、グロボトリアオシルセラミド(Gb3)をはじめとするスフィンゴ糖脂質が全身の細胞に蓄積する遺伝性代謝疾患である。
GLA遺伝子(Xq22.1)の変異によるX連鎖劣性遺伝を呈する。1898年にAndersonとFabryにより独立して報告された2)。有病率は約1万人に1人と推定されるが、新生児スクリーニングではより高頻度(1:3,000〜1:7,800)の報告もある3)。
臨床像は古典型と**遅発型(非古典型)**に大別される。古典型ではα-Gal A活性がほぼ消失し、幼児期から多臓器に障害が出現する。遅発型では残存酵素活性があり、成人期に心臓や腎臓の単臓器障害として発症する場合がある1)2)。
| 病型 | 発症時期 | 主な障害臓器 |
|---|---|---|
| 古典型 | 幼児〜学童期 | 多臓器(全身) |
| 遅発型 | 成人期 | 心臓・腎臓 |
はい、X連鎖劣性遺伝の疾患です。男性患者の娘は全員が保因者となり、息子には遺伝しません。女性保因者はX染色体の不活化パターンにより、無症状から重症まで幅広い症状を呈する可能性があります。ご家族に本疾患の方がいる場合は、遺伝カウンセリングを受けることをお勧めします。
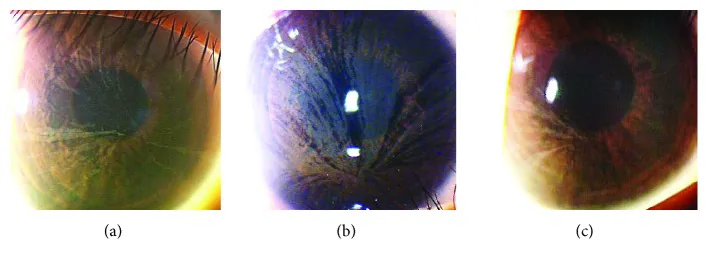
角膜の渦状混濁による視力低下はまれである。多くの場合、眼症状による自覚的な訴えは乏しい。
全身症状として、四肢末端の灼熱痛(acroparesthesia)が最も早期の症状である。発汗低下(低汗症)や消化器症状も小児期から出現する。
渦状角膜(cornea verticillata)
頻度:患者の50〜80%に出現
発症時期:6歳頃から認められる
部位:角膜上皮基底膜レベル
所見:灰色がかった淡い色素沈着が渦を巻くように角膜全体に広がる
保因者:女性ヘテロ保因者にも高頻度に観察される
ファブリー白内障
部位:後囊下および水晶体皮質
所見:車軸状(spoke-like)の混濁が特徴的
視力への影響:通常は軽微だが進行例では白内障手術の適応となる
血管系の変化
結膜血管:蛇行・拡張がみられる
網膜血管:両眼性の主幹静脈蛇行が特徴的
微小動脈瘤:結膜および網膜にみられることがある
遅発型や心臓限局型では、角膜や皮膚の典型的所見を欠くことがある。W162C変異を有する心臓型ファブリー病の症例では、眼科的評価で渦状角膜も被角血管腫も認められなかったと報告されている1)。
渦状角膜(cornea verticillata)は角膜上皮の浅い層に生じる沈着であり、通常は視力に影響しません。細隙灯顕微鏡検査で初めて発見されることが多く、患者さんご自身が気づくことはほとんどありません。ただし、白内障が進行した場合には視力低下が生じることがあります。
ファブリー病の原因はGLA遺伝子の変異である。1000種類以上の変異が報告されており、変異の種類により臨床像が大きく異なる2)。
X連鎖劣性遺伝であるため、男性(ヘミ接合体)は重症化しやすい。女性保因者(ヘテロ接合体)もX染色体不活化の偏りにより、無症状から古典型に近い重症まで多彩な臨床像を呈する1)。女性保因者の約1%にも症状が発現するとされ、角膜混濁の確認は男女ともにスクリーニングに有用である。
主なリスク要因はファブリー病の家族歴である。原因不明の四肢末端痛、若年性脳卒中、原因不明の心肥大、原因不明の腎障害を有する患者では本疾患を鑑別に挙げる必要がある2)4)。
細隙灯顕微鏡検査が最も重要である。渦状角膜は特徴的な所見であり、本疾患を疑う契機となる。白内障(後囊下車軸状混濁)の有無も確認する。非古典型の症例では眼科的所見が欠如する場合があるため1)、所見がないことで本疾患を否定してはならない。
| 検査項目 | 診断的意義 |
|---|---|
| α-Gal A活性 | 男性で確定的 |
| Lyso-Gb3 | バイオマーカー |
| GLA遺伝子解析 | 変異の特定 |
男性ではα-Gal A酵素活性の測定で確定診断が可能である。女性保因者ではX不活化の影響で酵素活性が正常範囲内を示すことがあるため、遺伝子解析が必要となる2)。血漿Lyso-Gb3は診断感度が高く、女性のスクリーニングにも有用なバイオマーカーである4)。
渦状角膜の鑑別として最も重要なのは**アミオダロン(抗不整脈薬)**による薬剤性角膜沈着症である。アミオダロン服用で生じる混濁はファブリー病の渦状角膜と極めて類似した所見を呈する。服薬歴の確認が鑑別の鍵となる。
そのほか、クロロキン、インドメタシンなどの薬剤性角膜沈着や、cornea verticillataの原因となる他の疾患との鑑別も必要である。
ファブリー病の根本的治療は**酵素補充療法(enzyme replacement therapy: ERT)**である。アガルシダーゼα(リプレガル®)またはアガルシダーゼβ(ファブラザイム®)を2週間ごとに点滴静注する。ERTにより四肢末端痛の軽減、腎機能低下の遅延、心肥大の進行抑制が期待される。早期開始が臓器障害の進行抑制に重要である。
ミガーラスタット(ガラフォルド®)は経口薬であり、amenable変異を有する患者に適応がある。変性したα-Gal Aタンパク質の立体構造を安定化させ、ライソゾームへの輸送を促進する。
渦状角膜に対する特異的な治療は不要である。白内障が進行し視機能に影響する場合には白内障手術の適応となる。
酵素補充療法(ERT)は腎臓・心臓・神経の症状進行を抑える効果がありますが、角膜の渦巻き状の沈着は通常ERTでは改善しません。ただし、角膜所見は視力に大きな影響を与えないため、積極的な治療は不要です。白内障が視力に影響する場合には手術が行われます。
ファブリー病では、GLA遺伝子変異によりα-Gal Aの活性が低下または消失する。その結果、本来この酵素が分解すべきGb3およびその脱アシル化体であるLyso-Gb3がライソゾーム内に蓄積する。蓄積したGb3は細胞機能障害、炎症カスケードの活性化、酸化ストレスを引き起こし、進行性の多臓器障害をもたらす。
角膜では、輪部の基底幹細胞にGb3が蓄積する。これらの細胞が遠心性に移動する過程で渦巻き状の沈着パターン(cornea verticillata)を形成する。沈着は角膜上皮基底膜レベルに生じる。
水晶体では上皮細胞および皮質繊維にGb3が蓄積し、後囊下に車軸状(spoke-like)の混濁が生じる。これがファブリー白内障と呼ばれる所見である。
血管内皮細胞および平滑筋細胞へのGb3蓄積は、結膜および網膜の血管蛇行・拡張を引き起こす。網膜では両眼性の主幹静脈蛇行として観察される。全身的には、腎糸球体のポドサイトや心筋細胞への蓄積が腎障害および心肥大の原因となる。
ファブリー病の治療は従来のERTに加え、複数の新規治療アプローチが研究されている。
遺伝子治療はGLA遺伝子をアデノ随伴ウイルス(AAV)ベクターなどで導入し、内因性にα-Gal Aを産生させる根治的治療法として期待されている。
**基質合成抑制療法(SRT)**はGb3の合成自体を抑制するアプローチであり、ERTと異なり静脈投与が不要な経口薬として開発が進んでいる。
新生児スクリーニングの拡大も重要な課題である。早期診断による早期治療介入が長期予後を改善する可能性がある3)。
表現型の多様性に関する知見も蓄積されている。同一のGLA変異であっても古典型から臓器限局型まで異なる臨床像を呈すること1)、女性保因者におけるX染色体不活化パターンが表現型を予測しないことなどが報告されている。非古典型ファブリー病の神経学的症候を主訴とする症例報告では、脳白質病変の精査からファブリー病の診断に至った例もある2)。