CLAu(結膜輪部自家移植)
適応:片眼性LSCD
方法:健眼の輪部結膜から2〜4時間分の組織を採取し、患眼の輪部に移植する
利点:一段階手術で完結し、培養施設不要
角膜上皮の幹細胞は角膜と結膜の境界である輪部(limbus)に存在する。輪部の柵状構造(palisades of Vogt: POV)が幹細胞のニッチ(微小環境)として機能し、角膜上皮の恒常性を維持している。
この輪部幹細胞が広範に障害されると**輪部幹細胞欠損症(limbal stem cell deficiency: LSCD)**が生じる。LSCDでは角膜上皮の再生が不可能となり、結膜上皮が角膜表面に侵入する(結膜化)4)。その結果、角膜混濁・表層血管新生・視力障害が進行する。
通常の角膜移植はLSCDには無効であり、移植片の表面が再び結膜化して不全に陥る3)。このため、正常な角膜上皮幹細胞を補充して眼表面を安定化させる眼表面再建術が必要となる。
再建術の目標は視力回復ではなく眼表面の安定化である。角膜実質の混濁が残存する場合は、眼表面安定化後に全層角膜移植(PKP)や深層層状角膜移植(DALK)を二段階で行う。
角膜輪部の幹細胞が広範に障害され、結膜上皮が角膜上に侵入している患者が対象となります。原因としては化学熱傷、Stevens-Johnson症候群、眼類天疱瘡、無虹彩症などが代表的です。結膜侵入が周辺部に限られている軽症例では、まず経過観察が行われます。
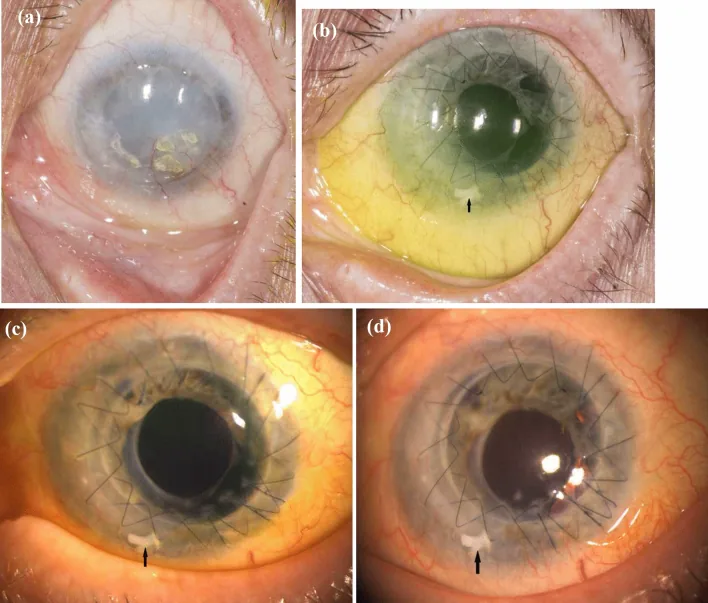
LSCDの重症度はDengらの国際分類1)により以下の3段階に分類される。
| 分類 | 結膜化の範囲 | 中心角膜 |
|---|---|---|
| Stage I | 輪部50%未満 | 非侵襲 |
| Stage II | 輪部50%以上 | 非侵襲 |
| Stage III | 全周性 | 中心侵襲 |
主な臨床所見は以下の通りである。
LSCDの原因は多岐にわたるが、化学熱傷が最多である。自家輪部移植の系統的レビューでは対象眼の88%が化学熱傷であった3)。
主な原因を以下に示す。
最も基本的な診断法である。POVの消失、結膜化の範囲、表層血管新生の程度を評価する。正常では上方・下方の輪部でPOVが観察しやすいが、10歳以下および70歳以上では観察困難な場合がある。
角膜上皮欠損の範囲を可視化する。結膜化した領域は点状染色パターンを示す。
角膜表面の細胞を採取して免疫染色を行う。角膜上皮マーカーであるサイトケラチン3(CK3)/CK12の消失と、結膜上皮マーカーであるCK13/MUC5ACの発現がLSCDの確定診断に有用である1)。
角膜上皮の厚さや構造の変化を非侵襲的に評価できる。結膜化した領域は正常角膜上皮とは異なる反射パターンを示す。
細胞レベルでPOV構造や基底細胞の形態を観察できる。角膜上皮と結膜上皮の鑑別にも有用であるが、検査機器が限られた施設にしかない。
治療法の選択は片眼性か両眼性かによって大きく異なる。片眼性LSCDでは健眼の輪部から自家組織を採取できるが、両眼性では自家輪部組織が利用できないため、口腔粘膜上皮などの代替細胞源を用いる。
CLAu(結膜輪部自家移植)
適応:片眼性LSCD
方法:健眼の輪部結膜から2〜4時間分の組織を採取し、患眼の輪部に移植する
利点:一段階手術で完結し、培養施設不要
SLET(簡便輪部上皮移植)
適応:片眼性LSCD
方法:健眼から小片の輪部組織を採取し、羊膜上に分散配置して移植する
利点:採取量が少なく健眼への負担が小さい
CLET(培養輪部上皮移植)
適応:片眼性(少量採取)または生体ドナーからのアロ移植
方法:輪部上皮細胞をex vivoで培養しシートとして移植する
利点:微小な組織から大面積シートを作製可能
COMET(培養口腔粘膜上皮移植)
適応:両眼性LSCD
方法:患者本人の口腔粘膜上皮細胞を培養しシートとして移植する
利点:自家移植のため拒絶反応が少なく、両眼性にも対応可能
Shanbhagらの系統的レビュー3)では、自家輪部幹細胞移植の3術式を以下のように比較している。
| 術式 | 解剖学的成功率 | 機能的成功率 |
|---|---|---|
| CLAu | 69% | 60% |
| SLET | 78% | 69% |
| CLET | 61% | 52% |
CLAu 22 case series(1023眼)、SLET 4 studies(253眼)、CLET 8 studies(581眼)の解析。CLAuの対象の88%、CLET・SLETの90%以上が化学熱傷であった。SLETとCLAuはCLETに比べ解剖学的成功率が有意に高かった。3)
Mazumdarらはアルカリ外傷による片眼性LSCDに対し、SLETと結膜自家移植を単段階で併施した症例を報告した2)。
24歳男性、アルカリ外傷後のstage III LSCD。術後24日で角膜上皮化が完了し、24か月の経過観察で最良矯正視力(BCVA)6/12pを達成した。単段階手術により結膜欠損の修復と輪部再建を同時に行う利点が示された。2)
眼表面再建後に角膜実質の混濁が残存する場合は、全層角膜移植またはDALKを追加する。内皮型拒絶反応の回避にはDALKが望ましい。免疫抑制薬(シクロスポリン、タクロリムス)の長期投与が必要な場合がある。
片眼性の場合は健常な反対眼の輪部から角膜上皮幹細胞を採取できます。両眼性では両眼とも輪部が障害されているため、角膜上皮幹細胞を採取できません。そのため口腔粘膜上皮など代替の細胞源を用いた培養移植(COMET)が選択されます。
眼表面再建術の主な目的は眼表面の安定化であり、直接的な視力回復を保証するものではありません。角膜実質に混濁がある場合は、再建後に角膜移植を行う二段階の治療が必要です。視力の改善には数か月から1年以上かかる場合があります。
角膜上皮幹細胞は輪部基底層のPOV内に存在する。POVは間質の乳頭状突起で構成され、血管や神経が豊富に分布する。この微小環境(ニッチ)が幹細胞の自己複製能と分化を制御している。
幹細胞は非対称分裂により自己複製しつつ、一方で**一過性増幅細胞(transit amplifying cell: TAC)**を産生する。TACは角膜中心方向へ移動しながら分裂・分化し、最終的に角膜上皮細胞となって表面から脱落する。
輪部幹細胞が障害されると以下の病態が連鎖的に進行する。
結膜化した角膜表面はバリア機能が低下し、遷延性上皮欠損を繰り返す。炎症の持続が実質融解や穿孔を招くこともある。
COMET(培養口腔粘膜上皮移植)では温度応答性培養皿が中核技術となる1)。培養皿表面のポリ(N-イソプロピルアクリルアミド)コーティングは37℃で疎水性、温度を下げると親水性に変化する。これにより、酵素処理なしに細胞シートを培養皿から剥離でき、細胞間接着やマトリクスを保持したままの移植が可能となる1)。
PMC10219018のCOMET症例では、移植後のシートおよび組織を免疫組織化学的に評価した1)。
日本では2021年6月に世界初のCOMET製品**Ocural®**が保険収載された1)。Ocural®はSymblepharon(瞼球癒着)のない両眼性LSCDに適応される。Symblepharonを伴う症例にはSakracy®が選択される1)。
Toshidaらは2症例のOcural®初期成績を報告した。症例1は79歳男性(両眼性stage III LSCD)、症例2も両眼性LSCDであり、いずれも生着を確認した。移植後のシートではp63・p75NTR・Ki-67の発現が確認され、幹細胞特性と増殖能の維持が示された。1)
片眼性LSCDにはNepic®(培養自家輪部上皮細胞シート)が使用可能である1)。
欧州ではHoloclar®が培養自家輪部上皮移植として初めてEUの医薬品として承認された1)。LSCD治療における再生医療の先駆けであり、日本のOcural®とは異なるアプローチ(輪部上皮由来 vs 口腔粘膜上皮由来)をとる。
Mazumdarらの報告では、SLETと結膜自家移植(CAG)を単段階で併施することにより、結膜欠損の修復と輪部再建を同時に達成した。術後24日で完全上皮化し、24か月でBCVA 6/12pに改善した。2)
従来のSLETでは結膜欠損部を露出強膜のまま残すか、羊膜で被覆していたが、CAGの同時施行により早期の結膜被覆と安定した眼表面が得られる可能性がある2)。
Shanbhagらの系統的レビュー(1857眼)では、自家輪部移植全体で解剖学的成功率69%、機能的成功率61%であった。術式別ではSLETとCLAuがCLETより有意に良好な成績を示した。ただし研究の質とサンプルサイズにはグループ間で有意差があり、解釈には注意を要する。3)
今後はランダム化比較試験や長期成績の蓄積が求められる。iPS細胞由来の角膜上皮細胞シートなど、次世代の細胞治療も研究段階にある。
培養口腔粘膜上皮細胞シート(CAOMECS)は2004年に報告され、両眼性LSCDに対する自家移植として有効性が確認されている。しかし長期観察では、角膜周辺部からの血管侵入による再混濁が一部症例で認められている。角膜上皮と口腔粘膜上皮の性質差が原因として示唆されており、根治的治療には角膜上皮細胞自身の使用がより望ましいと考えられている。
輪部幹細胞以外の細胞源を用いた角膜再生研究が進んでいる。
角膜実質にも前駆細胞の存在が示されており、角膜内皮についても水疱性角膜症などに対する新たな治療法として研究が進んでいる。
はい、2021年にCOMET製品であるOcural®が保険収載されました。ただし、使用できるのは日本角膜学会および日本角膜移植学会に所属し、所定の研修を修了した眼科専門医がいる施設に限られます。適応は中等度から重度の輪部幹細胞欠損症です。