独立したリスク因子
デュピルマブ投与量:高用量でリスクが上昇する
AD重症度:中等症〜重症ADで発生率が高い
治療前の結膜炎既往:既存の眼表面疾患がDIOSD発症を強く予測する

デュピルマブ(dupilumab、商品名:デュピクセント®)は、IL-4受容体αサブユニット(IL-4Rα)に結合しIL-4およびIL-13のシグナル伝達を阻害するヒトモノクローナルIgG4抗体である。アトピー性皮膚炎(AD)・気管支喘息・鼻ポリープを伴う慢性副鼻腔炎に対して承認されている。
第3相臨床試験では、デュピルマブ+ステロイド外用群の結膜炎発生率が14〜19%と、プラセボ群の8%を有意に上回った1)。市販後にはDIOSD(dupilumab-induced ocular surface disease)の頻度は最大50%に達するとの報告もある1)。眼合併症の80%は治療開始後4か月以内に発症するが、52週後の遅発例も報告されている1)。
DIOSDはADに対するデュピルマブ治療に特異的であり、喘息や副鼻腔炎への使用では報告されていない。この選択性はAD患者の眼表面がすでに脆弱であることを示唆している1)。
現時点では、DIOSDはアトピー性皮膚炎(AD)に対するデュピルマブ治療に特異的と考えられています1)。喘息や鼻ポリープを伴う慢性副鼻腔炎への使用では結膜炎の頻度上昇は報告されていません。AD患者の眼表面がもともとアレルギー性炎症で障害されていることが、デュピルマブによるサイトカインバランスの変化に対する脆弱性を高めていると推測されています。
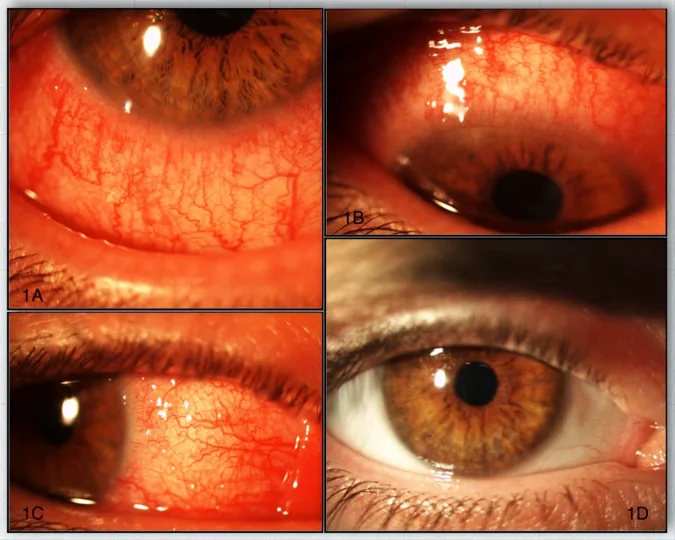
充血・痒み・刺激感・異物感・羞明・流涙・眼脂・視力低下を呈する。灼熱感や持続的な「砂っぽさ」も特徴的である1)。間欠的な単眼性複視が報告されることもある。
デュピルマブ単剤療法では平均約2週間後に発症する。ステロイド外用薬併用例では4〜8週間後と発症がやや遅延する。
DIOSDは以下の3段階に進行する。通常は両側性だが非対称である。
| 段階 | 所見 |
|---|---|
| 初期 | MGD・結膜充血・乳頭状結膜炎・点状表層角膜症 |
| 中間期 | 瞼球癒着・睫毛脱落・円蓋部短縮・角膜縁炎 |
| 進行期 | 眼瞼癒着・円蓋部消失・眼表面角化 |
DIOSDの臨床像は以下の5型に分類される1)。
1. デュピルマブ関連結膜炎(DAC):最も頻度が高く(36〜50%)、非特異性・乳頭性・濾胞性・角結膜炎型がある1)。輪部結節(トランタス斑様)を呈する場合もある。
2. 角膜障害:点状表層角膜症・角膜びらん・角膜潰瘍として発現する1)。BUT短縮を伴うことが多い。
3. 線維化合併症:瘢痕性結膜炎・瘢痕性眼瞼外反・涙点狭窄が報告されている1)。
4. ドライアイ:杯細胞減少と涙腺機能不全に起因する1)。涙液膜の不安定化と粘膜炎症を引き起こす。
5. 眼瞼炎・眼瞼結膜炎:眼瞼腫脹・発赤・眶周囲皮膚炎を呈する1)。瘢痕性眼瞼結膜炎は重症合併症である。
独立したリスク因子
デュピルマブ投与量:高用量でリスクが上昇する
AD重症度:中等症〜重症ADで発生率が高い
治療前の結膜炎既往:既存の眼表面疾患がDIOSD発症を強く予測する
病態の本質
IL-13阻害:IL-13は眼表面で最も優位なサイトカインであり、杯細胞の分化・ムチン分泌に不可欠である1)。デュピルマブによるIL-13阻害が杯細胞の低形成とムチン分泌低下を引き起こす
Th1/Th2バランスの偏倚:IL-4/IL-13阻害によりTh1優位の免疫応答(IFN-γ過剰)が誘導され、杯細胞密度がさらに低下する1)
生検所見:結膜生検で杯細胞密度の著減(中央値3.3個/mm、対照32.3個/mm)とCD3+/CD4+ T細胞・好酸球の上皮内浸潤が認められる1)
DIOSDの診断は病歴と臨床所見に基づく臨床診断である。検査室検査や生検は通常適応されない。
必要な病歴:中等症〜重症ADに対してデュピルマブを使用中であること。発症時期がデュピルマブ開始後(通常2〜8週間)であること。
以下の検査で病期と予後を評価する。
角結膜染色:フルオレセインおよびリサミングリーンで結膜の完全性を評価する。
Schirmer試験:涙液量10mm未満は進行例における涙腺障害を示唆する。
涙液層破壊時間(TBUT):短縮はムチン欠乏を反映する。
角膜知覚検査:綿棒またはCochet-Bonnet角膜知覚計で評価する。
デュピルマブ開始前から存在するアトピー性角結膜炎(AKC)との鑑別が最も重要である。AKCでは杯細胞密度が増加するのに対し、DIOSDでは減少する1)。アレルギー性結膜炎・ウイルス性結膜炎・眼類天疱瘡・眼部GVHDも鑑別に挙がる。
DIOSDの治療目標は炎症の制御と杯細胞機能の回復である。デュピルマブの中止は通常不要であり、眼科的治療を行いながら継続可能である1)。
第一選択
低力価ステロイド点眼:フルオロメトロン0.1%で5例中2例が完全消失、3例が著明改善した1)。眼圧上昇に注意する
タクロリムス眼軟膏:0.03%タクロリムス眼軟膏で4例中2例が完全消失、2例が著明改善した1)。カルシニューリン阻害薬は杯細胞を増加させ上皮細胞死を防ぐ可能性がある
シクロスポリン点眼:0.05%CsA点眼液を維持療法として使用する。1%酢酸プレドニゾロンとの併用で再発なく管理された報告がある
補助療法
人工涙液:眼表面の湿潤維持に使用する。単独では不十分であることが多い
温罨法・眼瞼マッサージ:MGD合併例に有効である1)
抗ヒスタミン点眼:単独では効果が乏しい1)
パッチテスト:接触性アレルギーの関与が疑われる場合に施行する。乳化剤・界面活性剤・香料の回避でDIOSD改善が報告されている1)
ほとんどの場合、中止は不要です1)。DIOSDのほぼ全例が眼科的治療(ステロイド点眼やカルシニューリン阻害薬)で改善します。デュピルマブのAD・喘息に対する効果が優れているため、中止による全身疾患の悪化を考慮し、眼科治療を行いながら継続するのが一般的です。ただし、重症の瘢痕性合併症(瘢痕性眼瞼結膜炎・角膜潰瘍)や治療抵抗性の場合は、集学的チームで中止を検討します。
DIOSDの機序は複雑であり、以下の5つの仮説が提唱されている1)。
デュピルマブによるIL-4/IL-13阻害はTh2応答を抑制する一方、Th1サイトカイン(IFN-γ)が優位となる1)。IFN-γは杯細胞密度を低下させ、ムチン分泌を減少させる。
IL-4/IL-13の抑制によりDemodexが増殖し、IL-17介在性の酒さ様炎症が誘導される可能性がある1)。
異常なOX40L介在性シグナルが活性化され、春季カタル様の病態が生じる可能性が指摘されている1)。
デュピルマブ治療中に末梢好酸球数が増加することがあり、眼表面への好酸球浸潤が炎症に関与する可能性がある1)。
最も有力な仮説である1)。IL-13は眼表面で最も優位なサイトカインであり、杯細胞の分化とムチン分泌に不可欠である1)。デュピルマブによるIL-13阻害は杯細胞の低形成を引き起こし、ムチン分泌低下・涙液膜不安定化・粘膜炎症の連鎖を誘導する1)。この病態は**DAMD(dupilumab-associated mucin deficiency)**と呼ばれる1)。
Bakkerらの結膜生検では、DIOSD患者で杯細胞の著減(3.3個/mm vs 対照32.3個/mm)と好酸球・T細胞の浸潤が確認された1)。これはアレルギー性結膜炎やAKCでの杯細胞増加(高IL-13発現)とは対照的であり、DIOSDが独立した疾患単位であることを裏付けている1)。
アレルギー性結膜炎やアトピー性角結膜炎(AKC)では、IL-13が高発現しており杯細胞密度は増加しムチン分泌も亢進しています。一方DIOSDでは、デュピルマブがIL-13を阻害するため杯細胞密度が減少します1)。生検所見でも杯細胞密度は対照の約10分の1に低下しています1)。つまり両者は炎症性眼表面疾患ですが、杯細胞の変化が正反対であり、病態メカニズムが根本的に異なります。
DIOSDとDAMDは比較的新しい疾患概念であり、デュピルマブの市販後に認識が急速に広がった1)。結膜生検による杯細胞減少の確認がこの病態の理解を大きく進展させた1)。
接触性皮膚炎がDIOSDの修飾因子である可能性が示唆されている。パッチテストで同定されたアレルゲン(乳化剤・界面活性剤・香料)の回避により、一部の患者でDIOSDが改善したとの報告がある1)。
カルシニューリン阻害薬が杯細胞密度を回復させるメカニズムの解明、バイオマーカーによるDIOSD発症の予測、長期予後データの蓄積が求められる。レチノイン酸代謝の異常がDIOSDに関与する可能性も指摘されており1)、ビタミンA補充療法の役割が今後検討される可能性がある。
- Reji MA, Haque A, Goyal S, Krishnaswamy G. Dupilumab-induced ocular surface disease: a primer. BMJ Case Rep. 2022;15:e249019.