ステージ1(軽症)
点状表層角膜症:角膜上皮の不整・過形成
涙液破壊時間短縮:涙液の安定性低下
表層新生血管:輪部からの血管侵入

角膜神経再建術(corneal neurotization; CN)は、神経栄養性角膜症(neurotrophic keratopathy; NK)に対し、健全な感覚神経を角膜に移行して再神経支配を図る手術である1)。NKは三叉神経の障害により角膜知覚が低下・消失し、上皮の恒常性が破綻する難治性疾患で、有病率は10,000人あたり約5人とされる。
従来のNK治療は人工涙液・瞼板縫合など対症的であり、根本的な神経障害に対処できなかった。CNは角膜感覚の回復を通じて眼表面を安定化させ、長期予後を改善しうる唯一の術式である1)。
以後、内視鏡下アプローチ・無細胞同種移植の導入など、術式は急速に多様化している1)。
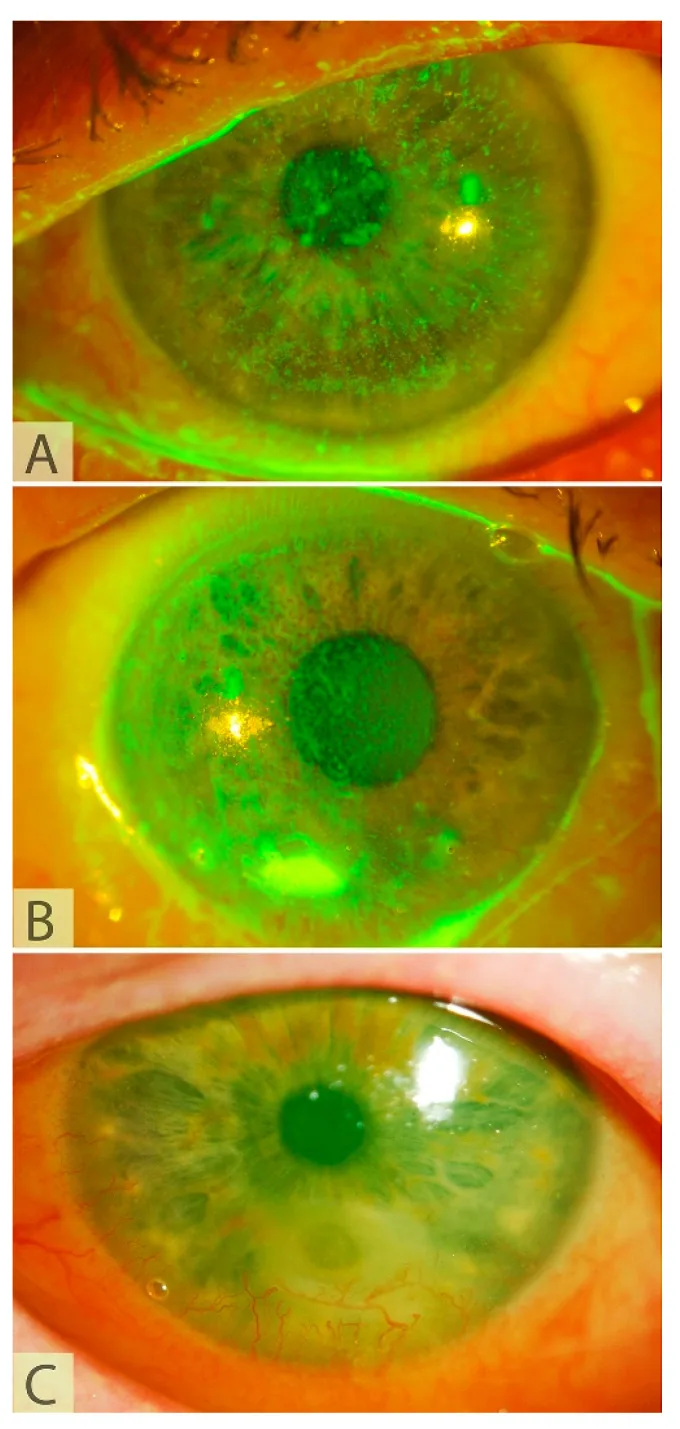
CNの対象となる神経栄養性角膜症の症状と所見を以下に示す。
NK患者は角膜知覚低下のため症状を自覚しにくい。
NKの重症度はMackie分類で評価する。
ステージ1(軽症)
点状表層角膜症:角膜上皮の不整・過形成
涙液破壊時間短縮:涙液の安定性低下
表層新生血管:輪部からの血管侵入
ステージ2(中等症)
遷延性上皮欠損:辺縁が丸く巻き上がった(rolled edge)上皮欠損
実質浮腫:Descemet膜皺襞を伴う
前房内炎症:軽度のフレアを認める
ステージ3(重症)
角膜融解:実質の菲薄化と潰瘍形成
角膜穿孔:融解が進行した最重症
感染合併:二次感染のリスクが高まる
角膜知覚はCochet-Bonnet角膜知覚計(CB)で定量評価する。0mm(無感覚)〜60mm(正常)のスケールで、20mm未満は低感受性と判定する1)。
NKは三叉神経の経路上のあらゆる部位の障害で生じる1)3)。
角膜上皮下神経叢の密度・形態を非侵襲的に観察する2)。術前のベースラインと術後の神経再生モニタリングに有用である。術後3ヶ月から神経パラメータの改善が確認される2)4)。
Cochet-Bonnet角膜知覚計(CBA)が標準的な定量検査である。0.12mm径のナイロンフィラメントを60mm(最大長、最小圧力)から角膜に垂直に当て、知覚があるまで10mm刻みで短くする。フィラメント長が短いほど圧力が増し、知覚低下が重度であることを示す。20mm未満で低感受性、50mm以上で高感受性と判定する。
NKの治療はMackieステージに応じた段階的アプローチが基本となる。
保存的治療に反応しない症例、1年以上の持続的角膜無感覚を有する症例がCNの候補となる1)。
ドナー神経を直接角膜輪部に移行する方法。
介在神経移植片を用いてドナー神経と角膜を架橋する方法。全症例の63%で採用される2)。
| 項目 | 直接法 | 間接法 |
|---|---|---|
| 知覚回復速度 | 早い | やや遅い |
| 12ヶ月時の成績 | 同等 | 同等 |
| 二次手術部位 | なし | あり |
12ヶ月時点では直接法と間接法に有意な知覚回復の差はない1)2)。
ドナー神経の選択は神経の生存能力・軸索数・角膜への近接性に基づく5)。
| 神経 | 有髄軸索数 | 特徴 |
|---|---|---|
| 眼窩上神経 | 約6,000 | 角膜に近く第一選択 |
| 滑車上神経 | 約2,500 | 解剖学的変異あり |
| 大耳介神経 | 約6,530 | 両側性NKで有用 |
Terzisらは有効な神経再建に必要な有髄軸索数のカットオフを900本と提唱している4)。眼窩上・滑車上神経の遠位部はいずれも2,000本以上の有髄軸索を含み、この基準を十分に満たす4)5)。
比較研究では、12ヶ月時点の角膜知覚回復に有意差はない。直接法は移植片が不要で知覚回復がやや早い(3〜6ヶ月でCB値が統計学的に有意に改善)が、間接法は小切開で施行でき両側性NKにも適用可能である。術式の選択はドナー神経の利用可能性、角膜までの距離、術者の経験に基づいて判断する。
角膜は体内で最も神経密度が高い組織の一つで、1mm²あたり約7,000個の侵害受容器が存在する。感度は歯髄の40倍、皮膚の400〜600倍である。
神経支配は三叉神経第1枝(眼神経)→鼻毛様体神経→長毛様体神経を経て角膜に至る。神経はBowman膜を貫通し上皮下神経叢を形成する。受容器の70%はポリモーダル(化学・熱・機械刺激に応答)、20%は機械受容器、10%は冷受容器である。
角膜神経はサブスタンスP・CGRP・ニューロペプチドY・VIPなどの神経伝達物質を含有・放出する。これらは上皮細胞の増殖・移動・再生を制御し、角膜の恒常性維持に不可欠である。
NGF・BDNF・GDNF・NT-3・NT-4/5などの栄養因子も角膜神経から供給される。これらの因子の喪失が、NKにおける上皮治癒遅延と恒常性破綻の根本原因となる。
CNでは健全なドナー神経が角膜強膜接合部に再配置される1)。
直接法ではドナー神経の遠位端を直接角膜に埋入する。間接法では介在移植片を介してドナー神経と角膜を架橋する。いずれの場合も、ドナー神経から軸索線維が角膜実質と上皮下層に伸展し、角膜の再神経支配が生じる1)。
軸索再生はWallerian変性の典型的パターンに従う1)。初期の軸索崩壊後、マクロファージが変性ミエリンを除去し、Schwann細胞がドナー神経の健全な近位部から分化・遊走して軸索再生を促進する。NGFやIL-1の上方調節が軸索発芽を促す重要な役割を果たす1)。
ラットモデルにおいて、CNは角膜神経密度を増加させたが、移植片を通って再生した軸索のうち角膜に到達したのはごく一部であった。角膜は特定の表現型をもつ無髄神経線維のみの成長を選択的に許容する可能性が示唆されている1)。
角膜神経の栄養機能は知覚機能よりも先に回復する傾向がある。このため、12ヶ月時点でCB値の改善が乏しくとも、IVCMで角膜神経が確認され上皮欠損が治癒している症例が存在する1)。
2025年のスコーピングレビュー(12研究・164眼)では、CNの成功率は60.7〜100%(平均90%)であった。術前CCS平均2.7mm(CBA)は術後36.0mmへ有意に改善した(範囲:21.1〜49.7mm)。角膜知覚は平均4.1ヶ月で出現し、12ヶ月でピークに達した2)。
間接法(腓腹神経移植)が全症例の63%を占め最多であった。無細胞同種移植は自家移植と同等の成績で、手術時間の短縮とドナー部位合併症の回避が利点である2)。
Catapanoらの19眼(平均年齢12.5歳)の報告では、87%の患者がCB 40mmに達し、64%が完全知覚を回復した。角膜強膜トンネルに束状を挿入した群はより早期の知覚回復を示した2)。
11歳男児のMackieステージ1症例では、MICN後6ヶ月で客観的知覚改善が出現し、21ヶ月で中心角膜知覚は20mmに達した。Schirmer試験は15mm→30mmへ改善し、視力は6/18→6/5に回復した6)。
高齢(62歳・70歳)かつ長期除神経(23年)の2症例では、MICN後に持続的な知覚改善が得られなかった。三叉神経近位部の損傷(聴神経腫瘍術後など)では「機能的予備能」が低く、末梢性原因(ヘルペス角膜炎など)と比較して予後不良となる可能性がある7)。
これらの知見から、高齢・長期除神経・三叉神経近位部障害はCNの予後不良因子と考えられ、患者選択とカウンセリングにおいて考慮すべきである7)。
2025年のスコーピングレビュー(164眼)では、成功率は60.7〜100%(平均90%)と報告されている。術前の角膜知覚(CBA)は平均2.7mmから術後36.0mmへ有意に改善し、12ヶ月時点で小児では60%以上が正常知覚に到達した。ただし、高齢・長期除神経症例では成績が劣る可能性がある。
- Hubschman S, Rosenblatt MI, Cortina MS. Corneal neurotization for the treatment of neurotrophic keratopathy. Curr Opin Ophthalmol 2025;36:294-301.
- Samoilă O, Samoilă L, Petrescu L. Corneal Neurotization, Recent Progress, and Future Perspectives. Biomedicines 2025;13:961.
- Dragnea DC, Krolo I, Koppen C, et al. Corneal Neurotization-Indications, Surgical Techniques and Outcomes. J Clin Med 2023;12:2214.
- Saini M, Jain A, Vanathi M, et al. Current perspectives and concerns in corneal neurotization. Indian J Ophthalmol 2024;72:1404-11.
- Serra PL, Giannaccare G, Cuccu A, et al. Insights on the Choice and Preparation of the Donor Nerve in Corneal Neurotization for Neurotrophic Keratopathy: A Narrative Review. J Clin Med 2024;13:2268.
- Lee BWH, Khan MA, Ngo QD, et al. Minimally invasive, indirect corneal neurotization using an ipsilateral sural nerve graft for early neurotrophic keratopathy. Am J Ophthalmol Case Rep 2022;27:101585.
- Ting DSJ, Pradhan SP, Barnes E, et al. Minimally invasive corneal neurotization for neurotrophic keratopathy: The potential effect of age, denervation chronicity and lesion location. Am J Ophthalmol Case Rep 2023;29:101804.