CNA1(常染色体優性型)
重症度:軽症
原因遺伝子:未同定(12q 領域の候補遺伝子)
角膜屈折力:約 38 D(正常より 3〜7 D 低い)
角膜中央:透明
遠視:軽度〜中等度(平均 +6.33 D)

扁平角膜(cornea plana)は角膜周辺部が強膜化することで角膜が扁平化する先天性疾患である。角膜と強膜の境界が不明瞭となり、透明角膜径が小さくなる。両眼性が多く、男女ともに発症する。
発生段階における輪部原基の異常により生じると考えられている。常染色体優性の CNA1 と常染色体劣性の CNA2 の 2 型に分類される。
きわめて稀な疾患である。CNA2 はフィンランド北部とサウジアラビアに創始者効果による集積が認められる。フィンランドの症例は世界の CNA2 症例の約 80% を占める。CNA1 はデンマーク・ドイツ・米国・オランダ・キューバで家系が報告されている。
CNA1(常染色体優性型)
重症度:軽症
原因遺伝子:未同定(12q 領域の候補遺伝子)
角膜屈折力:約 38 D(正常より 3〜7 D 低い)
角膜中央:透明
遠視:軽度〜中等度(平均 +6.33 D)
CNA2(常染色体劣性型)
重症度:重症
原因遺伝子:KERA 遺伝子(12q)のホモ接合型変異
角膜屈折力:約 30 D 以下1)
角膜中央:混濁を伴うことが多い
遠視:高度(+10 D 超)
CNA1 は常染色体優性遺伝で軽症型です。角膜中央は透明であり、角膜屈折力は約 38 D で正常範囲に近く、遠視も軽度です。一方 CNA2 は常染色体劣性遺伝で KERA 遺伝子変異が原因の重症型です。角膜中央に混濁を伴い、角膜屈折力は約 30 D まで低下し、+10 D を超える高度遠視を呈します。CNA2 では隅角異常や虹彩異常など他の眼合併症を伴うことも多く、予後は CNA1 より不良です。
高度の遠視による視力不良で小児期に受診することが多い。CNA2 では弱視を伴うことがある。角膜混濁による視力低下を訴える場合もある。
角膜が扁平化し角膜と強膜の境界が不明瞭である。角膜周辺部は混濁を呈し、CNA2 では中央にも混濁がみられることがある。比較的若年で老人環(arcus lipoides)が出現する。浅前房を認め、報告されている前房深度は 0.8〜2.1 mm である。
| 所見 | CNA1 | CNA2 |
|---|---|---|
| 角膜屈折力 | 約 38 D | 約 30 D 以下 |
| 角膜中央部 | 透明 | 混濁あり |
| 遠視度数 | +6.33 D 前後 | +10 D 超 |
CNA2 では角膜中央に直径 4〜6 mm の円形不透明肥厚を認めることがある。この肥厚は Descemet 膜に付着し、その周囲で角膜は最も菲薄化する。虹彩異常(虹彩萎縮・虹彩結節・瞳孔異常)を伴うこともある。
ある症例では K 値が 21.8/27.0 D および 19.4/28.7 D ときわめて扁平であり、前房深度は 1.15 mm および 0.97 mm、中心角膜厚は 410 μm および 315 μm と菲薄であった1)。
CNA2 は第 12 染色体上の KERA 遺伝子のホモ接合型変異により生じる。KERA 遺伝子はケラトカンをコードする。ケラトカンは角膜に特異的なプロテオグリカンであり、コラーゲン原線維の間隔と直径の制御に関与する。
ミスセンス変異とナンセンス変異の両方が報告されている。特にサウジアラビアの集団では 7 種類の異なる KERA 変異が確認されている。これまでに 15 の KERA 変異が報告されており、そのうち 7 つがミスセンス変異である1)。
CNA1 の原因遺伝子は未同定である。第 12 染色体上の 2 つの候補遺伝子の解析が進行中であるが、DCN・DSPG3・LUM・PITX2・FOXC1 などの既知遺伝子は原因として除外されている。
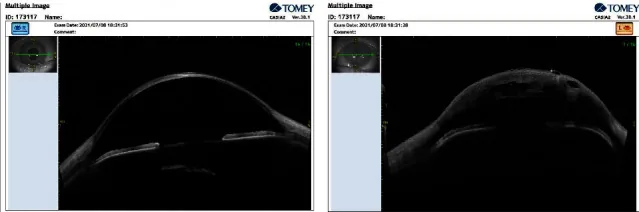
角膜周辺部の強膜化と角膜扁平化を確認する。細隙灯顕微鏡の観察系を側方に大きく振ると角膜の扁平化が一目瞭然となる。CNA2 では中央角膜の混濁も評価する。
角膜屈折力の測定は CNA1 と CNA2 の鑑別に有用である。CNA2 では 30 D 程度、CNA1 では 38 D 程度まで扁平となる。古い角膜曲率計では 30 D 未満を測定できないため、弱いプラスレンズを装着して測定範囲を拡張する手法がある。
角膜・隅角・虹彩の関係がわかりやすく有用である。中央角膜混濁の深さと範囲の評価にも使用される。
| 疾患 | 鑑別のポイント |
|---|---|
| 強膜化角膜 | 角膜不透明・扁平化のみ |
| EDS VI 型 | 全身症状を伴う |
| Rieger 異常 | 前眼部形成異常 |
その他、後部多形性角膜ジストロフィ(PPCD)・ムコ多糖症・小角膜との鑑別が必要である。全身奇形を伴わない孤立した角膜扁平化は扁平角膜の可能性が高い。
扁平角膜の診断は細隙灯顕微鏡検査による角膜の扁平化と周辺部の強膜化の確認、およびケラトメトリーによる角膜屈折力の低下の測定に基づきます。CNA2 では角膜屈折力が 30 D 程度まで低下します。前眼部 OCT は角膜・隅角の詳細な評価に有用です。確定診断には KERA 遺伝子の遺伝子検査が用いられます。鑑別診断として強膜化角膜、エーラス・ダンロス症候群 VI 型、Rieger 異常などを除外する必要があります。
混濁が周辺に限局する場合は遠視の屈折矯正が基本となる。眼鏡処方では自覚的屈折検査に基づき他覚的測定値よりも 3〜4 D 弱いレンズを処方することが推奨されている。
混濁が中央に及ぶ場合には角膜移植を検討する。しかし全層角膜移植の成績は不良であり、隅角異常に伴う緑内障への注意が必要である。
扁平角膜では浅前房と異常な K 値のため白内障手術が困難である。眼内レンズ 度数計算では通常の光学式測定器が使用できない場合があり、SRK 回帰式が用いられることがある1)。ある症例では 34 D のトリック 眼内レンズ を使用し、術後矯正視力 6/12 が得られた1)。手術時には粘弾性物質の十分な使用と高い灌流圧による前房維持が重要である1)。
浅前房のため閉塞隅角緑内障のリスクが高い。開放隅角緑内障の報告もある。定期的な眼圧測定と隅角検査によるモニタリングが不可欠である。
可能ですが技術的に困難です。浅前房と異常に扁平な角膜のため、眼内レンズ 度数計算は通常の測定器では対応できない場合があります。SRK 回帰式などの代替的な計算方法が使用されます。手術中は粘弾性物質を十分に使用して前房を維持し、角膜内皮を保護することが重要です。トリック 眼内レンズ の使用により高度乱視の矯正も可能です。最近の報告では良好な屈折結果が得られています。
KERA 遺伝子がコードするケラトカンは Small Leucine-Rich Proteoglycan(SLRP)ファミリーに属する。ケラトカンは 10 個のロイシンリッチリピート(LRR)モチーフを有し、角膜実質のコラーゲン原線維の間隔(42〜44 nm)と直径を制御する1)。この均一な原線維配列が角膜の透明性・屈折力・強度の維持に不可欠である。
KERA 変異によりケラトカンの構造が不安定化し、コラーゲン原線維への結合が障害される。ある新規変異(c.659T>C, p.Leu220Ser)ではタンパク質モデリングにより LRR モチーフ内の疎水性コアが破壊され、アスパラギンラダーの安定構造が損なわれることが示された1)。
PACD は 12q21.33 に位置する KERA・LUM・DCN・EPYC の 4 つの SLRP 遺伝子のヘテロ接合型欠失により生じる常染色体優性疾患である2)。扁平角膜と同様に K 値の低下(41 D 未満)と角膜菲薄化を呈する2)。両疾患の共通点は KERA 遺伝子異常による角膜構造の変化であるが、PACD は複数遺伝子の欠失、扁平角膜 CNA2 は KERA 単一遺伝子の点変異という遺伝的機序の違いがある。
遺伝子検査の進歩により新規 KERA 変異の同定が進んでいる。これまでに 15 の KERA 変異が報告され、遺伝カウンセリングの精度向上に寄与している1)。タンパク質モデリングを用いた意義不明変異体(VUS)の病原性予測は遺伝子診断の新たなアプローチとして注目される1)。
白内障手術においてはトリック 眼内レンズ やバイオメトリーの工夫により良好な屈折結果が得られるようになった1)。今後は細胞治療・遺伝子治療の臨床試験への参加も視野に入る1)。