グラム陽性球菌
ブドウ球菌:小円形で境界が比較的明瞭な限局性膿瘍を呈する。進行は緩徐であるが、MRSAでは重症化しやすい1)。アトピー性皮膚炎ではMRSA検出率が高い。
肺炎球菌:匐行性角膜潰瘍と呼ばれる特徴的な所見を示す。病変の一端が改善し他端が進行するため、這うように移動して見える1)。荚膜により好中球貪食に抵抗し、深部に進展して角膜穿孔を来しうる。

細菌性角膜炎は角膜実質への細菌感染により生じる炎症性疾患である。角膜潰瘍と呼ばれることもあるが、組織欠損(潰瘍)を伴わない感染もあるため厳密には同義ではない。未治療または重症例では角膜穿孔から眼内炎に至り、眼球喪失となることもある。
年齢別発症数は2峰性の分布を示す。10〜20歳代のピークではコンタクトレンズ関連が多く、60歳以上のピークでは原因不明例が多い。米国ではコンタクトレンズ装用が最大のリスク因子であり、世界の多くの地域では外傷が主因である。
グラム陽性菌とグラム陰性菌の双方が原因となる。ブドウ球菌・連鎖球菌・緑膿菌属で約80%を占めるが、地域差がある。SCUT試験(南インド中心の多施設研究)では肺炎球菌51.5%、緑膿菌22.7%、Nocardia 11.5%であった。混合感染も最大43%に認められ、外傷が主因となる。ナイセリア・コリネバクテリウム・リステリアは正常角膜上皮を貫通しうるため注意を要する1)。
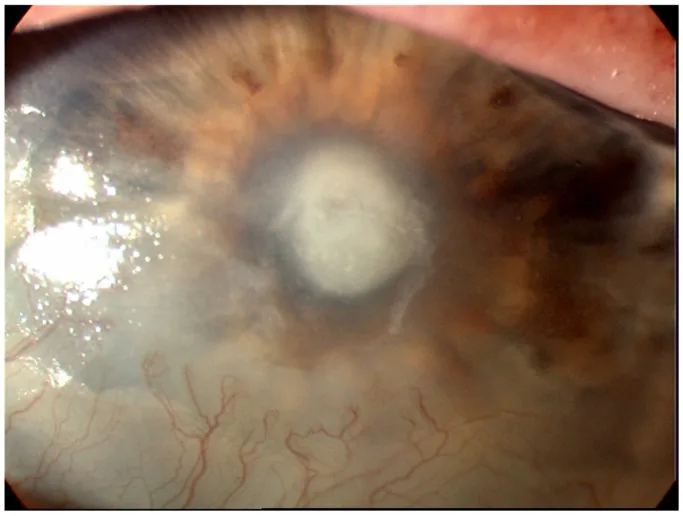
急激に発症する眼痛が特徴的である。充血、羞明、粘液膿性分泌物、視力低下を伴う。症状の進行速度は起炎菌の毒性に相関し、緑膿菌では24時間以内に急速に悪化しうる。
角膜浸潤(灰白色の混濁病巣)と上皮欠損が基本所見である。前房反応(細胞・フレア)や前房蓄膿を伴うことが多い。角膜後面沈着物(endothelial plaque)、デスメ膜皺襞、角膜菲薄化も認めうる。重症例では虹彩後癒着や続発緑内障を生じる。
グラム陽性球菌とグラム陰性桿菌では角膜所見が大きく異なるため、臨床像から起炎菌を推測する手がかりとなる1)。
グラム陽性球菌
ブドウ球菌:小円形で境界が比較的明瞭な限局性膿瘍を呈する。進行は緩徐であるが、MRSAでは重症化しやすい1)。アトピー性皮膚炎ではMRSA検出率が高い。
肺炎球菌:匐行性角膜潰瘍と呼ばれる特徴的な所見を示す。病変の一端が改善し他端が進行するため、這うように移動して見える1)。荚膜により好中球貪食に抵抗し、深部に進展して角膜穿孔を来しうる。
グラム陰性桿菌
緑膿菌:輪状膿瘍を伴い周囲角膜はすりガラス状に混濁する1)。プロテアーゼによる角膜融解で急速に進行し、穿孔に至ることが多い。ソフトコンタクトレンズ関連が多い。オルソケラトロジーとソフトCLの長期併用例でも輪状潰瘍を生じた報告がある3)。
モラクセラ:角膜中央に限局性で境界鮮明な潰瘍を形成する1)。糖尿病などの基礎疾患がリスク因子である。進行は比較的緩徐で、多くの抗菌薬に感受性を示す。
その他の起炎菌
セラチア:軽症の浅い潰瘍から広範な膿瘍まで多彩な病変を呈する1)。プロテアーゼ産生量の差が重症度に影響する。
淋菌:正常上皮を貫通し、急速に穿孔を来しうる1)。フルオロキノロン系の耐性化が進行している。
コリネバクテリウム:免疫低下やCL装用で起炎菌となる。フルオロキノロン耐性株に注意を要する1)。稀な菌種であるC. bovisでも重篤な角膜穿孔を来した症例が報告されている4)。
細菌性角膜炎は、角膜の防御機構が破綻し上皮欠損が存在する際に発症する。正常な角膜は重層扁平上皮と涙液中の防御物質(リゾチーム、ラクトフェリン、IgAなど)で守られており、感染は起こりにくい。
コンタクトレンズ関連
就寝時装用:日中装用と比較し感染リスクが約5倍に上昇する。オルソケラトロジーも同様のリスクを有する3)。
不適切なケア:洗浄液の継ぎ足し、水道水での保管・すすぎ、ケースの汚染がリスクとなる。
2週間頻回交換SCL:緑膿菌・モラクセラ・セラチアなどグラム陰性菌感染が多い。ディスポーザブルSCLは発症頻度が低い。
装飾用CL:医師の処方なしにインターネットや店頭で購入されたレンズは感染リスクが高い。
外傷・手術関連
眼表面・全身因子
眼表面疾患:ドライアイ、角膜ヘルペス、水疱性角膜症、Stevens-Johnson症候群が素因となる。神経栄養性角膜症も重要なリスクである。汚染された人工涙液から薬剤耐性緑膿菌が検出された事例もある2)。
全身因子:糖尿病、免疫抑制、アトピー性皮膚炎、膠原病が挙げられる。
薬剤関連:ステロイド長期使用、汚染点眼液、NSAIDs点眼がリスクとなる。
就寝時装用の回避と適切なレンズケアが最重要である。就寝時装用は感染リスクを約5倍に高める。レンズケースの定期交換(3ヵ月ごと)、毎日の洗浄・乾燥、水道水との接触回避が基本となる。また、定期的な眼科受診でレンズフィッティングと眼表面の状態を確認することが推奨される。
コンタクトレンズ装用歴(種類・装用時間・ケア方法)、外傷歴、既存の角膜疾患(ヘルペス角膜炎など)、眼科手術歴を確認する。全身既往歴(糖尿病・免疫抑制状態)、使用中の点眼薬(特にステロイド)、MRSA感染歴も聴取する。
角膜浸潤の部位・大きさ・深さを記録する。フルオレセイン染色で上皮欠損を評価し、前房反応(細胞・フレア・フィブリン・前房蓄膿)を確認する。角膜知覚、眼瞼閉鎖不全、涙道系の評価も行い、素因を探る。後極部が観察不能な場合は超音波Bモード検査を実施する。角膜混濁が高度で細隙灯検査による病変深度の判定が困難な場合は、前眼部OCT(AS-OCT)が補完的な評価手段となる。AS-OCTでは浸潤を実質内の高反射病変として、浮腫を角膜厚増大として客観的に描出でき、菲薄化の程度や穿孔リスクの評価にも有用である。
確定診断には角膜病巣の擦過培養による起炎菌の検出が必須である1)。抗菌薬投与前に検体を採取することが極めて重要である。点眼麻酔下に滅菌スパーテルで潰瘍辺縁部を含むように擦過する。穿孔の危険がある場合は滅菌綿棒を使用する。
塗抹検鏡:グラム染色が基本である1)。菌の染色性でグラム陽性・陰性を、形態で球菌・桿菌を判別し、起炎菌を推定する。
分離培養:血液寒天培地、チョコレート寒天培地、サブロー寒天培地、液体培地(チオグリコレートブイヨン)に接種する1)。チョコレート寒天培地はV因子・X因子を含むため、Haemophilus属や淋菌の増殖に適する。培養判定には48時間を要し、感受性結果は3〜4日かかる。
| 擦過の適応 | 培養培地 | 所要時間 |
|---|---|---|
| 浸潤径>2mm | 血液寒天 | 培養判定48時間 |
| 実質中層〜深層 | チョコレート寒天 | 感受性3〜4日 |
| 治療反応不良 | サブロー寒天 | 急ぐ場合は電話確認 |
角膜生検は、培養が陰性でありながら感染が強く疑われる場合に考慮する。
まず抗菌薬投与中であれば一時中止のうえ再培養を検討する。それでも陰性の場合は角膜生検を考慮する。また、非結核性抗酸菌やアカントアメーバなど特殊な病原体の可能性を再評価し、抗酸菌培養やPCR検査を追加する。広域抗菌薬による経験的治療を継続しつつ、治療反応を注意深く観察する。
培養結果が出るまでは広域抗菌薬による経験的治療を行う1)。起炎菌が推測不能な場合はニューキノロン系とβラクタム系の併用が推奨される。起炎菌を推測できる場合は臨床所見と背景因子から治療計画を立てる。
| 重症度 | 薬剤選択 | 投与間隔 |
|---|---|---|
| 軽症(周辺部小病変) | FQ点眼単剤 | 2〜6時間ごと |
| 中等症(上皮欠損+前房反応) | FQ点眼1剤 | 1時間ごと |
| 重症(視機能脅威) | 強化抗菌薬2剤 | 1時間ごと交互 |
重症例では強化トブラマイシン(またはゲンタマイシン)15 mg/mLと強化バンコマイシン25〜50 mg/mLを1時間ごとに交互投与する。感受性試験の結果に基づきデエスカレーションを行う。
フルオロキノロン系として第三世代のオフロキサシン(OFLX)、レボフロキサシン(LVFX)、トスフロキサシン(TFLX)と、第四世代のガチフロキサシン(GFLX)、モキシフロキサシン(MFLX)がある。セフェム系のセフメノキシム、アミノグリコシド系のトブラマイシン・ゲンタマイシン、グリコペプチド系のバンコマイシンも重要な選択肢である。
肺炎球菌は荚膜を有するため第三世代FQでは効果不十分の可能性があり、第四世代FQを選択する。緑膿菌にはアミノグリコシド系が有効であるがFQ耐性株もあるため併用する1)。グラム陰性桿菌による角膜炎では、抗菌薬開始後に死菌への免疫反応で一過性に悪化しうる点に注意する。
調節麻痺薬:前房反応が強い場合に投与し、疼痛管理と後癒着防止を図る。
眼圧降下薬:続発緑内障を伴う場合に併用する。
ステロイド点眼:起炎菌の同定後、抗菌薬への反応を確認してから(通常24〜48時間後)開始を検討する。SCUT試験のサブグループ解析では、抗菌薬開始2〜3日以内の投与で3ヵ月後の視力が改善した。ただしアカントアメーバ・ノカルジア・真菌感染では禁忌である。
薬物療法に反応しない場合や角膜穿孔例では外科的介入を行う。全層角膜移植または深層層状角膜移植(DALK)が選択される6)。小穿孔(<2mm)には角膜接着剤(シアノアクリレート)と治療用コンタクトレンズを用いる。SMILE後の重症感染ではcapをflapに変換して壊死組織を除去し抗菌薬で洗浄する手法が有効とされる5)。角膜穿孔に対してGundersen結膜弁手術を要した報告もある4)。
起炎菌が同定され、抗菌薬への反応が確認された後(通常は治療開始24〜48時間後)が目安である。SCUT試験では抗菌薬開始2〜3日以内の早期投与で視力改善が報告された。ただし真菌・アカントアメーバ・ノカルジア感染では使用を避ける。菌種が不明な場合は培養結果が判明するまで慎重に判断する。
正常角膜は重層扁平上皮と涙液中の防御物質(リゾチーム・ラクトフェリン・IgAなど)で保護されており、健常な状態では感染が起こりにくい。コンタクトレンズ装用、外傷、角膜手術などにより防御機構が破綻すると、涙液層や汚染物質から細菌が角膜実質に侵入する。
感染が成立すると、好中球を主体とする炎症細胞が浸潤し角膜膿瘍を形成する。とりわけ緑膿菌はプロテアーゼを産生して角膜実質を融解させ、急速な組織破壊と穿孔を来す1)。疾患の重症度は菌株の毒性、菌量、宿主の免疫応答、先行治療の有無、発症からの経過時間に依存する。
病態は進行性浸潤、活動性潰瘍形成、退行、治癒の4段階を経る。適切な治療が行われた場合でも角膜瘢痕による視力障害が残ることがあり、早期診断・早期治療が予後を左右する。
Morelli MKらは、市販の人工涙液(EzriCare)から分離された広範囲薬剤耐性(XDR)緑膿菌による角膜潰瘍の治療に、シデロフォアセファロスポリンであるセフィデロコルを全身投与し、局所イミペネム・ポリミキシンBの併用で治療に成功した。全ゲノム解析でblaVIM-80およびblaGES-9が同定された2)。
Kikuchiらは、オルソケラトロジーとソフトCLを10年間併用していた63歳男性に発症した緑膿菌角膜炎を報告した。角膜全面の浸潤と輪状潰瘍を呈し、レボフロキサシン・セフメノキシム・ゲンタマイシン点眼とイミペネム点滴で治癒したが角膜混濁が残存した3)。
Elsheikh Mらは、帯状疱疹角膜炎を背景にCorynebacterium bovisによる重篤な角膜感染から穿孔を来した89歳女性を報告した。近隣での牛との接触が感染経路と推定され、バンコマイシン・シプロフロキサシン併用とGundersen結膜弁手術で管理された4)。
Li Jらは、SMILE後に発症した細菌性角膜炎5例(7眼)を報告した。術後1〜3日で発症し、Staphylococcus epidermidisとStreptococcus pneumoniaeが培養された。重症例ではcapをflapに変換して壊死組織除去と抗菌薬洗浄を行い、全例で最終矯正視力20/32以上を達成した5)。
Arun KとGeorgoudisは、32歳CL装用男性の緑膿菌角膜炎に対し、急性期の抗菌薬治療後にDALKを施行して良好な視力回復を得た症例を報告した6)。
薬剤耐性菌の増加が世界的な課題であり、MRSA角膜炎やフルオロキノロン耐性菌への対応が求められている。角膜クロスリンキングの抗菌効果についても研究が進められている。
MRSAにはバンコマイシン点眼(25〜50 mg/mL)が第一選択となる。フルオロキノロン耐性菌に対してはアミノグリコシド系やセフェム系への変更を検討する。広範囲薬剤耐性(XDR)緑膿菌に対してはセフィデロコルなど新規抗菌薬の使用が報告されている2)。いずれの場合も感受性試験に基づく治療薬の選択が不可欠であり、培養検査の重要性が改めて強調される。