その他の構成疾患①
先天遺伝性角膜内皮変性症(CHED):出生時〜1〜2歳頃に両眼対称性の角膜浮腫が出現する常染色体劣性疾患である。SLC4A11の変異が原因であり、眼圧上昇は認めない。
後部多形性角膜変性症(PPCD):角膜内皮およびデスメ膜の常染色体優性疾患である。角膜浮腫を呈するが角膜径の増大は伴わない。角膜内皮検査が診断に有用である。

前眼部発生異常(anterior segment developmental anomalies; ASDA)は、前眼部形成異常(anterior segment dysgenesis; ASD)とも呼ばれ、角膜・虹彩・水晶体・前房隅角など前眼部構造に生じる先天性の発生障害を総称する概念である。
これらの疾患は表現型および遺伝学的に極めて多様であるが、房水流出路(線維柱帯・シュレム管)の発育異常に基づく眼圧上昇、すなわち発達緑内障が共通する重要な合併症となる。
ASDAに含まれる主な疾患には、後部胎生環、アクセンフェルト・リーガー症候群(ARS)、ピータース異常、原発先天緑内障(PCG)、無虹彩症、先天遺伝性角膜内皮変性症(CHED)、後部多形性角膜変性症(PPCD)、強膜化角膜、巨大角膜、虹彩角膜内皮(ICE)症候群などがある。
前眼部の発生には神経堤由来の間葉系細胞が関与しており、この細胞群は線維柱帯やシュレム管の発生にも寄与する。前眼部の形成異常が生じる場合、房水流出路の構造も同時に障害されることが多く、房水流出抵抗の増大から眼圧が上昇する。このため発達緑内障はASDAに共通する合併症となる。
ARSは眼症状と全身症状を呈する常染色体優性疾患である。眼所見としては後部胎生環(前方に転位・肥厚したシュワルベ線)、虹彩低形成、多瞳孔症、虹彩偏位がみられる。突出したSchwalbe線と虹彩に癒着を認めるものをAxenfeld異常、さらに虹彩や実質の萎縮を認めるものをRieger異常と呼ぶ。全身所見として骨発育異常や歯牙異常などを伴う場合をRieger症候群と呼んでいる。角膜は一般に正常で内皮の構造も正常であるが、遺残物による物理的な接触によって二次的に混濁をきたすことがある。PITX2(4番染色体)およびFOXC1(6番染色体)の転写因子遺伝子変異が原因となり、50〜75%で緑内障を合併する。緑内障は乳児期より発症する場合もあるが、ほとんどが小児期〜若年期に発症する。
角膜中央混濁と角膜内皮・デスメ膜の欠損を特徴とする先天性疾患である。80%が両眼性で、虹彩角膜癒着や水晶体角膜癒着を伴うことがある。PAX6、PITX2、CYP1B1の変異が関連する。ピータース・プラス症候群では口唇裂、低身長、精神発達遅滞などの全身異常を伴い、B3GLCT遺伝子の変異(常染色体劣性)が原因である。重症例では角膜移植が必要となるが、水晶体角膜癒着を合併する場合の予後は不良である。
線維柱帯の発達異常を原因とする常染色体劣性疾患である。CYP1B1遺伝子(GLC3A座位、2p21)の変異が最も多い。日本では約10万人に1人の頻度で、75%が両眼性、65%が男児に発症し、80%が生後1年以内に発症する。乳幼児の高眼圧は角膜径の増大(牛眼)、角膜浮腫・混濁、デスメ膜破裂(Haab線条)を引き起こす。
虹彩低形成を主体とする常染色体優性疾患で、PAX6遺伝子(11番染色体)の変異が原因である。虹彩の部分的〜全周性の欠損に加え、水晶体脱臼、角膜混濁、黄斑低形成による視力障害を伴うことがある。隣接するWT1遺伝子の欠失を合併するとWAGR症候群(ウィルムス腫瘍・無虹彩症・泌尿生殖器異常・精神遅滞)のリスクがあり、WT1の評価が必要である。
その他の構成疾患①
先天遺伝性角膜内皮変性症(CHED):出生時〜1〜2歳頃に両眼対称性の角膜浮腫が出現する常染色体劣性疾患である。SLC4A11の変異が原因であり、眼圧上昇は認めない。
後部多形性角膜変性症(PPCD):角膜内皮およびデスメ膜の常染色体優性疾患である。角膜浮腫を呈するが角膜径の増大は伴わない。角膜内皮検査が診断に有用である。
その他の構成疾患②
強膜化角膜:不透明な強膜組織が周辺部角膜に非炎症性・非進行性に侵入し、角膜と強膜の境界が不明瞭となる。FOXE3、PAX6などの変異が関連する。
巨大角膜:角膜径12.5mm以上に拡大する疾患で、CHRDL1遺伝子の変異によるX連鎖劣性遺伝が多い。眼圧と内皮細胞は通常正常である。先天巨大角膜はHaab線条や乳頭陥凹拡大を認めない点でPCGと鑑別される。
発達緑内障の初発症状は眼圧上昇に伴う角膜上皮浮腫の刺激症状である。具体的には眼脂を伴わない流涙、羞明、眼瞼けいれんがみられる。高眼圧が持続すると角膜上皮浮腫が高度となり角膜混濁を生じる。さらに眼球被膜(特に角結膜移行部)が伸展され、角膜径の増大(牛眼)と前房深度の増加を呈する。
角膜が伸展されると弾性の低いデスメ膜に破裂が生じ(Haab線条)、角膜実質への前房水の流入により角膜浮腫・混濁が急速に増悪する。Haab線条は永久的な混濁を残し視力障害の原因となる。
| 所見 | 正常値・基準 |
|---|---|
| 新生児の角膜径 | 9.5〜10.5mm(生後1年で10.0〜11.5mm)。生直後に12.0mmを超える場合はPCGを疑う |
| 視神経乳頭陥凹比(C/D比) | 乳児では0.3以上で緑内障を疑う。左右差0.2以上も緑内障を示唆する |
各疾患に特徴的な前眼部所見を確認する。後部胎生環(シュワルベ線の前方転位・肥厚)はARSやアラジール症候群に伴う。虹彩低形成・多瞳孔症・虹彩偏位はARSに特徴的である。角膜中央混濁と虹彩角膜癒着はピータース異常を示唆する。
緑内障診療ガイドライン(第5版)では、以下の5項目のうち2つ以上を満たす場合に小児緑内障と診断される。
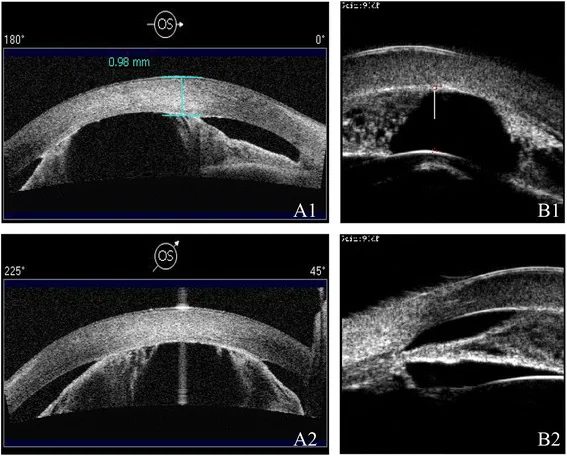
5歳以下の小児では催眠下あるいは全身麻酔下の検査が必要となることが多い。全身麻酔下では眼圧が覚醒時より低下するため、測定値の解釈に注意を要する。隅角検査は手持ち細隙灯とKoeppeレンズなどの直接型隅角鏡を用いる。角膜混濁で隅角鏡での観察が困難な場合には超音波生体顕微鏡(UBM)が有用である。
病型診断では前眼部所見により鑑別を行う。後部胎生環や虹彩異常(ARS)、白内障(ピータース異常)の有無を確認する。遺伝性が疑われる場合は血縁者の緑内障検査と遺伝子検査を検討する。
全身麻酔で用いられる薬剤はすべて眼圧を低下させる(唯一の例外はケタミンで軽度上昇させうる)。このため全身麻酔下の眼圧測定値のみでは緑内障を否定できない。可能な限り覚醒時の測定を行い、角膜径、Haab線条、視神経乳頭陥凹など眼圧以外の所見を総合的に評価することが重要である。
早発型発達緑内障は基本的に手術療法が必要な疾患であり、薬物療法は手術までの短期間の眼圧下降および術後の補助的治療として位置づけられる。患者が乳幼児であるため、再手術が必要となることも珍しくないことを保護者に十分説明し、理解を得ることが重要である。
初回手術としては隅角切開術(ゴニオトミー)や線維柱帯切開術(トラベクロトミー)が行われる。これらの手術は房水流出路の発達異常に直接介入する術式である。不成功の場合は濾過手術やチューブシャント手術が検討される。
眼圧がコントロールされた後も弱視治療が必要となる場合が多い。屈折性不同視、不正乱視、角膜混濁やHaab線条は弱視の原因となるため、術後も視力・屈折検査を定期的に行う。
角膜混濁が高度なピータース異常では角膜移植(全層角膜移植)が適応となるが、水晶体角膜癒着を合併する重症例では移植片不全のリスクが高い。
前眼部の発生において、表面外胚葉由来の角膜上皮・水晶体と、神経外胚葉由来の網膜色素上皮が、神経堤由来の間葉系細胞と相互作用することで正常な前眼部構造が形成される。神経堤細胞は角膜実質・角膜内皮、線維柱帯、虹彩実質などの形成に関与する。この遊走や分化の異常が前眼部形成異常を引き起こす。
50以上の遺伝子がASDAに関連していることが判明しているが、依然として40〜75%の症例で遺伝的原因が特定されていない。
| 遺伝子 | 染色体 | 関連疾患 | 遺伝形式 |
|---|---|---|---|
| PITX2 | 4q25 | ARS、ピータース異常 | 常染色体優性 |
| FOXC1 | 6p25 | ARS、虹彩隅角形成不全 | 常染色体優性 |
| PAX6 | 11p13 | 無虹彩症、ピータース異常 | 常染色体優性 |
| CYP1B1 | 2p21 | 原発先天緑内障 | 常染色体劣性 |
ARSではFOXC1とPITX2が物理的に相互作用し、神経堤細胞の正常な分化に不可欠であることが示されている。いずれの遺伝子の変異でも類似の表現型を生じうるのはこの相互作用による。
全例で確定できるわけではない。40〜75%の症例では現在のところ遺伝的原因が特定されていない。しかし、遺伝子検査は病型の鑑別(例:無虹彩症のPAX6変異と隣接するWT1遺伝子の評価によるWAGR症候群の除外)、家族内スクリーニング、遺伝カウンセリングに有用である。特にARSでは血縁者の50〜75%が緑内障を発症しうるため、遺伝子検査と家族の眼圧・緑内障検査が推奨される。
韓国の大規模研究では、受胎前3か月間および妊娠第1・第2三半期における母親の微小粒子状物質(PM2.5)への曝露増加が、子のASDリスク上昇と関連していることが報告されている。遺伝的要因に加え、妊娠中の感染症や催奇形性物質などの環境因子も正常な前眼部発生を阻害する可能性がある。