主な適応
眼内炎:細菌・真菌性の重篤な眼内感染症。
穿通性眼外傷:受傷後早期で修復不能な重篤外傷。
有痛性失明眼:麻薬鎮痛薬に抵抗する疼痛を伴う失明眼。
有痛性眼球癆:眼内腫瘍が否定されている場合に限る。
絶対緑内障:薬物・手術に抵抗する終末期緑内障。
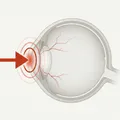
眼球内容除去術(evisceration)は、強膜殻・外眼筋付着部・眼窩付属器を温存しつつ、すべての眼球内容物(ぶどう膜・水晶体・硝子体・網膜)を除去する手術技法である。除去後の空洞内に眼窩インプラント(義眼台)を埋入し、眼窩容積を維持する。
歴史的には1817年にジェームズ・ベアー(James Bear)が駆出性出血後の処置として初めて報告した。19世紀後半にノイズ(Noyes)が眼内感染症治療として発展させ、ミューズ(Mules)が眼窩インプラント埋入を確立した。
眼外傷の疫学として、年間5500万件の眼外傷が世界で発生し、90%は予防可能とされる。眼外傷による失明は約1/100,000人/年と推計される1)。
強膜を外眼筋付きで温存したまま眼球内組織を除去する本術式は、強膜腔内にインプラントを挿入することで眼部陥凹が少なく、整容面において眼球摘出術よりやや有利である。インプラントを埋入しない場合でも眼球摘出術より陥凹が軽減される。なお、わが国では厚生労働省の認可を得た義眼台は存在しない。
除去術は強膜殻・外眼筋・眼窩付属器を温存し、眼球内容物のみを除去する。摘出術は眼球全体を摘出する。除去術の方が義眼可動性に優れ、手術侵襲も少なく整容面で有利である。詳細は「手術法の比較」の項を参照。
眼球内容除去術の適応となる眼は、ほぼ全例が失明状態である。主な自覚症状は以下の通りである。
眼球内容除去術の主な適応疾患は以下の通りである。
主な適応
眼内炎:細菌・真菌性の重篤な眼内感染症。
穿通性眼外傷:受傷後早期で修復不能な重篤外傷。
有痛性失明眼:麻薬鎮痛薬に抵抗する疼痛を伴う失明眼。
有痛性眼球癆:眼内腫瘍が否定されている場合に限る。
絶対緑内障:薬物・手術に抵抗する終末期緑内障。
禁忌
眼内悪性腫瘍:既知または疑いがある場合は絶対禁忌。ぶどう膜組織残存による腫瘍細胞播種リスクのため、眼球摘出術が推奨される。
眼球癆・小眼球症:相対的禁忌。インプラントを包むための強膜容積が不足する可能性がある。
外傷における選択基準として、強膜損傷やぶどう膜脱出が高度な場合は眼球摘出術を選択し、早期受診で顕微鏡下に修復可能な場合は除去術を選択する。
特殊な適応として、自己眼球損傷(Oedipism)がある。精神疾患を背景とした本疾患の年間発生数は約500例とされ、統合失調症・慢性うつ病が各約50%を占める。40〜50歳代に好発する1)。この場合、精神科・眼科・警察などの多職種連携が重要である。
除去術ではぶどう膜組織が残存するため、腫瘍細胞の眼窩への播種リスクがある。偶発的に発見される眼内腫瘍は13,591例中1.95%に及ぶとの報告がある。悪性腫瘍の疑いがある場合は眼球摘出術が推奨される。
術前評価として以下の検査が重要である。
全身麻酔・局所麻酔のいずれでも施行可能である。エピネフリン添加麻酔薬の球後注入により出血を軽減し術後疼痛を軽減できる。結膜下への局所麻酔薬注入(止血補助・テノン嚢との境界明瞭化)または術前10%フェニレフリン点眼も用いられる。
手技の概要は以下の通りである。
強膜バックルや緑内障ドレナージデバイスがある場合は除去する。シリコンオイルは周囲切開前に洗浄除去する。
主なインプラント素材を以下に示す。
| 地域 | 主な素材 |
|---|---|
| 日本 | PMMA(レジン球)・アクリル球・シリコーン球・自家骨片 |
| 欧米 | ハイドロキシアパタイト・メドボール・アルミナセラミック・多孔質ポリエチレン |
即時埋入と待機的(二次的)埋入の選好は術者によって異なる(眼形成外科医206名の調査では即時46%、二次的43%)。眼内炎67例の即時埋入での合併症率は12%であった。
必須ではないが、埋入により眼窩容積が保たれ眼部陥凹が軽減される。わが国では厚生労働省認可の義眼台が存在しないため、認可外使用となる現状がある。
コンフォーマ(仮義眼)は術直後から装着する。本義眼の調整は術後6〜8週で義眼師を受診して行う。オーダーメイド義眼は結膜囊が安定した後に作製する。術後2〜4週で疼痛・炎症が軽快してから開始するのが目安である。
除去術の利点
手術侵襲が少ない:手術時間が短く、術式が簡便で費用対効果が高い。
義眼可動性が良好:外眼筋・眼窩組織を温存するため、義眼の動きが自然になる。
感染管理が有利:眼内炎例で神経系への波及リスクが低い。
疼痛・麻酔リスクが低い:全身麻酔回避の可能性がある。
除去術の欠点
交感性眼炎リスク:術中にぶどう膜組織が曝露されるため理論上のリスクがある。ただし880例の調査で確定的な記録はない。
眼内腫瘍播種リスク:ぶどう膜組織残存による腫瘍細胞播種の可能性がある。
インプラント露出率:多孔質インプラントの露出率は除去術後0〜3.3%(摘出術後1.5〜21.6%)2)。
前向き研究(100名)では、強膜4分割+アロプラスチックインプラントの除去術とハイドロキシアパタイトインプラントの摘出術を比較し、除去術群でインプラント可動域が広くコストが低いことが示された。後方視的研究(摘出32例 vs 除去52例)でも除去術の方が可動性良好・術後合併症少であり、最終的な整容結果に有意差はなかった。
術中にぶどう膜組織が免疫学的に曝露されることで、対側眼に対する自己免疫反応(交感性眼炎)が生じる可能性が理論的に懸念される。しかし880例の調査では除去術後の交感性眼炎発症の確定的記録はない。また「14日以内に除去術を行えば交感性眼炎を予防できる」とする「14日ルール」に科学的根拠はないとされる。
術後創傷治癒において羊膜成分が注目されている。臍帯羊膜に豊富なHC-HA/PTX3複合体はIL-10を上方制御し、IL-12を下方制御することでマクロファージをM2(抗炎症)表現型に誘導し、抗炎症・抗瘢痕・組織再生を促進する2)。
小児では眼窩の発達に注意が必要である。5歳で眼窩容積は成人(14〜15歳で完成)の80%に到達し、出生〜思春期で眼球容積は3倍に増大する。骨への力学的刺激が眼窩成長に必須であるため、小児では適切なインプラント選択と長期フォローが重要である。
眼球内容除去術後の創離開(最も一般的な局所合併症の一つ)に対する新たな再建法として、臍帯羊膜の活用が報告されている。
Bunin(2022)は、増殖糖尿病網膜症を背景とした有痛性失明眼(51歳女性)に眼球内容除去術(最小16mmハイドロキシアパタイトインプラント埋入)を施行した後、術後に生じた結膜縫合部の離開に対し、ドナー強膜シェルと2.5×2.0cm AmnioGuard(Bio-Tissue社、マイアミ)を用いた再建を施行した2)。臍帯羊膜は通常の羊膜の約10倍の厚みを持ち、HC-HA/PTX3が豊富に含まれる。術後6週で良好な可動性、7週で義眼調整を完了し、8か月後も良好な整容結果が維持された。
除去術において後方強膜の背後にインプラントを配置する改良法(Longら)が報告されている。後方強膜切開後に視神経を切断し、強膜後方・前方フラップの背後に22〜23mmの大きなインプラントを配置する。前面を2層の強膜で被覆することで創離開・露出リスクを低減できるとされる。
除去術の一次移植において強膜前面リングとDFGを縫合する方法が報告されている。露出インプラントの代替として、特に5歳未満の小児では成長に伴い移植脂肪が増大する利点がある。
自己眼球損傷(Oedipism)を背景とした症例では、術後の精神医学的支援が転帰改善に寄与する。
Narangら(2021)は、統合失調症患者(58歳男性)の左眼自傷による3mm中心角膜穿孔・眼球内容自然脱出例に、ボールインプラントなしの眼球内容除去術+一期的閉鎖を施行した1)。さらなる自傷防止と交感性眼炎リスク低減を目的として除去術が選択された。術後5か月時点で精神状態良好・コンプライアンス維持を確認した。精神科・眼科・警察の多職種チームによる連携が重要と強調されている。