変性・萎縮性疾患

眼底自発蛍光(FAF)
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. 眼底自発蛍光とは
Section titled “1. 眼底自発蛍光とは”眼底自発蛍光(Fundus Autofluorescence; FAF)は、眼底に存在する天然蛍光物質(fluorophores)を光で励起し、その発光をマッピングする非侵襲的画像診断法である7)。フルオレセイン蛍光造影(FA)と異なり、造影剤の静脈注射を必要としない7)。
1995年、Deloriらがin vivoでヒト網膜の固有蛍光特性を初めて報告した7)。その後、共焦点走査型レーザー検眼鏡(cSLO)の普及により臨床応用が急速に広まった。
主な蛍光物質
Section titled “主な蛍光物質”FAFの主要な蛍光団(fluorophore)はRPE細胞内に蓄積するリポフスチン(lipofuscin; LF)である7)6)。LFは視細胞外節ディスク膜の不完全なライソゾーム分解により生成される副産物であり、少なくとも20種のビスレチノイド化合物を含む7)。
主要成分であるA2E(N-レチニリデン-N-レチニルエタノールアミン)は青色光(ピーク約470 nm)を吸収し、黄緑色光(600〜610 nm)を放出する6)7)。A2Eは光酸化により活性酸素種(ROS)を生成し、膜の不安定化やアポトーシスを誘発する7)。
各ビスレチノイドの吸収極大は以下の通りである7):
| 蛍光物質 | 吸収極大 |
|---|---|
| A2E | 439 nm |
| A2PE | 449 nm |
| isoA2E | 426 nm |
| A2-DHP-PE | 490 nm |
RPE細胞は生涯で約30億個の視細胞外節ディスクを貪食する6)。70歳以降にはLFとメラノリポフスチンがRPE細胞質容積の約25%を占めるまで蓄積する6)。
近赤外自発蛍光(NIR-AF)では787 nm前後の光でメラニンを主蛍光物質として励起する7)6)。これによりRPEおよび脈絡膜のメラニン分布を評価できる。
FAは造影剤の静脈注射が必要であり、血管構造や血液網膜関門の状態を評価する。FAFは造影剤不要で、RPE内リポフスチンの固有蛍光を利用してRPEの代謝状態を評価する。FAFの信号強度はFAの約100分の1と微弱だが、RPE障害を直接反映する点で補完的な情報が得られる7)。
2. 適応と臨床的意義
Section titled “2. 適応と臨床的意義”FAFは多岐にわたる網膜・脈絡膜疾患の診断・経過観察に用いられる。
血管・代謝性疾患
糖尿病網膜症(DR):硬性白斑は過蛍光、出血は低蛍光、嚢胞様黄斑浮腫(CME)は過蛍光を呈し、早期変化の検出に有用。
中心性漿液性脈絡網膜症(CSC):遷延例では点状過蛍光から全体過蛍光、さらに部分的低蛍光へと段階的に変化する。
炎症性・腫瘍性疾患
GA周囲FAFパターンと進行速度
Section titled “GA周囲FAFパターンと進行速度”GAの進行予測にはIFAG(International FAF Classification Group)分類が用いられ、8パターンに分類される(normal, minimal change, focal increase, patchy, linear, lace-like, reticular, speckled)6)。
各パターンの進行速度を以下に示す3)6):
| パターン | 特徴 | 進行速度(mm²/年) |
|---|---|---|
| None/minimal | 境界部変化なし | 最遅 |
| Diffuse trickling | 広範な点状高蛍光 | 約2.61 |
| Patchy/banded | 斑状・帯状 | 中等度 |
GA部位の低蛍光はRPE喪失を示し、周囲の高蛍光はRPE肥大・脱落RPEの遊走・マクロファージの集積を反映する3)。
Reticular pseudodrusen(網状偽ドルーゼン)はFAFで50〜400 μmの低蛍光斑として検出され、カラー眼底写真よりも感度が高い6)。
地図状萎縮(GA)の進行モニタリング、Stargardt病の蛍光定量(qAF)、網膜色素変性(RP)の高蛍光リング収縮評価が特に有用である。いずれも構造変化をOCT・FAよりも早期に捉えられる場合がある。詳細は「4. 正常所見と異常所見の読み方」を参照。
3. 検査手順と撮影方法
Section titled “3. 検査手順と撮影方法”FAF撮影には大きく3種類の装置が使用される。
cSLO型
共焦点走査型レーザー検眼鏡:共焦点ピンホールで焦点外光を遮断し、水晶体蛍光の影響が少ない7)6)。
Spectralis(Heidelberg):488 nm青色レーザー、>500 nmバリアフィルタ、15〜55度。OCT同時撮影・NIR-AF対応7)。
Nidek Mirante:490 nm励起、40〜60度7)。
眼底カメラ型
白色フラッシュ+バンドパスフィルタ:広視野の撮影が可能。
Topcon TRC-50DX:500〜610 nm / 535〜585 nm(Spaideフィルタ)励起7)。
Zeiss Clarus:青色光FAF(BLFI)、435〜585 nm励起、133〜200度対応7)。
超広角型
Optos(Natus):532 nm緑色レーザー、200度の超広角撮影。無散瞳(最小瞳孔径2 mm)で使用可能7)6)。
末梢病変の検出:通常の眼底カメラでは捉えられない周辺網膜病変の評価に有用。
主要装置の仕様比較
Section titled “主要装置の仕様比較”各装置の仕様を以下に示す7):
| 装置 | 励起波長 | 画角 |
|---|---|---|
| Spectralis | 488 nm | 15〜55度 |
| Optos | 532 nm | 200度 |
| Zeiss Clarus | 435〜585 nm | 133〜200度 |
標準的なB-FAF(青色光FAF)撮影では、患者の瞳孔を散瞳した後(または無散瞳で)装置に固定し、ライブ画像を確認しながら最良焦点で撮影する。cSLO型では複数フレームの平均加算処理によりS/N比を向上させる。
光退色(photobleaching)処理:撮影前に約20秒間の強光曝露を行うことで視物質を退色させ、FAF信号を約30%増強できる2)1)。MEWDS等の急性期病変の評価に活用される。
緑色光FAF(G-FAF):504/532 nm励起で撮影する方式であり、黄斑色素による吸収が少なく中心窩の評価に優れる4)6)。患者の快適性も高い。
外来での標準検査にはcSLO型(Spectralis等)が広く普及している。超広角撮影にはOptos、中心窩評価にはG-FAF対応機器が選択される。OCTと同時撮影が可能なcSLO型は経過観察での位置合わせ精度が高く、GA面積計測などの定量評価に適している4)7)。
4. 正常所見と異常所見の読み方
Section titled “4. 正常所見と異常所見の読み方”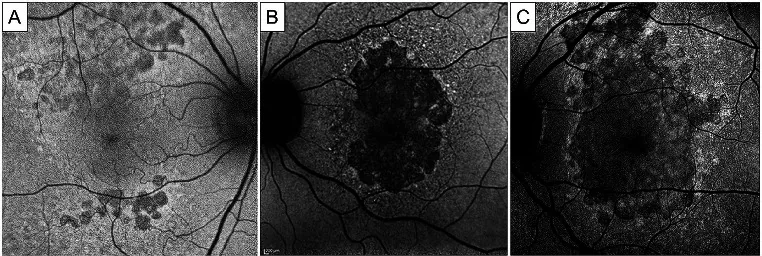
SW-AF(短波長FAF・B-FAF)での正常所見:
- 中心窩低蛍光:キサントフィル色素(黄斑色素)が青色光を吸収するため、中心窩は低蛍光を示す6)7)。
- 視神経乳頭低蛍光:RPEが存在しないため低蛍光となる7)。
- 網膜血管低蛍光:血液が光を吸収するため低蛍光を示す7)。
- 最強蛍光域:中心窩から5〜15度の傍中心窩が最も強い蛍光を示す6)。
NIR-AF(近赤外自発蛍光)での正常所見:
中心窩はメラニン密度が高いため、NIR-AFでは逆に過蛍光として描出される6)7)。これはSW-AFとの重要な違いである。
異常所見の読み方
Section titled “異常所見の読み方”過蛍光・低蛍光の原因と代表疾患を以下に示す7)1)2):
| パターン | 主な原因 | 代表疾患 |
|---|---|---|
| 過蛍光 | LF蓄積・黄斑色素消失・網膜下蛍光物質 | Stargardt病・MEWDS・GA周囲 |
| 低蛍光 | RPE萎縮・出血遮蔽・線維化 | GA・出血・瘢痕 |
過蛍光のメカニズム分類:
過蛍光の発生機序は一次的上昇と二次的上昇に分類される2)。
- 一次的上昇:ABCA4・RDH12の機能異常によりビスレチノイドが過剰に生成される。Stargardt病・RDH12関連網膜ジストロフィに相当する。
- 二次的上昇:視細胞障害を契機に下流でビスレチノイドが蓄積する。RPや他の原因による視細胞死に続発する。
光退色との鑑別:過蛍光がphotobleaching処理後に消失する場合、視物質(ロドプシン)の蛍光による偽過蛍光の可能性がある1)。
黄斑色素の減少(加齢・太陽光曝露)や光退色(photobleaching)でも過蛍光が出現しうる。OCTと併用して構造変化の有無を確認し、真の病的過蛍光との鑑別を行う。また装置間での見え方が異なる場合があるため、経時比較には同一装置を使用することが重要である4)7)。
5. 注意点と限界
Section titled “5. 注意点と限界”6. 技術的原理(リポフスチン・メラニン・蛍光団)
Section titled “6. 技術的原理(リポフスチン・メラニン・蛍光団)”蛍光の物理学的基礎
Section titled “蛍光の物理学的基礎”蛍光とは、光子を吸収した分子が励起状態から基底状態に戻る際に低エネルギーの光子を放出する現象である7)。放出光は常に吸収光より長波長(低エネルギー)となる(ストークスシフト)。
リポフスチンの生化学的形成過程
Section titled “リポフスチンの生化学的形成過程”LFの主要成分A2Eの形成経路は以下の通りである7)2):
- 11-cis-レチナールの光異性化:光受容で all-trans-レチナールが生成される。
- ホスファチジルエタノールアミン(PE)との反応:all-trans-レチナールがPEと縮合してN-レチニリデン-PE(NRPE)を形成する。
- NRPE→A2-GPE:ディスク膜内でNRPEが2分子目のall-trans-レチナールと反応し、A2-GPE(A2E前駆体)を形成する。
- A2-GPEの加水分解→A2E:RPEによるディスク膜貪食後、ライソゾームでA2-GPEが加水分解されA2Eが生成される。
ABCA4の役割:ABCトランスポーターABCA4はNRPEをディスク膜の細胞質面に輸送し、all-trans-レチノールへの還元を促進する2)。ABCA4機能欠損(Stargardt病の原因)では、NRPEがディスク膜内に留まりビスレチノイドの過剰蓄積をきたす。
メラニンとNIR-AF
Section titled “メラニンとNIR-AF”メラニンはNIR-AF(787 nm励起)の主要蛍光物質であり、RPEおよび脈絡膜に分布する7)6)。加齢によるメラニン減少はNIR-AF信号の減弱として観察される。メラノリポフスチン(メラニンとLFの複合体)もNIR-AF信号に寄与する。
蛍光定量(qAF)
Section titled “蛍光定量(qAF)”qAFは488 nm励起下で内部蛍光参照(キュベット内の標準蛍光物質)を用いて補正した定量的蛍光値である2)7)。qAF値は年齢・偏心度・性別・人種によって変動し、標準化が課題となっている。
蛍光寿命イメージング(FLIO)
Section titled “蛍光寿命イメージング(FLIO)”FLIOは各蛍光物質固有の蛍光減衰曲線(寿命)を計測する技術であり、蛍光強度だけでなく蛍光物質の種類を識別できる6)7)。現時点では研究用途が中心である。
7. 最新の研究と今後の展望
Section titled “7. 最新の研究と今後の展望”qAFの臨床試験エンドポイントへの応用
Section titled “qAFの臨床試験エンドポイントへの応用”qAFはStargardt病・RPなどの遺伝性網膜疾患において、疾患進行の客観的指標として臨床試験のエンドポイントに採用されつつある2)。校正された装置と測定プロトコールの標準化が課題である。
GA治療薬試験でのFAFの役割
Section titled “GA治療薬試験でのFAFの役割”pegcetacoplan(APL-2)およびavacincaptad pegol(Zimura)を用いたGA治療の臨床試験では、FAF画像によるGA面積計測が主要エンドポイントとして採用されている4)。B-FAFはGA面積を過大評価する傾向があり、G-FAFの方が中心病変の評価に優れることも報告されている4)。
AI・深層学習による自動解析
Section titled “AI・深層学習による自動解析”Optos超広角FAF画像と深層学習アルゴリズムを組み合わせた加齢黄斑変性検出モデルが報告されており、高感度での早期病変検出が可能とされている6)。
遺伝性網膜疾患の自動分類では、ニューラルネットワークがStargardt病・Best病・RPを約95%の精度で識別したと報告されている5)。
G-FAFの臨床応用拡大
Section titled “G-FAFの臨床応用拡大”G-FAFは中心窩黄斑色素の影響が少なく、SW-AFで観察困難な中心窩病変の検出に優れる4)。患者の眩しさも少なく、快適性の点でも有利である。今後の普及が期待される。
FLIOの臨床応用
Section titled “FLIOの臨床応用”蛍光寿命イメージング(FLIO)は加齢黄斑変性・Stargardt病・糖尿病黄斑症などで疾患固有の蛍光寿命パターンを示し、強度ベースのFAFに先行して代謝変化を捉えられる可能性がある7)。
マルチモーダルイメージング統合
Section titled “マルチモーダルイメージング統合”FAF・OCT・OCT-A・FAを統合したマルチモーダルイメージングにより、各検査法の限界を補完し合う診断体制が構築されつつある4)。
qAFの標準化による定量的疾患モニタリング、AI・深層学習による自動診断(遺伝性網膜疾患で約95%の精度)、FLIOの臨床応用、G-FAFの普及が主な展望である5)6)。GA治療薬の臨床試験でFAFが主要エンドポイントに採用されており、今後の網膜診療における重要性はさらに高まると見込まれる4)。
8. 参考文献
Section titled “8. 参考文献”- Mantovani A, Corbelli E, Sacconi R, et al. Blue-light fundus autofluorescence in inflammatory photoreceptor diseases. Diagnostics. 2023;13(14):2466.
- Parmann R, Bhatt M, Sarraf D, et al. Primary versus secondary autofluorescence elevations in inherited retinal dystrophies. Int J Mol Sci. 2023;24(15):12327.
- Curcio CA, Meleth AD, Gelman R, et al. FAF variation in geographic atrophy: clinicopathologic correlation. Invest Ophthalmol Vis Sci. 2025;66(1):49.
- Ranetti AE, Ranetti MO, Pop A, et al. Blue-light and green-light fundus autofluorescence in age-related macular degeneration. Diagnostics. 2025;15(13):1688.
- Oh J, Lee CS, Kim JM, et al. Fundus autofluorescence in inherited retinal disease. J Clin Med. 2025;14(7):2293.
- Sahinoglu Kekek E, Sermet F. Fundus autofluorescence in dry age-related macular degeneration. Turk J Ophthalmol. 2021;51(3):169-176.
- Pole C, Ameri H. Fundus autofluorescence and clinical applications. J Ophthalmic Vis Res. 2021;16(3):432-461.
