適合型
定義:視細胞外節とRPE(網膜色素上皮)の間に分離を認めない型。
特徴:陥凹内で視細胞とRPEが密着したまま落ち込む。比較的安定した経過をとる場合が多い。
OCT所見:陥凹部のRPEと光受容体層が一体となって脈絡膜側へ変位する。

限局性脈絡膜陥凹(Focal Choroidal Excavation; FCE)は、光干渉断層計(OCT)で検出される脈絡膜の限局的な陥凹性変化である。後部ぶどう腫や強膜拡張を伴わない点が特徴である。2006年にJampolが初めて報告し、2011年にMargolisらによって命名された。
FCEの形態は大きく2型に分類される。
適合型
定義:視細胞外節とRPE(網膜色素上皮)の間に分離を認めない型。
特徴:陥凹内で視細胞とRPEが密着したまま落ち込む。比較的安定した経過をとる場合が多い。
OCT所見:陥凹部のRPEと光受容体層が一体となって脈絡膜側へ変位する。
非適合型
定義:視細胞外節とRPEの間に隙間(サブ網膜液や高反射物質)を認める型。
特徴:黄斑新生血管(脈絡膜新生血管)や漿液性網膜剥離の合併リスクが高い。
OCT所見:陥凹内のRPEと光受容体層の間に液体貯留または高反射物質を認める。
形状による分類(円錐型・おわん型・混合型)および部位による分類(中心窩型・中心窩外型)も用いられる。
Capellanらは病因に基づき3型に分類した。type 1(近視性)・type 2(先天性)・type 3(後天性/炎症性)である。type 3ではCNV(脈絡膜新生血管)合併率が40%に達する7)。
40歳未満での有病率は0.18%(1697眼中3眼)とされる1)。中心性漿液性脈絡網膜症(CSC)患者でのFCE有病率は2.8〜7.8%と一般人口より高い1)。OCT検査の普及とともに検出例が増加している。
近年、FCEはパキコロイド(pachychoroid)疾患スペクトラムから除外される方向にある。炎症によるBruch膜欠損と限局性脈絡膜菲薄化の結果として生じる独立した病態と位置づけられている8)。
40歳未満での有病率は0.18%と低いが、OCT検査の普及に伴い偶発的に発見される例が増加している1)。多くは無症状であり、眼底検査やOCT検査の際に初めて気づかれる。
多くは無症状で、OCT検査時に偶発的に発見される。有症状例では以下を呈する。
FCEの32例シリーズでは60〜77%の症例が何らかの視覚障害を訴えた。
無症状かつ黄斑新生血管や漿液性網膜剥離を伴わない場合は経過観察が基本である。ただし黄斑新生血管の合併リスクがあるため、定期的なOCT・OCTA検査によるモニタリングが推奨される(詳細は「標準的な治療法」の項参照)。
FCEの発症機序は完全には解明されておらず、複数の仮説が提唱されている。
FCEと関連する主な疾患・リスク因子を以下に示す。
| カテゴリ | 疾患・因子 | 備考 |
|---|---|---|
| 遺伝性眼疾患 | Best病 | 6%にFCE合併3) |
| 遺伝性眼疾患 | ABCA4関連網膜症 | 進行性深化の報告7) |
| 全身疾患 | Alagille症候群 | JAG1遺伝子変異6) |
| 脈絡膜疾患 | 中心性漿液性脈絡網膜症/ポリープ状脈絡膜血管症 | 有病率2.8〜7.8%1) |
| 生活習慣 | 喫煙 | 酸化ストレス→Bruch膜欠損4) |
その他のリスク因子として、近視・女性・アジア人への偏りが知られている。両眼性は18例中7例(38.89%)に認められた1)。
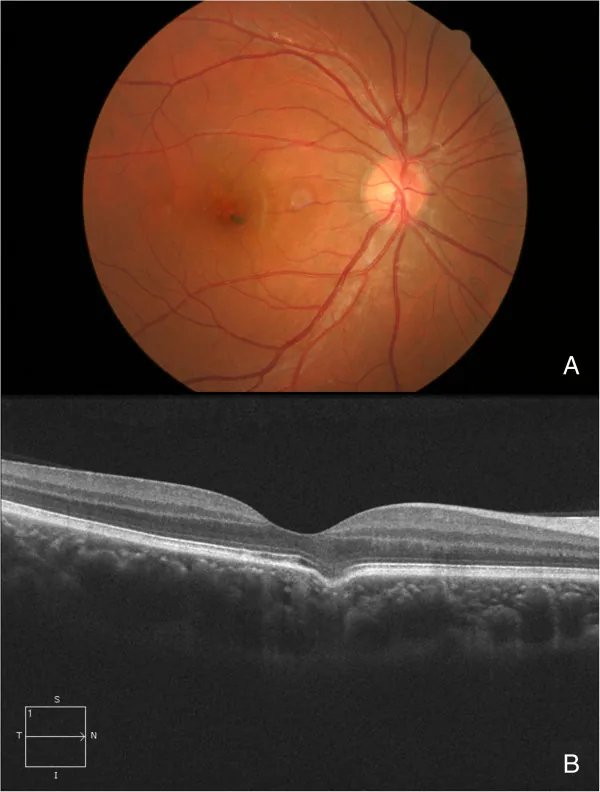
FCEの診断にはOCTが不可欠である。以下の検査を組み合わせて診断・評価を行う。
OCT
役割:診断のゴールドスタンダード。
所見:脈絡膜の限局的陥凹。適合型と非適合型の判別が可能。形状(円錐型・おわん型・混合型)や深さの計測も行う。
OCTA
役割:非侵襲的な黄斑新生血管検出。造影剤なしで診断可能2)。
所見:FCE領域の脈絡膜毛細血管層に暗調フローシグナルvoid area。黄斑新生血管合併時はflower-like net状の新生血管が描出される2)。
FA・ICGA
FA所見:後期過蛍光(leakage / staining)。CNV・RPE変性の評価に有用5)。
ICGA所見:脈絡膜血管構造の評価。パキコロイドや拡張脈絡膜血管の評価に有用4)。
その他の補助的検査として、FAF(RPE健康状態の評価)やBモード超音波(後部ぶどう腫との鑑別)を用いることがある。
以下の疾患との鑑別が重要である。
無症状で黄斑新生血管や漿液性網膜剥離を伴わない例は定期的な経過観察が基本方針である。生涯にわたるOCT・OCTAモニタリングが推奨される1)。
FCEにCSCが合併した両眼例において、focal laser(スポットサイズ50μm、出力70mW、照射時間0.1秒)とSML(Subthreshold Micropulse Laser)の組み合わせで、5ヶ月後に漿液性網膜剥離が消失した報告がある1)。
黄斑新生血管を合併した例には抗VEGF療法が第一選択である。主な治療成績を以下に示す。
| 報告 | 薬剤 | 治療結果 |
|---|---|---|
| Duke 20252) | Bevacizumab 1.25mg/0.05mL | 3回投与で20/40→20/20 |
| Sato 20214) | Aflibercept 月1回×3ヶ月 | CNV消失+FCE消失、12ヶ月再発なし |
| 文献集計4) | 抗VEGF全般 | 76眼中54眼(71%)が良好な解剖学的応答 |
Duke RCTら(2025)は30歳女性の中心窩下黄斑新生血管合併FCE例にBevacizumabを3回投与し、OCTA上のflower-like net状黄斑新生血管が退縮してBCVA 20/40から20/20への改善が得られたと報告した2)。
Satoら(2021)はAflibercept月1回3ヶ月投与後にCNV消失とともにFCEそのものが消失した症例を報告した4)。12ヶ月観察でCNV・FCEとも再発を認めなかった。FCE消失は抗VEGF後の線維血管瘢痕がBruch膜欠損部を架橋したためと推察されている。
抗VEGF療法は有効であり、76眼中54眼(71%)で良好な解剖学的応答が得られたと報告されている4)。一部の症例ではFCE自体が消失することもある4)。ただし再発リスクがあるため、治療後も継続的なモニタリングが必要である。
現在最も支持されているのはBruch膜欠損仮説である。Bruch膜の脆弱化・欠損部位において、眼内圧(IOP)の作用でRPE・Bruch膜複合体の外層が外方に突出する。その際、内境界膜(ILM)は偏位しない。これがOCTで観察されるFCEの形態的特徴に一致する4)。
Bensonら(2022)はABCA4関連網膜症患者において8年間の連続OCTで以下の経過を記録した7)。
この観察は適合型と非適合型がスペクトラム上に存在し、段階的に進行しうることを示す直接的証拠である7)。
OCTA解析では、FCE領域の脈絡膜毛細血管層に暗調フローシグナルvoid areaが認められる1)。これはFCE部位の脈絡膜毛細血管の血流低下を示唆し、局所的な虚血が炎症・Bruch膜脆弱化・黄斑新生血管形成へとつながる可能性がある2)。
脈絡膜陥凹→局所的脈絡膜菲薄化→虚血・慢性炎症→Bruch膜脆弱化→黄斑新生血管という経路が推定されている2)。type 3 FCEではCNV合併率が40%に達することが報告されており7)、FCEの型分類が臨床的なリスク評価に重要である。
Alagille症候群(AGS)はJAG1遺伝子変異(97%以上)を病因とする多臓器疾患である。Notchシグナル経路の異常による脈絡網膜萎縮を背景に、FCEと黄斑円孔が合併することが報告されている6)。
従来FCEはパキコロイド疾患スペクトラムに含まれることもあったが、近年の大規模レビューによって再分類が進んでいる。Cheungら(2024)はFCEをパキコロイド疾患スペクトラムから除外し、炎症によるBruch膜欠損と局所的脈絡膜菲薄化を病因とする独立した病態として位置づけることを提唱した8)。
BensonらはABCA4関連網膜症のFCEを8年間にわたって連続OCTで追跡し、適合型FCEが非適合型へと移行し最終的に黄斑円孔に至る自然経過を世界で初めて文書化した7)。この観察はFCEの進行性を理解するうえで重要な知見である。
OCTA(光干渉断層血管造影)とSD-OCT(スペクトラル・ドメインOCT)を組み合わせることで、造影剤(フルオレセイン、ICGA)を用いずにFCE合併黄斑新生血管を診断できることが報告された2)。侵襲的造影検査への依存を低減する可能性がある。
Satoら(2021)はAflibercept投与後にFCEそのものが消失した初の報告を行った4)。線維血管瘢痕によるBruch膜欠損の架橋がFCE消失のメカニズムとして推察されており、抗VEGF療法がFCEの形態的変化にも影響する可能性が示された。
Capellanらによる3型分類(type 1: 近視性、type 2: 先天性、type 3: 後天性/炎症性)は、リスク評価・治療方針決定に有用なフレームワークとして注目されている7)。今後の前向き大規模研究による検証が期待される。
大部分のFCEは安定した経過をたどるが、黄斑新生血管合併率は長期観察で約16%と報告されている2)。ABCA4関連網膜症などの進行性網膜変性を背景に持つ例では、適合型から非適合型へ段階的に深化し、黄斑円孔に至った報告もある7)。生涯にわたるモニタリングが推奨される1)。