イールズ病は周辺部網膜 の特発性閉塞性血管炎で、若年男性に好発する。
再発性の硝子体出血 が主な臨床像であり、突然の視力 低下・飛蚊症 を引き起こす。
最大87%が両側性であり、経過中に反対眼も罹患しうる。
結核菌蛋白への過敏反応が最有力の病因とされるが、培養では菌は検出されない。
炎症期・虚血期・増殖期の3段階で進行し、病期に応じた治療が必要となる。
炎症期にはステロイド 全身投与、虚血期にはレーザー光凝固 が主体となる。
適切な治療により良好な視力予後が期待できるが、治療が遅れると牽引性網膜剥離 や血管新生緑内障 に至ることもある。
イールズ病(Eales disease)は、1880年に英国の眼科医Henry Ealesが健康な若年男性における再発性硝子体出血として初めて報告した疾患である。特発性の閉塞性網膜血管炎 であり、周辺部網膜の静脈周囲炎・血管閉塞・新生血管 を特徴とする。
発生頻度は地域差が大きい。北米では稀な疾患であるが、インド・中東・アジアなど結核感染率の高い地域では比較的多く認められる1) 。20〜30歳代の男性に好発し、男女比は約20:1と男性優位である。最大87%の症例で両側性を示す1) 。
他の網膜血管炎・全身性疾患・糖尿病を除外した後に診断が確定する除外診断疾患である。
Q イールズ病はどのくらいまれな疾患か?
A 北米では非常に稀であるが、インドや中東など結核流行地域では比較的多く認められる1) 。男女比は約20:1で男性に著しく偏り、最大87%が両側性を示す。
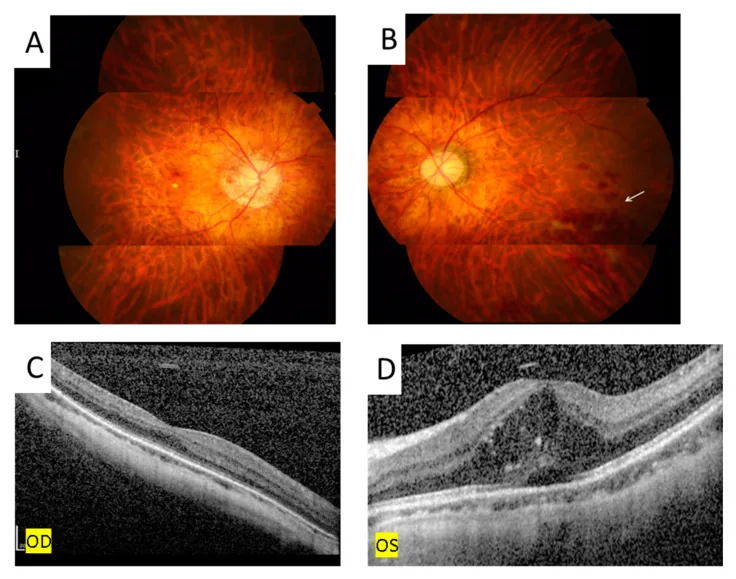
Eales Disease image Ping-Ping Meng; Chun-Ju Lin; Ning-Yi Hsia; Chun-Ting Lai; Henry Bair; Jane-Ming Lin; Wen-Lu Chen; Yi-Yu Tsai. Use of Ultra-Widefield Fluorescein Angiography to Guide the Treatment to Idiopathic Retinal Vasculitis, Aneurysms, and Neuroretinitis—Case Report and Literature Review. Medicina (Kaunas). 2022 Oct 16; 58(10):1467. Figure 5. PMCID: PMC9611749. License: CC BY.
Fundus photography showed retinal hemorrhage ((B), arrow) and OCT disclosed subretinal and intraretinal fluid with hyperreflective material over the left eye (D). There is no retinal hemorrhage (A) nor macular edema (C) over the right eye.
病初期は無症状であることが多く、周辺部の静脈周囲炎の段階では自覚症状を欠く。病状の進行とともに以下の症状が出現する。
飛蚊症 :硝子体出血による急性発症の浮遊感。突然の光視症 を伴うこともある1) 。霧視 4) 。視力低下 :硝子体出血・黄斑浮腫 ・牽引性網膜剥離により生じる。
イールズ病は炎症期・虚血期・増殖期の3段階で進行する1) 。
炎症期
周辺部静脈周囲炎 :周辺部網膜静脈に沿った白鞘形成。血管周囲の炎症細胞浸潤。
網膜出血 :周辺部の点状・火炎状出血。
FA での静脈漏出
虚血期
毛細血管無灌流 :周辺部の広範な無灌流領域 形成。
動静脈シャント :虚血に対する代償的な血管変化。
静脈数珠状変化 :静脈の不規則な拡張と狭窄の交互出現。
増殖期
新生血管(sea-fan様) :虚血領域に隣接して発生する増殖性新生血管。
硝子体出血 :新生血管の破綻による反復性出血。
牽引性網膜剥離(TRD) :線維血管増殖膜 による牽引。混合性網膜剥離 ・血管新生緑内障・白内障 ・視神経萎縮 に至ることもある4) 。
Saxena分類では病期をIa〜IVbの7段階に細分化する。Ia/Ibは周辺部静脈炎、IIaは虚血・無灌流、IIbは新生血管出現、IIIa/IIIbは硝子体出血の程度、IVa/IVbはTRDの範囲による分類である。
黄斑浮腫は58.2%の症例で認められ4) 、視力予後に直結する重要な合併症である。
なお蛍光眼底造影(FA)では活動性炎症での静脈漏出、慢性硬化期での壁染色、無灌流領域の広さを評価できる。
原因は未解明であり特発性とされるが、結核菌蛋白への過敏反応が最有力の病因説である。
結核との関連 :網膜前膜 の50〜70%からMycobacterium tuberculosisのMPB64遺伝子がPCRで検出される。しかし菌培養は陰性であり、非生存菌またはDNA断片への免疫学的過敏反応が発症機序と考えられる3) 。VEGFの関与 :硝子体 中にVEGF・IL-6・IL-8・MCP-1が高濃度で検出され、病的血管新生を促進する3) 。免疫学的素因 :HLA-B5・DR1・DR4との関連、低グルタチオン、C3補体 変化が報告されている4) 。凝固異常 :第V因子Leiden変異ヘテロ接合体では血栓リスクが約7倍増加し、血管閉塞の一因となりうる4) 。コカインの関与 :コカイン乱用が免疫学的トリガーとなりイールズ病を発症した症例報告がある4) 。
結核流行地域に在住または渡航歴がある場合、結核スクリーニング(QuantiFERON、マントー試験)を受けることが推奨されます。
コカイン等の薬物使用は網膜血管障害のリスク因子となりえます4) 。
飛蚊症の増加や突然の視力低下が生じた場合は、速やかに眼科を受診してください。
Q イールズ病と結核の関係はどのようなものか?
A 網膜前膜の50〜70%でMycobacteriumのPCR陽性が報告されているが、培養では菌は検出されない3) 。生きた菌による直接感染ではなく、非生存菌またはDNA断片に対する免疫学的過敏反応が発症機序と考えられている。このためマントー試験陽性例では抗結核薬の併用が推奨される。
イールズ病は除外診断である。他の網膜血管炎・全身疾患を除外した上で診断を確定する1) 。
主な検査所見を以下に示す。
検査項目 目的・除外対象 QuantiFERON/マントー 結核感染の評価 ANA/ANCA/抗dsDNA抗体 SLE ・血管炎血清ACE/リゾチーム サルコイドーシス 血糖/HbA1c 糖尿病網膜症 血液検査(CBC、凝固系) 鎌状赤血球・凝固異常 梅毒血清反応/ライム病 感染性血管炎
蛍光眼底造影(FA) :最重要検査。静脈漏出(活動性炎症)・壁染色(硬化)・無灌流領域の範囲を評価する。治療適応の判断と光凝固の照射領域決定に不可欠である。OCT :黄斑 病変の評価。黄斑浮腫・黄斑前膜・牽引性網膜剥離の有無と程度を把握する。眼底検査 ・硝子体手術 記録
鑑別疾患としては糖尿病網膜症、網膜静脈分枝閉塞症 (BRVO )、Coats病、サルコイドーシス、SLE、鎌状赤血球網膜症 、ベーチェット病 などが挙げられる1) 4) 。
Q イールズ病はどのように診断するのか?
A 除外診断であり、糖尿病・サルコイドーシス・SLEなどの全身疾患を血液検査・画像検査で除外した後に診断する1) 。蛍光眼底造影(FA)が最も重要な検査であり、周辺部静脈周囲炎・無灌流領域・新生血管の分布を確認する。
治療は病期に応じて選択する。病期別の主な治療を以下に示す。
病期 主な治療 補助治療 炎症期 経口ステロイド ATT(マントー陽性時) 虚血期 網膜光凝固(PRP ) 抗VEGF注射 増殖期 硝子体手術・光凝固 抗VEGF注射
経口ステロイドが第一選択である。プレドニゾン40mg/日から開始し漸減する方法が用いられる1) 。デキサメタゾン1mg/kg/日4か月漸減投与により最終視力20/20を達成した報告もある4) 。Biswasら(500例898眼)の大規模報告では、急性炎症期のステロイド投与により視力が有意に改善したことが示されている2) 4) 。
黄斑浮腫(CME )にはデキサメタゾンインプラント(オザデックス)の硝子体内注射 が有効である2) 。
マントー試験陽性例には抗結核薬を併用する。RIPE(リファンピシン・イソニアジド・ピラジナミド・エタンブトール)4剤を4か月、その後イソニアジド単独で5か月の計9か月投与が行われる2) 3) 。結核感染が示唆された場合のATT開始アルゴリズムとして国際コンセンサス(COTSガイドライン)が参考にされる2) 。
網膜光凝固(PRP) :虚血期の主軸治療。セクター別光凝固で89%以上の新生血管退縮が報告されている。1例では3回の汎網膜光凝固により新生血管が退縮した1) 。ステロイドと光凝固の相乗効果が期待できる1) 。抗VEGF硝子体内注射 :ベバシズマブ により新生血管退縮・硝子体出血吸収促進が期待できる。ただしTRD形成を促進するリスクがある3) 。ラニビズマブ 無効例にアフリベルセプト (VEGF-A・B・PlGFを結合)を使用し、長期間(43か月・28か月)にわたり20/25〜20/20を維持した症例報告がある3) 。硝子体手術(PPV ) :3か月以上持続する硝子体出血、または黄斑を脅かすTRDが適応となる。33年間のフォローアップでも20/20の視力が維持された報告がある2) 。
全身ステロイド投与中にマントー陽性が判明した場合はATTの併用が必要である。
ベバシズマブはTRD形成を促進するリスクがあり、増殖性変化が強い症例では特に注意が必要である3) 。
ステロイドと光凝固を組み合わせることで相乗的な効果が期待できるが、治療の順序と病期の判断が重要である1) 。
Q イールズ病の視力予後はどうか?
A 適切な治療を早期に行うことで良好な視力予後が期待できる。硝子体手術後33年間にわたり20/20の視力が維持された報告もある2) 。一方、治療が遅れると牽引性網膜剥離・血管新生緑内障・白内障・視神経萎縮に至ることもある4) 。
イールズ病の病態は、周辺部静脈周囲炎を起点とした段階的な進行過程で理解される1) 2) 。
第1段階(炎症) :周辺部網膜静脈に沿った炎症細胞浸潤と静脈周囲炎が発生する。結核菌PCRは網膜前膜の50〜70%で陽性を示すが、培養では菌は検出されない3) 。非生存菌またはDNA断片が宿主の免疫系を活性化し、反応性炎症を引き起こすと考えられる1) 。
第2段階(虚血) :炎症による血管壁障害が血栓形成と血管閉塞を引き起こす。毛細血管無灌流領域が拡大し、虚血が進行する。
第3段階(血管新生) :虚血網膜からVEGFが大量に分泌される3) 。硝子体中にはVEGFのほかIL-6・IL-8・MCP-1が高濃度で検出され、病的血管新生と炎症の持続ループを形成する3) 。sea-fan様の新生血管が虚血境界部に出現し、脆弱な新生血管からの出血が繰り返される。
なお、イールズ病と結核関連網膜血管炎(TRV)は臨床像がほぼ区別不能であり、スペクトラム関係にある可能性が示唆されている2) 。
コカインは血管収縮・内皮障害を介して血栓形成を促進し、免疫学的トリガーとして働く可能性がある4) 。第V因子Leiden変異ヘテロ接合体は血栓リスクを約7倍増加させ、血管閉塞の遺伝的リスク因子となる4) 。
国際コンセンサスガイドライン(COTS)によりTRV(結核関連網膜血管炎)の管理アルゴリズムが整理されつつある2) 。イールズ病とTRVはこれまで別疾患として扱われてきたが、その境界が再検討されており、臨床像・病因の連続性が議論されている2) 。
ラニビズマブ無効のイールズ病に対してアフリベルセプトを使用し、43か月後に20/25を維持した症例および28か月間3か月ごとの反復投与で20/20を維持した症例が報告されている3) 。これはイールズ病に対するアフリベルセプト使用の初の症例報告であり、VEGF-A・B・PlGFを同時に結合することで既存の抗VEGF薬 に抵抗する症例にも効果を示す可能性がある3) 。
コカイン乱用や第V因子Leiden変異といった新たなリスク因子が個別症例から同定されており4) 、今後は免疫学的・遺伝学的な素因の解明が進むことが期待される。
Horvath D, Aljameey U, Douglas E. Double Trouble: Eales Disease in a Background of Paradoxical Embolism. Cureus. 2023;15(9):e44708.
Kiryakoza LC, Sengillo JD, Fernandez MP, Pathengay A, Albini TA, Flynn HW Jr. Retinal Vasculitis in the Setting of Mycobacterium tuberculosis Exposure. Case Rep Ophthalmol. 2025;16:18-26.
Hsia NY, Lin CJ, Lai CT, Bair H, Chang CH, Lin JM, Tsai YY. Intravitreal Aflibercept as a Rescue Therapy for Retinal Neovascularization and Macular Edema due to Eales Disease. Case Rep Ophthalmol Med. 2021;2021:8887362.
Iannetti L, Scarinci F, Alisi L, Beccia A, Cacciamani A, Saturno MC, Gharbiya M. Cocaine Abuse as an Immunological Trigger in a Case Diagnosed with Eales Disease. Medicina. 2023;59(1):169.
Biswas J, Sharma T, Gopal L, Madhavan HN, Bharat R, Badrinath SS. Eales disease—an update. Surv Ophthalmol. 2002;47(3):197-214.
Saxena S, Kumar D. A new staging system for idiopathic retinal periphlebitis. Eur J Ophthalmol. 2004;14(3):236-239.
Goel N, Kumar V, Seth A, Ghosh B. Pattern of macular involvement in Eales’ disease. J Ophthalmic Inflamm Infect. 2011;1(3):109-116.
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト) してください