経過観察
第一選択:3〜6ヶ月の経過観察で乳頭浮腫が自然消失する症例が多い。
定期検査:OCTと蛍光眼底造影で乳頭浮腫とMEの推移を追う。
血糖管理:急激な血糖変動を避けた安定したコントロールを継続する。

糖尿病性乳頭症(Diabetic Papillopathy; DP)は、糖尿病患者に生じる比較的稀な視神経乳頭浮腫である。1971年にLubowとMakleyが1型DM若年患者において初めて報告した。発症率は約0.5%と低いが、1型・2型を問わず全年齢層で発症する。
DPの本態は、視神経乳頭前層(ONH: optic nerve head)領域における軽度で可逆的な虚血と考えられている2)。乳頭虚血のスペクトラムの一端として、機能障害を伴わない乳頭浮腫からNA-AIONの明瞭な梗塞まで連続した病態が存在するという考え方も提唱されている2)。
DPの特徴は、著明な乳頭浮腫を呈しながらも視力・視野への影響が最小限にとどまる点にある。RAPD(相対的求心性瞳孔反応障害)は軽微のみで、高度な視野欠損は通常認めない2)。乳頭浮腫は自然消失し、視神経萎縮をほとんど残さない2)。
一部の著者はDPをNA-AIONの一形態と捉えるが、その病態的位置づけについてはまだ結論が出ていない。診断は除外診断であり、他疾患との鑑別が必要である(「診断と検査方法」の項参照)。
明確な関連はない。糖尿病網膜症(DR)を伴わなくてもDPは発症しうる。一方、63〜80%の症例でDRが併存するという報告もあり、両者の合併は頻繁に見られる。DRの重症度とDPの発症には相関が認められていない1)。
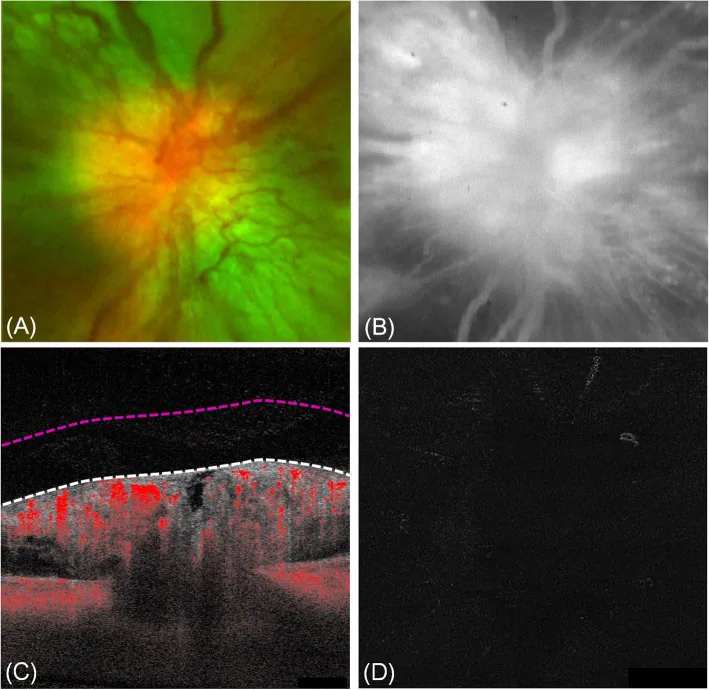
多くの患者は無症状で、糖尿病の定期眼科検診において偶発的に発見される。症状を訴える場合でも軽微である。
乳頭浮腫の程度と視力・視野への影響の乖離がDPの特徴である。以下にDPの主な臨床所見を示す。
| 所見項目 | 特徴 |
|---|---|
| 乳頭浮腫 | 充血性・表面血管拡張 |
| 初診視力 | 20/20〜20/200 |
| RAPD | 軽微のみ |
| 色覚異常 | 通常なし |
| 視野 | 盲点拡大のみ |
| 乳頭浮腫の持続 | 最大12ヶ月後に自然消失 |
乳頭表面には拡張した微小血管が認められることが約50%の症例でみられる。この乳頭表面の血管拡張は硝子体中に進展せず、増殖糖尿病網膜症における新生血管(NVD)と区別される点が重要である。
黄斑浮腫(ME)は50%以上の症例に合併する1)。また、対側眼にcrowded optic disc(小型で窮屈な乳頭)を認めることが高頻度で報告されている2)。乳頭浮腫は最大12ヶ月持続した後、自然消失することが多く、視神経萎縮をほとんど残さない2)。
Arapiら(2021)が報告した症例1(60歳女性、2型DM、HbA1c 10.9%)では、右眼視力6/360と重度の乳頭浮腫にsplinter hemorrhage(線状出血)を認めた。治療後7週で視力は20/30まで回復した1)。
DPの病因は完全には解明されていないが、糖尿病性微小血管症が基盤にあると考えられている。1型・2型糖尿病の双方で発症する。
主なリスク要因は以下の通りである。
NA-AIONのリスク因子としてDMが挙げられており、DPとNA-AIONは共通の病態基盤を持つ可能性がある2)。
急速な血糖コントロール(インスリン新規開始など)がDPの発症に寄与するとされている。血糖値の急低下により視神経乳頭周囲に水分が蓄積し、乳頭浮腫を引き起こす機序が推測されている。インスリン治療開始時は眼科でのフォローアップが重要である。
DPは除外診断である。以下の診断基準に合致し、他疾患を除外することが必要である2)。
DPの診断基準(Salvetat et al. 2023)2):
DPとNA-AIONの鑑別点を以下に示す。
| 鑑別点 | 糖尿病性乳頭症 | NA-AION |
|---|---|---|
| RAPD | 軽微/なし | 明瞭 |
| 視野欠損 | 盲点拡大のみ | 水平半盲 |
| FA所見 | early leakage | 充盈遅延あり |
DPはRAPD陰性、視野欠損最小限、自然軽快が特徴である。NA-AIONでは水平半盲、明瞭なRAPD、視神経萎縮が生じる。FA所見では、DPは乳頭表面からのvery early leakage、NA-AIONは充盈遅延を示す2)。両者はONH虚血のスペクトラム上の連続した病態とも考えられている2)。
経過観察が基本である。DPは3〜6ヶ月(最長12ヶ月)で自然寛解することが多く、視力を維持したまま乳頭浮腫が消退する。
経過観察
第一選択:3〜6ヶ月の経過観察で乳頭浮腫が自然消失する症例が多い。
定期検査:OCTと蛍光眼底造影で乳頭浮腫とMEの推移を追う。
血糖管理:急激な血糖変動を避けた安定したコントロールを継続する。
ステロイド療法
テノン嚢下注射(STTAI):triamcinolone 40mg/mLを使用。IVTAより眼圧上昇リスクが低い1)。
Mansourらの報告:subtenon betamethasoneを6眼に投与し、自然経過5ヶ月を3週間に短縮1)。
IVTA(硝子体内注射)との比較:Ozdekらによれば、IVTAはSTTAIの3倍の眼圧上昇リスク(>21mmHg)1)。
抗VEGF+ステロイド併用
IAI(aflibercept 2mg/0.05mL)+STTAI(TA 40mg/mL):重症例に対する併用報告がある1)。
効果:5〜7週以内に乳頭浮腫と視力が回復。12ヶ月の経過観察で安定を維持1)。
その他:ranibizumabやbevacizumabによる抗VEGF単独療法の報告もある。
Arapiら(2021)は重症DPの2症例に対してIAI(aflibercept 2mg)とSTTAI(triamcinolone 40mg/mL)の併用療法を施行した1)。症例1(HbA1c 10.9%)は右眼6/360→7週後20/30、左眼6/60→5週後20/25に改善した。症例2(HbA1c 11.2%)は左眼6/120→5週後20/30に回復した。いずれも12ヶ月のフォローアップで安定した経過を示した。
多くの症例は3〜6ヶ月(最長12ヶ月)で自然寛解し、92%で視力が維持される。経過観察が第一選択である。重症例や著明な黄斑浮腫を合併する場合は、ステロイドや抗VEGFによる治療が回復を促進する可能性がある1)。
DPの病態は糖尿病性微小血管症を基盤とする。現在提唱されている主な機序は以下の通りである。
DPに対する抗VEGF療法(aflibercept、ranibizumab、bevacizumab)とステロイドの併用療法は、重症例における有効性が症例報告レベルで報告されている。Arapiらは併用療法によって重症DPの視力回復と乳頭浮腫の消退が促進されることを示した1)。しかし現時点では症例報告にとどまり、治療プロトコールの標準化には大規模前向き研究が必要である1)。
Salvetatら(2023)はDPをONH虚血スペクトラムの軽症端として位置づけ、DPとNA-AIONが病態的に連続した疾患群を形成する可能性を論じている2)。この視点は、DPの予後因子の同定や治療介入のタイミングを決める上で重要な意義を持つ。両者の境界を規定するバイオマーカーや画像診断指標の開発が今後の課題である2)。