自覚症状
視力低下:DMEなしでも視力不良となる。
霧視・中心暗点:黄斑部虚血に伴う機能低下。
視野欠損:虚血領域に対応した局所欠損。

糖尿病黄斑虚血(diabetic macular ischemia; DMI)は、糖尿病患者において黄斑部の網膜毛細血管が閉塞・萎縮・消失し、毛細血管前細動脈の狭窄・閉塞を呈する状態である。FA(蛍光眼底造影)またはOCTA(光干渉断層血管造影)で、FAZ(中心窩無血管領域)の拡大・不整および黄斑部の非連続的無血管領域の拡大として描出される。
歴史的には、Norman Ashtonが死後眼の周辺虹彩前癒着染色・墨汁注入法による研究で、糖尿病網膜症における動脈・毛細血管の関与を初めて詳細に記述した。病理学的には、終末細動脈・毛細血管前血管の硝子様変性→管腔閉塞→動脈・毛細血管床消失→静脈側新生血管形成という経過をたどる。
糖尿病黄斑症は黄斑浮腫・虚血性黄斑症・RPE症の3型に分類されるが、DMIは虚血性黄斑症に相当する。
有病率は糖尿病網膜症の重症度と密接に関連する。
| DMI重症度 | 発生率 |
|---|---|
| なし | 39.7% |
| 疑い | 18.4% |
| 軽度 | 25.2% |
| 中等度 | 11.0% |
| 重度 | 5.6% |
CSME(臨床的に意義のある黄斑浮腫)症例の29.4%にDMIが併発し、うち19.4%が中等度〜重度である。また増殖糖尿病網膜症(PDR)の77.2%、重症非増殖糖尿病網膜症(NPDR)の59.7%にDMIが認められる。
DMIの所見は「特徴のない網膜(featureless retina)」として特徴づけられることがある。中心窩反射が不良となり、出血・微小血管瘤・滲出物・軟性白斑・新生血管が消失または軽度にとどまる。
自覚症状
視力低下:DMEなしでも視力不良となる。
霧視・中心暗点:黄斑部虚血に伴う機能低下。
視野欠損:虚血領域に対応した局所欠損。
臨床所見
featureless retina:中心窩反射不良、出血・滲出物の消失・軽度化。
ゴースト血管:灌流を失った毛細血管の残影。
細動脈狭小化:中等度〜重度DMIでは平均細動脈径が狭小化。
機能検査
マイクロペリメトリ:DCP非灌流領域で網膜感度が著しく低下。1)
AO-OCT:DCP非灌流領域で視細胞シグナル密度(IS/OS・COST)が約40%低下。1)
DMI重症度と視力の相関については、中等度〜重度DMIで有意な視力低下が認められる。VA-FAZ相関はR²=0.41〜0.51と報告されており、視神経乳頭黄斑間虚血は視力低下と独立して関連する。
Datlingerら(2021)はAO-OCTとマイクロペリメトリを用いた研究で、DCP非灌流領域において視細胞シグナル密度(IS/OSおよびCOST)が約40%低下し、同領域の網膜感度も著しく低下していることを示した。1)
軽度DMIでは視力への有意な影響が生じない場合がある。中等度〜重度になると視力低下との有意な相関が認められ(VA-FAZ相関R²=0.41〜0.51)、視神経乳頭黄斑間虚血も視力低下と独立して関連する。DMEを伴わないにもかかわらず視力不良な場合は、「診断と検査方法」の項の検査によるDMI評価が重要となる。
DMIのリスク因子は糖尿病網膜症全般のリスク因子を反映している。
DMIの存在はDMEおよびDRの重症度増加と関連する。内科的加療(血糖・血圧・脂質の管理)が網膜症進行抑制に有効である。
なお、良好な血糖コントロール(HbA1c 6.1%→5.6%への改善)によって毛細血管非灌流領域(NPA)の自然再灌流が生じた症例も報告されている。2)
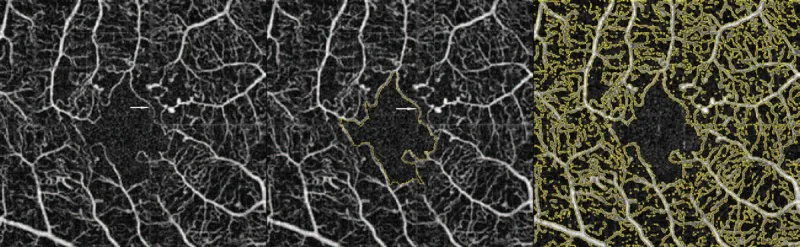
FAはDMI診断のゴールドスタンダードである。
FAの欠点として、侵襲性(静脈内造影剤投与)、合併症リスク(死亡リスク約1/20万)、所要時間20分以上が挙げられる。
OCTAは非侵襲的・高解像度の検査で、SCP(表層毛細血管網)・DCP(深層毛細血管網)・CC(脈絡毛細血管層)の層別解析が可能である。
FAとOCTAの特性比較を以下に示す。
| 特徴 | FA | OCTA |
|---|---|---|
| 侵襲性 | あり | なし |
| 層別解析 | 不可 | 可能 |
| NPA検出範囲 | 限定的 | 広範 |
FA
ゴールドスタンダード:FAZ拡大・毛細血管消失を描出。
侵襲的:造影剤静注が必要。死亡リスク約1/20万。
所要時間:20分以上を要する。
OCTA
非侵襲的・高解像度:SCP/DCP/CCの層別解析が可能。
NPA定量化:DR重症度と相関。前臨床的変化も検出。3)
2種類のNPA検出:菲薄化の有無でFAとの検出範囲が異なる。2)
FAがゴールドスタンダードだが侵襲的である。OCTAは非侵襲的で、FAよりも広範なNPAを検出できる利点がある。2) 特に網膜菲薄化を伴わない早期NPA(菲薄化なしNPA)はOCTAのみで検出可能である。両者の特性は相補的であり、臨床状況に応じて使い分けることが望ましい。
DMIに対する確立された特異的治療法は現時点で存在しない。DMEを伴わない黄斑虚血に対する直接的な治療法はなく、全身管理が基本となる。
良好な血糖管理がNPA自然再灌流に寄与する可能性が報告されており、2) 内科的加療(血糖・血圧・脂質)が網膜症進行抑制の基本戦略である。
severe NPDR以降の段階では、PRP(汎網膜光凝固術)または抗VEGF療法の検討が推奨される。3)
DMIにDMEが併発する場合、以下の治療が行われる。
DMIに対する確立された特異的治療法は現時点でない。全身管理(血糖・血圧・脂質)が基本であり、良好な血糖コントロールによってNPAが自然再灌流した症例報告がある。2) DMEを合併している場合は抗VEGF薬等で浮腫を治療するが、虚血自体を直接改善することはできない。
周細胞消失と内皮細胞損傷がDR血管変化の最も初期の兆候である。
III型・IV型コラーゲン沈着による毛細血管基底膜肥厚が進行すると、管腔が狭小化する。白血球停滞(leukostasis)も生じ、異常内皮細胞が誘発することで血管閉塞を悪化させる。
酸素・微量栄養素供給の低下がVEGF発現を刺激し、毛細血管網の段階的萎縮→毛細血管間隙拡大→長期低酸素→視細胞損傷へと進展する。DRの進行に伴い静脈異常・IRMA・重症の出血・滲出が出現する。3)
黄斑部には3層の網膜血管層(SCP・ICP/MCP・DCP)が存在する。DCPは視細胞の酸素供給に10〜15%寄与しており、1) その閉塞が直接的な視細胞障害につながる。
ミュラー細胞(MC)は灌流障害下で視細胞に乳酸を供給するエネルギー源として機能する。1) MC障害が生じると、錐体・桿体・MC機能低下に加え、視細胞外節のパッチ状消失と毛細血管脱落の共局在が認められる。1)
虚血パターンは以下の4型に分類される(Takashiらの分類)。
| 虚血タイプ | 頻度 |
|---|---|
| 周辺部型 | 2.6% |
| 中間周辺部型 | 61.2% |
| 中心部型 | 26.3% |
| 広範型 | 9.9% |
DCP(深層毛細血管網)の非灌流により、視細胞への酸素供給が低下する(DCPは視細胞酸素供給に10〜15%寄与)。1) ミュラー細胞障害も視細胞へのエネルギー供給を阻害する。AO-OCTを用いた研究では、DCP非灌流領域でIS/OS・COSTの視細胞シグナル密度が約40%低下することが確認されている。1)
Datlingerら(2021)は、AO-OCTとOCTAの組み合わせにより単一錐体視細胞レベルのDMI評価が可能となることを示した。マイクロペリメトリとOCTAを統合した研究アプローチが、DMIの時間経過の理解に寄与すると述べ、これらの先進的イメージングパラメータが将来の治療研究でバイオマーカーとなる可能性を指摘した。1)
従来、毛細血管閉塞は不可逆と考えられてきたが、自然再灌流の症例が報告されている。
Houら(2022)は、HbA1cが6.1%から5.6%に改善した糖尿病患者において、NPAの自然再灌流を観察した。IRMAがNPA内に侵入して新たな毛細血管網を形成する過程をOCTAで経時的に記録した。2)
この報告から、NPAには2種類の性質が示唆されている。2)
1年間のOCTA追跡研究では、ベースライン非灌流とDR進行のオッズ比(OR)=8.73、深層非灌流と治療介入のOR=3.39が報告されており、OCTA非灌流指標が予後予測バイオマーカーとなる可能性が示されている。FAZのベースライン面積は既知のDMI眼で年間5〜10%拡大する傾向がある。AIのOCTA画像解析への応用も研究が進められている。3)
まれながら自然再灌流の報告がある。Houら(2022)はIRMAがNPA領域に侵入し新たな毛細血管網を形成する過程を報告した。2) 特に菲薄化を伴わないNPA(早期変化)は2か月以内に再灌流しやすい傾向がある。良好な血糖コントロールが再灌流を促進する可能性も示されている。
Datlinger F, Georgi T, Stegmann H, et al. Assessment of detailed photoreceptor structure and retinal sensitivity in diabetic macular ischemia using adaptive optics-OCT and microperimetry. Invest Ophthalmol Vis Sci. 2021;62(13):1.
Hou S, Chen L, Shan K, et al. Spontaneous retinal reperfusion of capillary nonperfusion areas in diabetic retinopathy. Case Rep Ophthalmol. 2022;13:818-824.
American Academy of Ophthalmology Retina/Vitreous Panel. Diabetic Retinopathy Preferred Practice Pattern. Ophthalmology. 2024.