Stage 1〜2
Stage 1:網膜毛細血管拡張のみを認め、滲出物を伴わない段階。
Stage 2A:毛細血管拡張に加え、中心窩外に滲出物を認める段階。
Stage 2B:滲出物が中心窩にまで及んでいる段階。視力低下が顕在化する。

コーツ病(Coats disease)は、1908年にGeorge Coatsが報告した特発性の網膜血管疾患である。網膜毛細血管の異常な拡張(毛細血管拡張症)と、血管壁からの網膜内・網膜下への滲出物蓄積を本態とする。
疾患の性格は散発性かつ非遺伝性であり、全身疾患や家族歴との関連は認めない1)。発症率は10万人あたり0.09人と稀である2)。患者の約75%が男性、95%が片眼性であり、20歳以下(平均5歳前後)に好発する。
成人発症は非常に稀だが、小児型と異なる臨床像を呈する。成人発症例は小児型より軽症で進行が緩徐であり、治療反応も良好とされる3)。ある報告では成人発症48眼のうち滲出性網膜剥離を来たしたのは21%にとどまり、小児発症の81%に比べて有意に低かった3)。
軽症型はLeber粟粒血管腫症(Leber’s miliary aneurysms)とも呼ばれ、コーツ病のスペクトラムの一端を形成する。1型特発性黄斑毛細血管拡張症も同一疾患スペクトラムに含まれると考えられている。
35歳以上での発症例が報告されており、成人発症コーツ病として認識されている3)。小児型と比べて病変の進行が緩徐で滲出性網膜剥離を来たす頻度が低く、治療への反応も良好な場合が多い。ただし発症自体は稀であり、成人で類似所見を認めた場合は他疾患との鑑別が重要である。
乳幼児期に発症した場合、患児自身が症状を訴えることは少ない。
成人発症例では視力が比較的保たれており、健診で偶然発見される場合もある3)。
眼底所見の特徴は、周辺部に集中する異常拡張した網膜血管と、黄白色の網膜下・網膜内滲出物の蓄積である。蛍光眼底造影では、周辺部の網膜血管閉塞、毛細血管拡張、毛細血管瘤、新生血管が特徴的所見として描出される。進行すると滲出性網膜剥離を来たし、最終的には全剥離に至る。超音波検査やCT、MRIでは網膜下液が隅々まで均質に描出され、この点が石灰化を伴う不均質な像を呈する網膜芽細胞腫との重要な画像上の鑑別点となる。
後期には虹彩ルベオーシスや新生血管緑内障などの前眼部合併症を生じる。黄斑円孔はまれな合併症であり、文献上で7例程度しか報告されていない4)。線維性結節は視力予後不良の因子であり、OCTAでは結節内にtype 3 新生血管(SVC→DVC→無血管複合体)が確認されている5)。
Shields分類はコーツ病の病期を以下の5段階に分類する。治療方針の選択と予後推定に用いる。
Stage 1〜2
Stage 1:網膜毛細血管拡張のみを認め、滲出物を伴わない段階。
Stage 2A:毛細血管拡張に加え、中心窩外に滲出物を認める段階。
Stage 2B:滲出物が中心窩にまで及んでいる段階。視力低下が顕在化する。
Stage 3
Stage 3A1:中心窩外の亜全網膜剥離を伴う段階。
Stage 3A2:中心窩を含む亜全網膜剥離を伴う段階。視力予後が不良となる。
Stage 3B:全網膜剥離を来たした段階。緊急的な介入が必要となる。
Stage 4〜5
Stage 4:全網膜剥離に続発性緑内障を合併した終末期前段階。疼痛を伴うことがある。
Stage 5:終末期。眼球癆(萎縮)に至った状態。眼球摘出が検討される段階。
白色瞳孔を呈する疾患は複数あり、コーツ病はその一つにすぎない。最も重要な鑑別疾患は網膜芽細胞腫(Rb)であり、生命予後に直結するため緊急評価が必要である。そのほか未熟児網膜症、永続性胎生血管症候群(PHPV)、眼内炎なども鑑別に挙がる。詳細は「診断と検査方法」の項を参照。
コーツ病の発症原因は不明であり、全身疾患や家族歴との関連は認められていない。遺伝的背景を示す報告として第3・13染色体の不安定性、NDP遺伝子(Norrie病関連)、CRB1遺伝子との関連が示唆されているが、確立されたものではない。
病態の出発点として、内部血液網膜関門(iBRB)の破綻が中心的な役割を果たすと考えられている1)。周皮細胞(血管内皮を支持する細胞)の減少により血管壁が脆弱化し、異常に拡張した毛細血管や動脈瘤が形成される1)。血漿成分が血管壁内・網膜層内へ漏出・蓄積することで血管壁が肥厚し、さらなる滲出を招くという悪循環が成立する2)。
高VEGF環境が末梢部毛細血管の拡張を促進することも示唆されており2)、この機序が抗VEGF療法の理論的根拠となっている。
診断には複数の検査を組み合わせ、特に網膜芽細胞腫(Rb)との鑑別を確実に行うことが最重要課題となる。
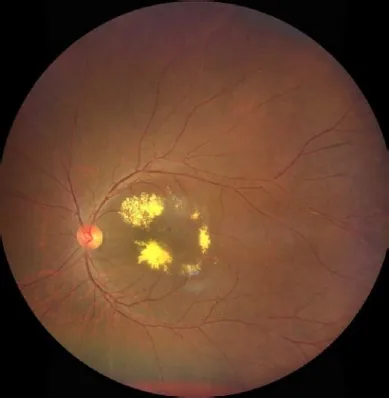
散瞳下眼底検査で、周辺部に蛇行した異常血管網と黄白色の網膜下滲出物を確認する。滲出物が黄斑部に及ぶと硬性白斑様の外観を呈する。
コーツ病診断における最重要検査の一つである。毛細血管の著明な拡張、毛細血管瘤、動静脈吻合、および「light bulbs」(電球状の蛍光漏出)が特徴的所見である。異常血管の範囲確認とレーザー凝固部位の決定に不可欠である。
固形腫瘤を認めないことを確認する。RbはBモードで固形腫瘤内に高輝度エコー(石灰化)を示すことが多いが、コーツ病では固形腫瘤は形成されない。
石灰化の有無を評価する。Rbは高率に石灰化を伴うのに対し、コーツ病は石灰化を来たさない。この所見が鑑別の重要な根拠となる。
コーツ病と網膜芽細胞腫の主な鑑別点を以下に示す。
| 項目 | コーツ病 | 網膜芽細胞腫 |
|---|---|---|
| 好発年齢 | 5歳前後 | 1〜2歳 |
| 性差 | 男性75% | なし |
| 両眼性 | 約5% | 約40% |
| 石灰化 | なし | あり(高率) |
| 固形腫瘤 | なし | あり |
治療の目標は異常血管を閉塞させ、滲出物の産生を停止させることである。病期に応じた段階的アプローチをとる。
第一選択治療である。FAで確認した異常拡張血管・毛細血管瘤を直接凝固し、さらに周辺部無灌流領域にも光凝固を行う。小児では全身麻酔下で施行する。複数回のセッションが必要な場合が多く、治療後も定期的なFAによる再評価と追加凝固を繰り返す。
前部周辺部の病変や、光凝固困難な部位に用いる次のオプションである。光凝固と組み合わせて使用することもある。
レーザー凝固
適応:Stage 1〜3Aの異常血管・滲出病変。
方法:FA誘導下に毛細血管拡張部位と無灌流領域を直接凝固。小児は全麻下で施行。
特徴:繰り返し施行が可能。治療後の定期FA再評価と追加凝固が標準的管理。
冷凍凝固
適応:光凝固困難な前部周辺病変、Stage 3B以下の重症例での補助。
方法:経強膜的に冷凍プローブを当て、異常血管を凝固・閉塞する。
特徴:混濁媒体下や最周辺部でも施行できる利点がある。
硝子体・網膜手術
適応:Stage 3B(全網膜剥離)以上、冷凍凝固無効例。
方法:外部排液または硝子体手術による網膜下液の排液と、内部からの網膜復位8)。
特徴:黄斑円孔を合併した症例には内境界膜(ILM)翻転法が有効との報告がある4)。
抗VEGF薬のコーツ病に対する使用はコンセンサスが未確立であり、標準治療ではなく光凝固との併用における補助療法として位置づけられる。
成人発症コーツ病の1例にranibizumab 0.5mgの硝子体内注射とレーザー凝固を組み合わせた治療を行い、最終矯正視力が指数弁から20/60へと改善したとの報告がある3)。
小児例にbevacizumab 1.25mgの硝子体内注射、sub-Tenon トリアムシノロン、レーザーの併用療法をEUA(全麻下試験)で6週ごとに行った報告では、治療後に逆説的な滲出増悪(paradoxical exudative retinopathy)が生じる場合があることが指摘されている2)。
bevacizumab抵抗例に対しbrolucizumabが有効であったとの報告も出現している2)。線維性結節の形成予防に抗VEGF療法が寄与する可能性が示唆されている5)。
疼痛を伴う失明眼(Stage 4〜5)で、かつRbの否定が困難な場合には眼球摘出が選択される。
コーツ病では数年の経過で再燃・再剥離を起こす症例があり、また両眼性で発症時期が異なる症例もある。治療完了後も定期的な蛍光眼底造影による再評価を行い、新規病変が確認された場合には追加の光凝固または冷凍凝固を施行する必要がある。
現時点では抗VEGF薬のコーツ病への使用に関するコンセンサスは確立されておらず、標準治療としての位置づけではない。レーザー光凝固との併用補助療法として報告が蓄積されつつあるが、有効性・安全性の評価はさらなる研究を要する。
コーツ病の発症機序の中心は内部血液網膜関門(inner blood-retinal barrier; iBRB)の破綻である1)。
iBRBは網膜毛細血管の内皮細胞と、それを支持する周皮細胞によって構成される。コーツ病では周皮細胞の数が著明に減少しており、これが血管内皮支持機能の低下をもたらす1)。内皮細胞自体の数も減少していることが免疫染色および電子顕微鏡観察で確認されている1)。
内皮BRBの破綻により、血漿成分(主にリポタンパク質、コレステロール)が血管壁内・網膜内・網膜下へ漏出・蓄積する1)。蓄積した脂質は脂質含有マクロファージ(泡沫細胞)の浸潤と肉芽腫性免疫反応を惹起し、組織障害を増悪させる1)。
高VEGF環境が末梢部毛細血管のさらなる拡張を促進し、病変の進行に関与する2)。OCTAによる観察では、進行した病変部の黄斑線維性結節内にtype 3 新生血管(SVC→DVC→無血管複合体の順に形成)が確認されており5)、新生血管形成プロセスの解明が進んでいる。
黄斑円孔が生じる機序として、末梢部レーザー照射による網膜短縮が接線方向の牽引を生じ、黄斑部に穿孔をきたすと考えられている4)。
OCTAは線維性結節内の微小血管構造を非侵襲的に評価することを可能にした。
Ongら(2021)はOCTAを用いて黄斑結節内の血管構造を詳細に分析し、SVC→DVC→無血管複合体の順に形成されるtype 3 新生血管の存在を明らかにした5)。この知見は結節形成機序の解明と抗VEGF療法の標的として重要である。
抗VEGF治療開始後に逆説的に滲出が増悪する現象が報告されており、機序解明と管理法の確立が求められている。
Kalavar ら(2022)は、治療開始後に一過性の滲出増悪と黄斑部星芒状滲出(macular star formation)を来たした小児コーツ病例を報告した2)。bevacizumab抵抗例に対してbrolucizumabを使用したところ有効であったとされ、新たな治療選択肢として注目されている2)。
Nawrockaら(2023)は、コーツ病に合併した黄斑円孔に対しinverted 内境界膜 flap法を用いた硝子体手術を施行した1例を報告した4)。術後18ヶ月で黄斑円孔の閉鎖が確認され、最終矯正視力は20/40であった。コーツ病関連黄斑円孔はPubMed上で7例程度しか報告されていない稀な合併症である4)。
成人発症コーツ病は従来過小認識されてきた疾患概念であり、報告数が増加している3)。小児型との臨床的差異(軽症・緩徐進行・良好な治療反応)の整理が進み、成人における適切な治療プロトコールの確立が課題となっている。