ブロルシズマブ
分子量:26 kDa
構造:scFv(一本鎖可変領域断片)Fc領域なし
モル濃度:アフリベルセプトの約12倍6)
硝子体内半減期:約3.0日

ブロルシズマブ(商品名:ベオビュ®)は、ヒト化一本鎖可変領域断片(scFv)からなる抗VEGF薬である。VEGF-A(血管内皮増殖因子A)のすべてのアイソフォームに結合し、VEGF受容体への結合を阻害する。
分子量は26kDaと既存の抗VEGF薬の中で最小であり12)、組織浸透性に優れる。VEGF165に対する結合親和性(KD)は28.4 pMで、VEGFR2に対するIC50は0.86 nMである6)。
同一投与量(6mg)でのモル濃度は、アフリベルセプトの約12倍、ラニビズマブの約22倍に相当する6)。
承認状況は以下の通りである。
既存薬との分子量の比較を以下に示す。
ブロルシズマブ
分子量:26 kDa
構造:scFv(一本鎖可変領域断片)Fc領域なし
モル濃度:アフリベルセプトの約12倍6)
硝子体内半減期:約3.0日
アフリベルセプト
分子量:97〜115 kDa
構造:融合タンパク質(VEGFR1/2細胞外ドメイン+IgG1 Fc)
モル濃度:ブロルシズマブの1/12
硝子体内半減期:約4.7日
ラニビズマブ
ブロルシズマブはscFv構造により分子量26kDaと最小で、同一濃度でのモル数がアフリベルセプトの約12倍と高い6)。小分子であるため組織浸透性も高く12)、注射間隔を長くできる可能性がある。一方でIOIの発症率が他剤より高い点が注意事項である。詳細は「安全性と副作用」の項を参照。
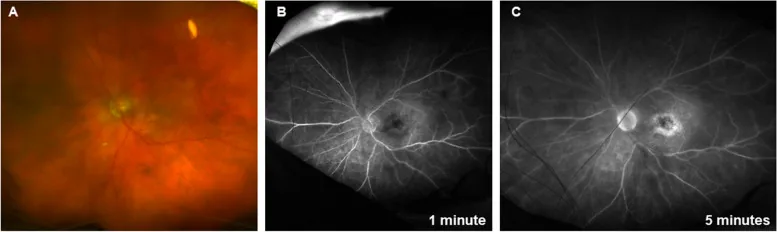
HAWK・HARRIER試験は計1817例を対象とした第III相無作為化比較試験であり、アフリベルセプト(2mgを8週間隔)を対照にブロルシズマブ(3mgおよび6mg)の有効性を検討した10)。
主要評価項目であるBCVA(最高矯正視力)の変化量(48週)は以下の通りであった。
| 試験 | ブロルシズマブ6mg | アフリベルセプト2mg |
|---|---|---|
| HAWK 48週 | +6.6文字 | +6.8文字 |
| HAWK 96週 | +5.9文字 | +5.3文字 |
| HARRIER 48週 | +6.9文字 | +7.6文字 |
| HARRIER 96週 | +6.1文字 | +6.6文字 |
いずれも非劣性基準を満たした10)。96週時点での成績も同等であり、長期有効性が確認されている。
網膜内液・網膜下液・RPE下液の残存割合はブロルシズマブ群で有意に低く、液体減少効果が優れていた10)。
維持期に12週間隔投与が維持できた割合は、HAWK 55.6%・HARRIER 51.0%であった。
HAWK/HARRIER試験では、MERLIN試験(4週間隔)においてIOI発症率が9.3%と高く、試験が中断された10)。この結果から最低2か月間隔の投与が推奨されている。
日本人ポリープ状脈絡膜血管症患者における48週時点の最高矯正視力変化量は、ブロルシズマブ群+10.4文字・対照群+11.6文字であり、96週では+11.4文字・+11.1文字と同等だった11)。
12週間隔投与が維持できた割合は48週時点で76%、96週時点で68%であった11)。
ポリープ消退率はブロルシズマブで約78.9%と、ラニビズマブ(約30%)・アフリベルセプト(約50%)を大きく上回る11)。脈絡膜厚は15〜20%減少し12)、ポリポイダル病変の80〜90%で退縮が確認されている12)。
Carta Vら(2023)は、黄斑部に脂質滲出を伴うポリープ状脈絡膜血管症 1例にブロルシズマブ硝子体内注射を行い、8回の注射後に視力が20/400から20/60に改善し、脂質滲出がほぼ完全に吸収されたことを報告した1)。
KESTREL(6mg群)では52週時点の最高矯正視力変化量+9.2文字(対照+10.5文字)、KITE試験では+10.6文字(対照+9.4文字)であった9)。52週までの中央値投与回数は7回であり、55%(KESTREL)・50%(KITE)の患者で12週間隔維持が達成された9)。
HAWK/HARRIER(nAMD)
対象:nAMD 1817例、第III相RCT
結果:48週最高矯正視力でアフリベルセプトと非劣性10)
12週間隔達成:HAWK 55.6%・HARRIER 51.0%
KESTREL/KITE(糖尿病黄斑浮腫)
対象:糖尿病黄斑浮腫、52週追跡
結果:アフリベルセプト比較で非劣性9)
12週間隔達成:KESTREL 55%・KITE 50%9)
適応外・症例報告
Villegasら(2022)は放射線網膜症の1例にブロルシズマブを投与し、1回の注射後に嚢胞様黄斑浮腫が消退し、最高矯正視力が20/200から20/50に改善したと報告した5)。
Chakraborty・Shethら(2022)は血管様線条に伴う脈絡膜新生血管の1例に対し、ブロルシズマブ単回投与で最高矯正視力が20/120から20/32に改善したと報告した6)。
Chakraborty・Shethら(2022)はブロルシズマブとSF6ガスによる気送転位術を組み合わせた網膜下出血(SMH)の3例を報告し、全例で血腫が消退した8)。
ブロルシズマブは硝子体内注射(IVT)により投与する。製剤は120mg/mL、1回6mg(0.05mL)の防腐剤フリー単回使用バイアルである。保存温度は2〜8℃。
適応別の投与スケジュールを以下に示す。
| 適応 | 導入期 | 維持期 |
|---|---|---|
| nAMD | 月1回×3回 | 8〜12週間隔 |
| 糖尿病黄斑浮腫 | 6週間隔×5回 | 8〜12週間隔 |
投与手技の要点は以下の通りである。
薬剤費はアフリベルセプトと同程度とされている。
導入期終了後は8〜12週間隔での維持投与が可能である。HAWK/HARRIER試験では約55%の患者が12週間隔を維持できた10)。ただし4週間隔(MERLIN試験)ではIOI発症率が9.3%と高くなったため、最低2か月間隔が推奨される10)。個々の病勢に応じて主治医が決定する。
IOIはブロルシズマブに特徴的な有害事象であり、最も注意が必要な副作用である。
各試験・集団別のIOI発症率を以下に示す。
| 試験・集団 | ブロルシズマブ | 対照群 |
|---|---|---|
| HAWK/HARRIER(IOI全体) | 4.6% | — |
| HAWK/HARRIER(網膜血管炎) | 3.6% | — |
| HAWK/HARRIER(血管閉塞) | 2.1% | — |
| KESTREL(6mg) | 3.7% | 0.5% |
| MERLIN(4週間隔) | 9.3% | — |
| 日本人症例 | 15〜20% | — |
市販後データでは、血管炎と閉塞の複合発症率は10,000回注射あたり3.73件と報告されている3)。アジア人ポリープ状脈絡膜血管症患者では9〜19%のIOI発症率、重症視力障害をきたす閉塞性血管炎は1〜2%とされる12)。
大多数のIOIは初回投与後6か月以内・4回以内の注射後に発症する7)。
IOI発症後の治療としては、トリアムシノロンアセトニド(STTA)5〜20mgの結膜下注射または後部Tenon嚢下注射が有効であり、予防にも用いられる4)7)。
Saito Mら(2022)は、レーザーフレアセルフォトメーター(LFP)を用いてIOI後のブロルシズマブ再投与を安全に行った症例を報告し、LFPが炎症モニタリングに有用であることを示した7)。
Shigemoto Yら(2021)は、ブロルシズマブ関連IOIの1例にSTTA(5mg)と継続投与を組み合わせて治療し、炎症制御と良好な視力維持を達成したと報告した4)。
Takayama Tら(2024)は、硝子体内ブロルシズマブ注射後に強膜炎を発症した日本人3例を世界で初めて報告した2)。3例はいずれも前眼部炎症を伴わない後部強膜炎のパターンを示し、眼圧は24〜49mmHgに上昇した。このうち1例は網膜動脈閉塞と血管炎に進展した2)。
強膜炎はIOIの非典型的な発現形態として認識されており、眼圧上昇を伴う後眼部炎症では本合併症を念頭に置く必要がある。
HAWK試験ではATE(ブロルシズマブ3mg群1.1%・6mg群1.4%)、HARRIER試験では1.6%に認められた10)。網膜動脈閉塞はブロルシズマブ3mg群で4例・6mg群で6例に認めた10)。
急激な視力低下・飛蚊症の悪化・充血・眼痛などの症状が現れた場合は、速やかに眼科を受診する。診断後はトリアムシノロンアセトニド(STTA)の結膜下あるいはTenon嚢下注射が有効であり、多くの症例で炎症は改善する4)7)。ブロルシズマブの再投与はLFPなどで炎症が消退したことを確認してから慎重に判断する7)。
ブロルシズマブはscFv(single-chain variable fragment)構造をとる。scFvは抗体の重鎖可変領域(VH)と軽鎖可変領域(VL)のみからなる最小機能単位であり、Fc領域を持たない。
この構造的特徴により、分子量26kDaという小ささを実現し12)、硝子体および網膜・脈絡膜への迅速な組織浸透が可能となる。
VEGF-Aとの結合は2:1(VEGF-Aダイマー1分子にscFv 2分子)の化学量論比で行われる。KD=28.4 pMの高親和性でVEGF-Aに結合し、VEGFR1・VEGFR2への結合を競合的に阻害する。
脈絡膜の厚みを15〜20%減少させる効果は12)、パキコロイド表現型を持つポリープ状脈絡膜血管症において特に有利に働くと考えられている。
ブロルシズマブに関連するIOIの病態には免疫学的機序が関与する。
Sharmaら(2022)は、ブロルシズマブ関連網膜血管炎の病態を総説し、ADAを介した免疫複合体沈着がIII型過敏反応を惹起し、閉塞性血管炎をもたらすメカニズムを詳述した3)。
主な原因として3点が挙げられる。第一に治療前からのADA陽性率がラニビズマブ・アフリベルセプトの5%未満に対して35〜52%と高く3)、免疫応答が起きやすい素地がある。第二にscFv構造がFc領域を欠くため免疫寛容誘導が弱い可能性がある。第三に高いモル濃度が免疫刺激を強める可能性がある3)。これらが組み合わさりIII型過敏反応を引き起こすと考えられている。
ポリープ状脈絡膜血管症・黄斑部毛細血管拡張症1型(AT1)を対象とした試験であり、ブロルシズマブの有効性・安全性を評価する12)。アジア人特有の疾患に対するエビデンスの蓄積が期待される。
結膜下・Tenon嚢下トリアムシノロンアセトニド(STTA)とブロルシズマブの併用投与は、IOI予防と滲出制御の両面で有効な可能性がある4)7)。至適用量・投与タイミングの標準化に向けた研究が進んでいる。
レーザーフレアセルフォトメーター(LFP)は前房炎症を定量評価できる非侵襲的装置であり、IOI発症後の再投与判断に活用できる可能性が示されている7)。
治療前のADA検査によってIOI高リスク患者を事前に同定し、投与適応や監視強度を個別化する戦略が検討されている3)。ADAバイオマーカーの臨床実装が実現すれば、より安全なブロルシズマブ使用が可能となる。