化学性
発症時期:出生後24時間以内
所見:軽度の充血・流涙のみ
経過:2〜4日で自然消退

新生児結膜炎(ophthalmia neonatorum)は生後28〜30日以内に発生する結膜の炎症である。 歴史的には1880年にCredeが1%硝酸銀点眼を導入し、淋菌性結膜炎の予防に大きく貢献した。 現在は抗菌点眼薬による予防が主流となっている。
世界的な発生率は2.04%(95%CI 0.70〜5.79%)、有病率は7.79%(95%CI 2.93〜19.10%)である。1) 地域差が大きく、低所得国では6.90%、高所得国では1.36%と報告されている。1) 世界全体で年間約10,000例が発生すると推計される。1)
分娩様式・在胎週数も発生率に影響する。
病因は化学性・細菌性・ウイルス性に大別される。 細菌性ではクラミジアが最も頻度が高く、淋菌が最も重症な転帰をもたらす。
世界的な発生率は約2.04%で、年間約10,000例が発生すると推計される。1)地域差があり、先進国では1.36%と低い一方、低所得国では6.90%に達する。
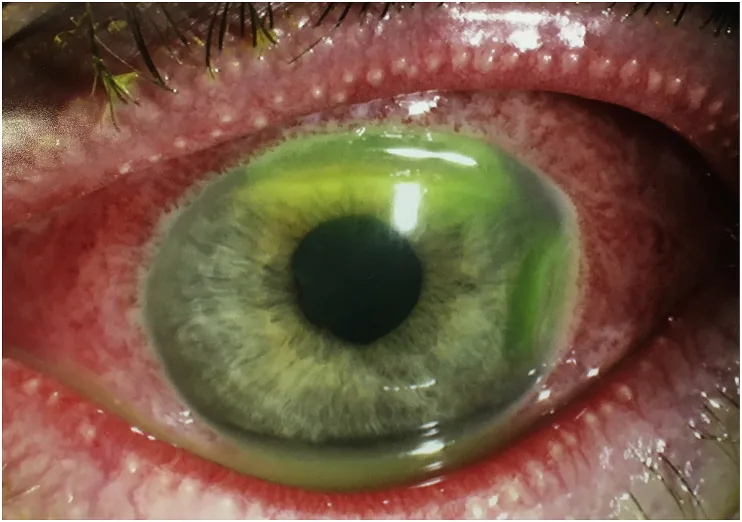
新生児は症状を訴えることができない。 保護者や医療者が客観的に観察する。
新生児では涙液分泌低下・分泌型IgA欠如・リゾチーム活性低下があり、感染に対して脆弱である。
発症時期が原因推定の最重要手がかりとなる。 各原因の特徴的な所見を以下に示す。
化学性
発症時期:出生後24時間以内
所見:軽度の充血・流涙のみ
経過:2〜4日で自然消退
淋菌性
クラミジア性
ウイルス性(HSV)
発症時期:生後1〜2週間
所見:微小樹枝状・地図状角膜潰瘍(新生児では特徴的所見に乏しい)
注意:新生児単純ヘルペスウイルス感染は全身感染に進展しうる
モラクセラ属は生後7〜10日以降に発症し、pseudogonococcal conjunctivitisと呼ばれる。
発症時期は原因推定の最重要手がかりである。化学性は24時間以内、淋菌性は生後1〜3日、クラミジア性は生後3〜10日、単純ヘルペスウイルスは生後1〜2週間が典型的な発症時期である。ただし確定診断には微生物学的検査が必要である。
産道感染が最も多い感染経路である。 母体の性感染症が主なリスク因子となる。
その他のリスク因子は以下の通りである。
Crede法(1%硝酸銀点眼)に始まる点眼予防は有効で、30試験・79,198新生児を対象としたコクランレビューでは予防薬の使用により全原因結膜炎の発生率が低下することが示された(中等度確実性)。2)
WHOが推奨する5つの予防薬は以下の通りである。2)
帝王切開でも発生率は1.88%と報告されており、完全には防げない。1)産道感染以外の経路(上行性感染など)が原因となる場合があるため、帝王切開後も注意が必要である。
発症時期による鑑別が最重要であり、「臨床所見」の項を参照して原因を推定する。 確定診断には微生物学的検査が不可欠である。
発症時期と染色所見の組み合わせが診断の鍵となる。
| 染色法 | 対象 | 観察する所見 |
|---|---|---|
| グラム染色 | 淋菌 | 好中球に貪食されたグラム陰性双球菌 |
| ギムザ染色 | クラミジア | 封入体(Prowazek小体) |
| フルオレセイン染色 | 角膜病変 | コバルトブルー光で上皮欠損を確認 |
類似症状を示す疾患を除外することが重要である。
治療は原因に応じて選択する。 日本における治療を中心に、海外の標準的プロトコールも補足する。
以下は日本での治療プロトコールである。
| 原因 | 推奨治療 |
|---|---|
| 化学性 | 人工涙液 QID(自然消退を待つ) |
| 淋菌性 | ceftriaxone 25〜50mg/kg 単回投与 |
| クラミジア性 | アジスロマイシン20mg/kg 3日間4) |
| 単純ヘルペスウイルス | アシクロビルIV 45mg/kg/日 14〜21日間 |
エリスロマイシン内服はクラミジア性結膜炎の全身治療として有効だが、乳幼児肥厚性幽門狭窄症(IHPS)との関連に注意が必要である。
新生児ではceftriaxoneの使用により高ビリルビン血症のリスクがある。3)このため眼窩蜂窩織炎を合併した重症例などではcefotaximeの使用が推奨される。投与にあたっては新生児の黄疸の状態を確認したうえで選択することが重要である。
新生児の眼は成人に比べ感染に対して脆弱である。 主な要因は以下の通りである。
偽膜はフィブリン・好中球・炎症性滲出物が結膜に付着したものである。 クラミジア性結膜炎では、腺様組織が未発達のため濾胞を形成しない(偽膜性結膜炎)。
淋菌は健常な角膜上皮を持つ眼にも感染できる唯一の細菌である。 その病原性は以下の機構による。
ケニアでは罹患児の最大16%に角膜病変が生じると報告されており、2)早期治療が不可欠である。
クラミジア(Chlamydia trachomatis)は偏性細胞内寄生体である。 細胞外では感染型の基本小体(EB)として存在し、細胞内で複製型の網状小体(RB)に変換される。 感染した上皮細胞内に封入体(Prowazek小体)を形成する。成人型封入体結膜炎では下方結膜円蓋部に大型の充実性濾胞を多数認めるのに対し、新生児封入体結膜炎は生後7日前後に発症しリンパ組織が未発達のため濾胞を認めないことが特徴である。
従来の主要病原体に加え、新たな病原体の報告が蓄積されている。
Mechel et al.(2021)は4日齢の女児においてSARS-CoV-2による新生児結膜炎の初報告例を記載した。7)結膜下出血と粘膿性眼脂を呈し、8日間で自然消退した。
Albuquerque et al.(2024)はNeisseria meningitidisが新生児結膜炎の1〜2%を占め、10〜29%が侵襲性疾患に進展するリスクがあると報告した。5)IV cefotaxime 200mg/kg/日の7日間投与で完治が得られた。
Merzouk et al.(2025)は、腸内グラム陰性桿菌(E. coli等)がNICU関連感染において増加傾向にあると報告した。母体のE. coliコロニゼーション率は19.9%、垂直伝播率は21.4%であった。8)
Das(2023)は、韓国の研究で新生児結膜炎の1.2%をAcinetobacter baumanniiが占め、52.4%がS. aureusであったと報告した。6)多剤耐性A. baumanniiによるNICU関連院内感染が問題となっている。
コクランレビュー(Malik and Gilbert 2022)では、予防薬の種類による優劣は現時点では確立されていないと結論づけており、最適な予防薬の選択は今後の研究課題である。2)
Law et al.(2024)は、治療遅延により眼窩蜂窩織炎に進展した新生児結膜炎の2症例を報告した。3)早期の診断・治療介入の重要性が改めて示された。
Asiamah R, Owusu G, Amoako PT, et al. Epidemiology of ophthalmia neonatorum: a systematic review and meta-analysis. BMC Pediatr. 2025;25:31.
Malik ANJ, Gilbert C. Cochrane corner: interventions for preventing ophthalmia neonatorum. Eye. 2022;36:356-357.
Law NL, Tan VC, Lim TH, et al. Ophthalmia neonatorum complicated with neonatal orbital cellulitis: A case series. Malays Fam Physician. 2024;19:5.
Nwokeji I, Ding K, Ketner S. A Case of Neonatal Chlamydial Conjunctivitis. Cureus. 2024;16(7):e64463.
Albuquerque C, Dias ME, Pelicano M, et al. Neisseria meningitidis: The Unforeseen Agent of Acute Neonatal Conjunctivitis. Cureus. 2024;16(7):e65681.
Das G. Acinetobacter baumannii ophthalmia neonatorum - A very rare presentation. Indian J Ophthalmol. 2023;71:2595-2597.
Mechel E, Trinh M, Kodsi S, et al. Ophthalmia neonatorum as the presenting sign of SARS-CoV-2. J AAPOS. 2021;25:230-231.
Merzouk B, Schwartzman K, Yossuck P, et al. A Rare Case of Neonatal Escherichia coli Conjunctivitis With Maternal Asymptomatic Bacteriuria. Cureus. 2025;17(9):e92936.