特発性頭蓋内圧亢進症(IIH)は原因不明の頭蓋内圧上昇を特徴とし、偽脳腫瘍とも呼ばれる。
肥満体型の出産可能年齢の女性に好発し、肥満の流行に伴い世界的に発症率が上昇傾向にある。
乳頭浮腫 が主要な眼科的所見であり、未治療では進行性の視神経萎縮 ・失明に至りうる。頭痛・一過性視覚消失・拍動性耳鳴が三大症状であり、修正Dandy基準に基づく除外診断を行う。
第一選択薬はアセタゾラミド であり、すべての肥満患者に5〜10%の減量が推奨される。
薬物治療抵抗例には視神経 鞘切開術・CSFシャント術・静脈洞ステント留置術が選択される。
再発率は8〜38%であり、体重管理の継続が再発予防に重要である。
特発性頭蓋内圧亢進症(idiopathic intracranial hypertension; IIH)は、偽脳腫瘍(pseudotumor cerebri)とも呼ばれ、原因不明の頭蓋内圧上昇を特徴とする神経眼科疾患である。乳頭浮腫が主要な眼科的所見であり、未治療では視神経萎縮・失明に至りうる。1937年にDandyが診断基準を確立し、現在は修正Dandy基準として使用されている。
疫学 :米国での発症率は一般人口10万人あたり0.9〜1.0人。女性は1.6〜3.5人、過体重女性では7.9〜20人と高い。米国1997〜2016年のデータでは年間発症率1.15/10万人が報告されており1) 、女性1.97/10万に対し男性は0.36/10万と著明な性差がある1) 。最高発症率は18〜44歳の2.47/10万1) である。人種差もあり、黒人2.05、白人1.04、ヒスパニック0.67、アジア太平洋諸島民0.16/10万と報告されている1) 。IIHの有病率は肥満の流行に伴い世界的に上昇傾向にある1) 。
以下に発症率の主要な数値を示す。
対象群 発症率(/10万人) 一般人口(米国) 0.9〜1.15 女性 1.97 過体重女性 7.9〜20 男性 0.36
男性患者は成人IIH患者の10%未満だが、視機能予後が女性より悪い傾向がある。思春期前では肥満・女性への偏りはない。
Q 特発性頭蓋内圧亢進症は男性にも発症するか?
A 男性は成人IIH患者の10%未満だが罹患しうる。男性では視機能予後が女性より悪い傾向があることが知られており、診断が遅れやすい点も注意を要する。思春期前の小児では性別・肥満への偏りはない。
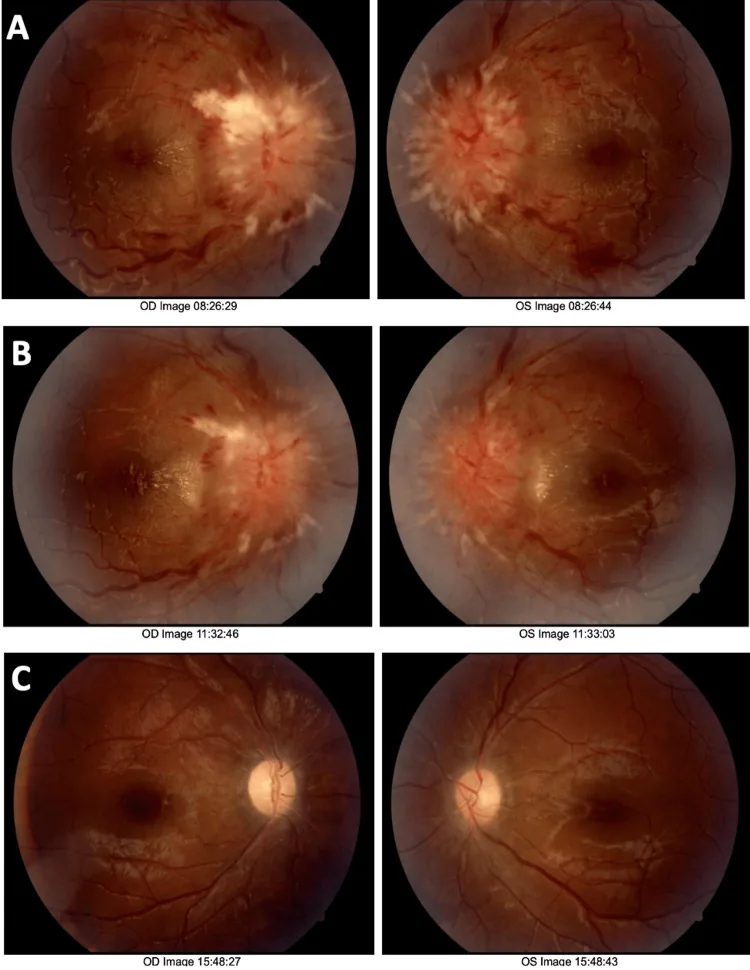
pseudotumor cerebri papilledema follow up fundus When One Tap Isn’t Enough: A Case of Pseudotumor Cerebri Requiring Venous Sinus Stenting. Cureus.; 17(10):e94778. Figure 1. PMCID: PMC12619920. License: CC BY.
Fundus photography. (A) Initial fundus photograph demonstrates severe papilledema with elevated, blurred optic disc margins and obscuration of vessels on and leaving the optic disc. (B) Two-week follow-up shows minimal improvement in papilledema. There is evidence of reduced hemorrhage; however, disc elevation and blurred margins remain unchanged. (C) Ten-month follow-up demonstrates significant improvement in papilledema, with clear disc margins and resolution of disc elevation. The image shows peripapillary atrophy in both eyes, highlighting residual damage resulting from elevated intracranial pressure.
頭痛 :最多の症状で約90%に出現。びまん性・非特異的で悪心・嘔吐を伴うことがある。初期は起床時に悪化する頭蓋内圧上昇性頭痛として始まり、経時的に片頭痛 様(光過敏・音過敏を伴う)に変化する2) 。一過性視覚消失(transient visual obscurations) :68%で報告2) 。通常数秒間持続し、体位変換やバルサルバ法後に生じる。拍動性耳鳴(pulsatile tinnitus) :52%で報告2) 。心拍に同期した片側性の拍動音で、IIHの診断において特異性が高い。視覚障害 :約33%が視力 低下で受診。周辺視野障害(鼻下側欠損・弓状暗点・高度視野狭窄)が主体で、視力低下は通常遅発である2) 。水平複視 :外転神経(第VI脳神経)麻痺に伴い出現。背部痛 :53%で報告2) 。その他、めまい・光過敏・頸部痛・神経根痛も生じうる1) 。
乳頭浮腫(papilledema) :IIHの決定的徴候。通常は両側性・対称性だが片側性・非対称性もある。Frisénスケールで重症度を分類する。乳頭浮腫を伴わないIIH症例も少数報告されている2) 。外転神経麻痺 劇症型IIH(fulminant IIH) :少数に発生。急性発症で数週間以内に重度の視力低下をきたす。初回LP平均CSF初圧は541 mmH2O(29〜70 cm H2O)と極めて高値。治療後も50%が法的盲となり、全例に残存視野欠損 と視神経萎縮を認める2) 。初診時pRNFL が高いほど長期視覚転帰が不良。HVFベースラインMDが-7 dB未満では視力回復が困難である2) 。
Q 乳頭浮腫がなければ特発性頭蓋内圧亢進症ではないのか?
A 乳頭浮腫はIIHの決定的徴候だが、乳頭浮腫を伴わないIIH症例も少数報告されている2) 。一方で、偽乳頭浮腫(視神経乳頭ドルーゼン など)との鑑別が重要であり、光干渉断層計 (OCT)や自家蛍光などの精査が必要となる。
IIHの病因は未解明だが、以下のリスク因子が明らかになっている。
肥満 :最も確立されたリスク因子。出産可能年齢の女性での肥満が最大のリスクとなる1) 。内分泌疾患 :アジソン病、副甲状腺機能低下症、ステロイド 離脱。ホルモン変動 :妊娠、閉経、ホルモン避妊薬使用。アンドロゲン異常 :調節異常の関与が示唆されている2) 。関連全身疾患 :OSA・甲状腺機能低下症・貧血・SLE ・ベーチェット病 ・PCOS・凝固障害・尿毒症。乳頭浮腫患者の10%に治療可能な鉄欠乏性貧血が認められる2) 。関連薬剤 :テトラサイクリン系、ビタミンA誘導体(レチノイン酸など)、リチウム、同化ステロイド、経口避妊薬、ナリジクス酸、シクロスポリン 、組換え成長ホルモン。薬剤性はほぼ投与開始との時間的関連がある2) 。遺伝的要因 :家族内発症の報告あり。ゲノムワイド関連研究で染色体5・13・14番に候補領域が同定されているが、メンデル遺伝のパターンは確立されていない1) 。
IIHは肥満単独とは異なる全身性代謝疾患として認識が進んでいる2) 。
Q どの薬剤が特発性頭蓋内圧亢進症のリスクを高めるか?
A リスクが指摘されている薬剤には、テトラサイクリン系抗菌薬・ビタミンA誘導体(レチノイン酸など)・リチウム・同化ステロイド・経口避妊薬・ナリジクス酸・シクロスポリン・組換え成長ホルモンが含まれる。これらは投与開始との時間的関連が認められることが多い2) 。疑わしい薬剤がある場合は速やかに主治医に相談する。
IIHは除外診断であり、以下の修正Dandy基準(5項目)をすべて満たすことが必要である。
頭蓋内圧上昇の徴候・症状(頭痛・悪心・嘔吐・一過性視覚消失・乳頭浮腫)
外転神経麻痺を除く局在性神経学的徴候がない
CSF組成正常、初圧 >25 cm H2O
画像で水頭症・腫瘤・構造的/血管的病変なし
頭蓋内圧上昇の他の原因なし
LP初圧25〜30 cm H2Oは境界域であり、多くの神経眼科医は再評価を検討する2) 。肥満・鎮静下の小児では28 cm H2Oまで正常の場合がある。
MRI + MR静脈造影(MRV) :第一選択の神経画像。後極部平坦化・空鞍/部分的空鞍・ガドリニウム造影での篩板前視神経増強・視神経周囲クモ膜下腔拡張・眼窩 内視神経蛇行・横静脈洞狭窄などの特徴的所見を確認する。眼科検査 :散瞳 下眼底検査 ・視野検査 (Humphrey 30-2)・視神経写真・視力・色覚検査を行う。偽乳頭浮腫との鑑別 :視神経乳頭ドルーゼン・異常乳頭・遠視 /近視 との鑑別に、自家蛍光またはOCT enhanced depth imagingが有用である2) 。
側臥位で測定し、初圧 >25 cm H2Oで異常と判断する。CSFはタンパク正常/低値、グルコース・細胞数正常が典型的所見である。貧血のスクリーニングも乳頭浮腫患者に推奨される(10%に鉄欠乏性貧血)2) 。
鑑別すべき主な疾患を以下に示す。
頭蓋内占拠性病変(腫瘍・膿瘍)
閉塞性水頭症・髄液吸収障害(感染性髄膜炎後・クモ膜下出血)
静脈還流閉塞(静脈洞血栓症・頸静脈圧迫)
偽乳頭浮腫・視神経乳頭炎・高血圧性視神経症・CRVO ・ION・LHON
急性発症の鑑別:悪性高血圧・髄膜炎・脳静脈疾患・視神経炎 (MOG抗体 関連疾患・NMOSD )・視神経浸潤(白血病・リンパ腫)
治療目標は頭蓋内圧症状の緩和と視機能保護の2つである。
減量 :すべての肥満患者に推奨。5〜10%の減量で症状・徴候が改善し、乳頭浮腫・頭痛・頭蓋内圧が減少する。ただし急性期には不十分なため、他の急性期治療と併用する。体重維持 :体重変動の回避が再発予防に重要である。肥満外科手術(bariatric surgery) :病的肥満での選択肢。BMI 20.5 kg/m²まで低下し再発なしの症例が報告されている2) 。診断的腰椎穿刺 :急性期症状を一時的に緩和するが、長期治療との併用が必要である。
アセタゾラミド(acetazolamide) :IIHの第一選択薬。炭酸脱水酵素阻害薬 としてCSF産生速度を低下させる。軽症例では500 mg×2/日から開始し、漸増で1,000 mg×2/日まで増量する2) 。劇症型では500 mg×3/日から開始し3〜4 g/日まで急速漸増する2) 。副作用による忍容性の問題が生じることがある2) 。IIHTT(Idiopathic Intracranial Hypertension Treatment Trial、2014年、165人のRCT)では、アセタゾラミド+減量はプラセボ+減量と比較して視野平均偏差を有意に改善した(1.43 dB vs 0.71 dB改善)。乳頭浮腫グレードが高い患者ほど効果が顕著であった。トピラマート(topiramate) :弱い炭酸脱水酵素阻害作用を持つ抗てんかん薬 。頭痛改善・減量効果を有し、視覚症状に対する有効性はアセタゾラミドと同等である。フロセミド(furosemide) :ループ利尿薬。頭蓋内圧低下効果はやや限定的。アセタゾラミド不耐時の代替としてスピロノラクトンとともに選択肢となる2) 。ステロイド :長期使用は推奨されない(体重増加・中止後リバウンドのリスク)。劇症型IIHでの短期IV methylprednisolone 1 g/日×3日は北米で一般的だが、英国では成人に通常使用されておらず、エビデンスは不足している2) 。
薬物治療抵抗性・進行性視力障害・難治性頭痛・重度/急速進行性視野欠損に適応となる。
視神経鞘切開術
ONSF(optic nerve sheath fenestration) :重度視力障害+乳頭浮腫があるが頭蓋内圧症状が軽い場合に選択される。
成績 :80〜90%で視力維持/回復。
注意 :経験豊富な術者が必要。頭痛の改善効果は低い。
CSFシャント術
LPシャント(腰椎腹腔)またはVPシャント(脳室腹腔) :視力障害と頭蓋内圧症状の両方がある場合に最適。
特徴 :IIH患者は脳室が拡大していないためVPは技術的に困難だが合併症率が低い。
注意 :シャント不全・感染のリスクあり。
静脈洞ステント留置術
VSS(venous sinus stenting) :横静脈洞狭窄に基づく比較的新しい術式。
機序 :MRVで狭窄部位を特定し、圧較差10 mmHg以上で適応。静脈圧低下→CSF吸収促進→頭蓋内圧低下。
注意 :施設の経験・術者の利用可能性に基づいて選択する。
小児でも治療アプローチは同様だが、視野検査が不正確になりやすいため外科的介入をより早期に検討する。
予後 :疾患経過は数週間〜数年と多様。治療後は通常改善または安定するが、完全回復に至らない患者も多い。永久的な視力障害の独立危険因子は男性・黒人・病的肥満・貧血・OSA・急性発症(劇症型IIH)である。再発率は8〜38%で、体重増加が再発に関連する。IIH患者(女性)は心血管疾患リスクが2倍に増加することも報告されている1) 。
Q アセタゾラミドの副作用で服用できない場合、代替治療はあるか?
A 代替薬として、弱い炭酸脱水酵素阻害作用を持つトピラマートや、ループ利尿薬のフロセミド、スピロノラクトンが選択肢となる2) 。これらでも管理が困難な場合は、視神経鞘切開術・CSFシャント術・静脈洞ステント留置術などの外科的治療が検討される。
Q 特発性頭蓋内圧亢進症は再発するか?
A 再発率は8〜38%と報告されており、体重増加が再発に強く関連する。そのため治療後も体重を安定して維持することが再発予防の要となる。定期的な眼科フォローアップにより、再発の早期発見が可能である。
IIHの病態生理は完全には解明されていない。CSF動態の調節障害と代謝・ホルモン因子の関与が考えられている1) 。
頭蓋内圧-容積の関係 :頭蓋内圧はS字型の圧-容積曲線を示す。容積が30 cm³増加するまでは代償機構(静脈血の頭蓋外排出)によりICP変化は軽微だが、代償機構が消耗されると急激なICP上昇が生じる1) 。
横静脈洞狭窄 :IIH患者の93%に両側性横静脈洞狭窄が認められるとの報告があるが、一次的原因か二次的結果かは不明である。静脈洞狭窄→静脈圧上昇→CSF吸収障害→ICP上昇という悪循環が提唱されている1) 。
主な病態仮説(すべて未確定)を以下に示す。
腹腔内圧上昇 :肥満→腹腔内圧上昇→心充満圧上昇→脳静脈還流障害→頭蓋内静脈圧上昇。非肥満症例を説明できない点が弱点。ビタミンA :IIH患者で血清・CSF中のビタミンA・レチノール・レチノール結合タンパク質が上昇。CSF中の過剰レチノールがCSF再吸収を阻害する理論があるが、大規模研究は未実施。微小血栓 :矢状静脈洞の微小血栓がクモ膜顆粒でのCSF吸収をブロックするとの説。脳室拡大を伴わない点が反論となる。性ホルモン :研究は少なく、さらなる調査が必要。グリア-神経-血管インターフェース :グリア細胞・神経・毛細血管の複雑な相互作用がICP上昇に関与する新たなメカニズム候補として注目されている1) 。
IIHは肥満単独とは異なる全身性代謝疾患として認識が進んでいる2) 。インスリン抵抗性・アンドロゲン調節異常・副腎皮質ホルモン代謝変化など、複数の代謝経路が関与する複合疾患としての理解が深まっている。
アセタゾラミドのICP低下効果は限定的である可能性が示唆されており、新規薬剤標的の探索が進んでいる1) 。オクトレオチド (成長ホルモン・IGF阻害薬)の頭蓋内圧減少効果が評価されている。11β-ヒドロキシステロイド脱水素酵素1型(11β-HSD1)阻害薬なども候補として研究されている。
Bonelliら(2024)は、現時点で高品質エビデンスに基づく外科的介入の推奨が不足していると指摘した2) 。静脈洞ステント留置術(VSS)とCSFシャント術を直接比較するランダム化比較試験(RCT)の実施が求められている。
研究優先課題として以下が挙げられている1) 。
IIHの病因解明
頭痛の発症機序と薬物療法
急性 vs 緩徐な視力低下の差異と予測因子
視機能モニタリング法・バイオマーカー の開発
ホルモンの影響・減量介入の役割
Toshniwal SS, Kinkar J, Chadha Y, et al. Navigating the Enigma: A Comprehensive Review of Idiopathic Intracranial Hypertension. Cureus. 2024;16(3):e56256.
Bonelli L, Menon V, Arnold AC, Mollan SP. Managing idiopathic intracranial hypertension in the eye clinic. Eye. 2024;38:2472-2481.
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト) してください