直接浸潤による所見

多発性骨髄腫の眼症状
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. 多発性骨髄腫の眼症状とは
Section titled “1. 多発性骨髄腫の眼症状とは”多発性骨髄腫(Multiple Myeloma; MM)は、免疫グロブリン(Ig)を産生する形質細胞が制御不能に増殖する悪性疾患である。血液関連悪性腫瘍の約10%を占め、診断時の年齢中央値は65〜70歳。50歳以上の男性に多い。
MMは全身疾患であり、眼瞼・虹彩・角膜・網膜・視神経・脳を含む多彩な眼症状を呈する。眼症状の主な機序は2つある。
- 直接浸潤:形質細胞腫瘤による眼内・眼周囲構造への圧迫と破壊。
- 過粘稠度:異常免疫グロブリンの増加による血液粘稠性亢進。網膜血管の血流停滞・閉塞をきたす。
神経眼科的所見が最も多く、MM患者の約50%にみられる。眼窩内浸潤はMMの初期所見となることがあるため、眼科医が全身疾患発見の端緒となりうる。治療を行った場合の生存期間中央値は約7年である。
神経眼科的所見がMMの眼合併症のなかで最多であり、患者の約50%にみられる。眼窩内浸潤がMMの初発症状となることもあるため、原因不明の眼症状では全身精査が重要である。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”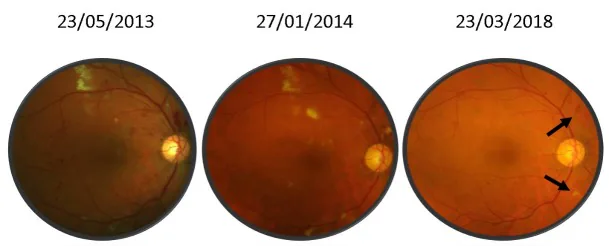
多くの患者は初期には無症状であり、無症状でも多くの眼合併症が潜んでいる可能性がある。症状が出現した場合、以下のものが多い。
- 複視(diplopia):外転神経・動眼神経の障害による眼球運動障害に起因する。
- 眼の痛み・圧迫感:眼窩内腫瘤や骨破壊による疼痛。
- 眼瞼下垂(ptosis):動眼神経障害による。
- 眼球突出(proptosis):眼窩内腫瘤による前方変位。
- 視力低下:視神経圧迫・浸潤、あるいは網膜虚血による。
- 霧視:硝子体出血や黄斑部網膜浮腫に起因する。
- 視野異常:黄斑部出血による中心暗点など。
眼症状は直接浸潤と過粘稠度の2系統に分けて把握すると理解しやすい。
過粘稠度による所見
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”MMの根本原因は形質細胞の制御不能な増殖であり、以下の2系統の機序が眼症状をもたらす。
- 直接浸潤:形質細胞腫瘤が周囲構造を圧迫・破壊する。
- 過粘稠度:異常免疫グロブリンの増加により血液粘稠性が上昇する。血液粘稠度が4センチポアズを超えると眼内の血栓性事象が発生しうる。
MM発症のリスク要因として、電離放射線・ベンゼン・除草剤などへの曝露が挙げられる。また、前駆状態としてMGUS(意義不明の単クローン性ガンマグロブリン血症)が存在し、年率約1%でMMへ移行する。
全身症状としては、貧血・腰痛・蛋白尿の3大症状のほか、高カルシウム血症・腎機能障害・易感染性・骨融解像・病的骨折がみられる。
眼窩内浸潤がMMの初発症状となることがあり、眼科診断が全身疾患の発見につながる場合がある。両眼性の網膜変化や眼球突出など、全身疾患を示唆する眼所見では積極的に血液内科との連携を検討すべきである。
4. 診断と検査方法
Section titled “4. 診断と検査方法”- 眼底検査・眼底写真撮影:網膜出血・静脈拡張・乳頭浮腫などMMに特徴的な所見を検出する。
- フルオレセイン蛍光眼底造影(FA):毛細血管閉塞による無血管領域の検出、色素流入の遅延、灌流障害の定性的診断を行う。網膜静脈の拡張と周辺血管からの漏出も確認できる。
MMの診断は主に血液内科が担うが、眼科医も基本的な検査体系を把握することが重要である。
- 尿検査:Bence Jones蛋白の有無は診断に重要。24時間蓄尿による尿蛋白電気泳動(UPEP)・免疫固定法を行う。
- 血液検査:赤血球増多・M蛋白・高γグロブリン血症の検出。全血算・末梢血塗抹標本・基本代謝パネル。
- 血清蛋白電気泳動(SPEP)・免疫固定法:異常免疫グロブリンのM蛋白を検出する。
- 骨髄生検:形質細胞の異常増殖を確認する。確定診断に不可欠。
- 骨系統検査:レントゲンによる全身骨の溶骨性病変の検索。
MMの診断には以下の所見が用いられる。
| 基準項目 | 閾値・内容 |
|---|---|
| 骨髄クローナル形質細胞 | 10%以上(または形質細胞腫の生検証明) |
| 標的臓器障害(CRAB基準) | Ca >11.5 mg/dL、Cr >2 mg/dL、Hb <10 g/dL、溶骨性病変 |
| 超高リスク(標的臓器障害なし) | クローナル形質細胞が60%以上 |
- 全身疾患の鑑別:くすぶり型骨髄腫・MGUS・POEMS症候群・孤立性形質細胞腫・形質細胞性白血病・ALアミロイドーシス。
- 眼底出血の鑑別:糖尿病網膜症(綿花状白斑・硬性白斑を伴う)、高血圧網膜症(線状出血が主体)と区別する。両眼性であること・ソーセージ様静脈変化がMMを示唆する。
5. 標準的な治療法
Section titled “5. 標準的な治療法”MMの治療は血液内科が主体であるが、眼科医との連携が重要である。
- 化学療法:古典的にはメルファランが用いられてきた。現在ではステロイドとの併用や造血幹細胞移植が標準的。
- 分子標的薬:ボルテゾミブ(プロテアソーム阻害薬)、サリドマイド(血管新生抑制作用あり)、レナリドミド(サリドマイドの誘導体で副作用軽減)が使用される。
- 主な薬剤の組み合わせ例:
- レナリドミド+低用量デキサメタゾン
- ボルテゾミブ+デキサメタゾン
- ボルテゾミブ+サリドマイド+デキサメタゾン
- ビンクリスチン+ドキソルビシン+デキサメタゾン
- 高リスクでない患者:メルファラン+プレドニゾン+サリドマイドを12サイクル後に経過観察。
- 高リスク患者:非アルキル化剤ベースの導入療法2〜4サイクル後、骨髄移植適応を評価。
- 無症状MM:積極的治療が不要な場合がある。
- プラズマフェレーシス(血液浄化):過粘稠症候群に対して施行される。
- その他の支持療法:高カルシウム血症・骨疾患・感染症に対する予防的治療も必要。
全身的化学療法は眼局所に到達しにくいため、眼科的治療の併用が必要となることがある。
眼窩・眼内への放射線療法の線量目安を以下に示す。
| 対象病変 | 放射線量 |
|---|---|
| 眼窩内浸潤 | 20〜40グレイ |
| 虹彩浸潤・白血病網膜症・続発緑内障 | 2.5グレイ×5日間 |
| 視神経浸潤による視力低下 | 7〜20グレイ(大量照射) |
- 結膜への細胞浸潤:全身化学療法が有効。
- 網膜無血管帯・網膜虚血:豆まき状レーザー光凝固術(散瞳下)を施行し、網膜新生血管・硝子体出血を予防する。
- 抗血小板療法・抗凝固療法:網膜静脈拡張・蛇行・CRVO様所見があるとき考慮する。
- 硝子体手術:硝子体出血が自然吸収しない場合に施行する。
- 共同管理:MMを疑う眼科医は血液内科医に紹介する。眼科医は眼症状を定期的に評価し、内科担当医と密に連絡をとることが重要。
眼窩内浸潤には放射線療法(20〜40グレイ)が行われる。過粘稠度網膜症に伴う網膜無血管帯にはレーザー光凝固術を施行して新生血管・硝子体出血を予防する。硝子体出血が自然吸収しない場合は硝子体手術を行う。網膜静脈閉塞様所見では抗凝固療法を考慮する。いずれの治療も血液内科との連携が前提となる。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”形質細胞と免疫グロブリンの異常
Section titled “形質細胞と免疫グロブリンの異常”形質細胞はBリンパ球から分化し、免疫グロブリンを産生する。免疫グロブリンは2本の重鎖(IgG・IgM・IgA・IgE・IgD)と2本の軽鎖(κまたはλ)で構成される。MMでは通常IgGまたはIgAレベルが上昇する。
病勢の進行に伴い、重鎖に対して軽鎖が過剰産生される。κ/λ比のモニタリングにより重症度を評価できる。
細胞遺伝学的異常
Section titled “細胞遺伝学的異常”以下の遺伝子異常の組み合わせがMMの約90%の原因となる。
- サイクリンD1(11q13)・サイクリンD3(6q21)・maf-B(20q11)の活性化。
- 免疫グロブリン重鎖遺伝子座(第14染色体)への転座。
- BCL-2過剰発現によるアポトーシス率の低下。
眼症状の2大機序
Section titled “眼症状の2大機序”- 直接浸潤:腫瘤形成により周囲構造が圧迫・破壊される。眼窩骨破壊による眼球突出・神経圧迫による複視・視力低下が生じる。
- 過粘稠度:ポアズイユの法則に従い、血管内流抵抗は粘稠度に比例して増大する。血液粘稠度が4センチポアズを超えると眼内での血栓性事象が発生しうる。血清の粘性亢進と病的蛋白質による血管内皮細胞障害が眼底病変の主因である。
