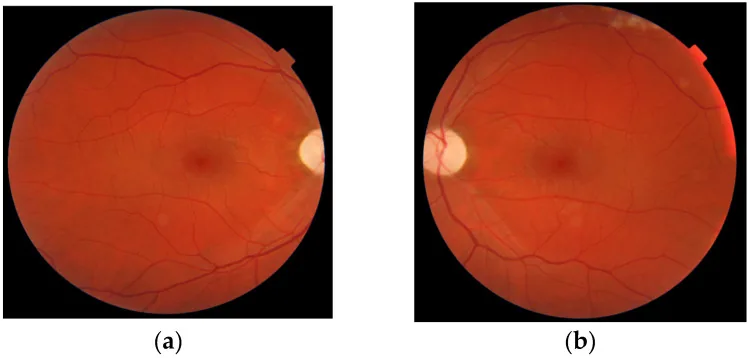
栄養性視神経症(NON)は、ビタミンB群や銅の欠乏によって両眼の視神経 が障害される疾患である。
無痛性・両眼性・対称性の亜急性視力 低下と中心暗点 が特徴的である。
肥満外科手術後・ヴィーガン食・偏食・アルコール依存症が現代における主なリスク要因である。
診断には欠乏栄養素の血液検査と、圧迫性・脱髄性疾患を除外するMRIが必須となる。
早期の栄養補充により視力回復が期待できる。慢性例では回復が限定的となる。
肥満外科手術後の患者は、生涯にわたるビタミン・微量元素のモニタリングが必要となる。
栄養性視神経症(Nutritional Optic Neuropathy;NON)は、栄養欠乏に起因する両眼性・対称性・進行性の視神経障害である。代謝性神経症のグループに属し、中毒性視神経症と同じスペクトラムに位置するが、栄養欠乏を原因とする点で区別される。
主な原因栄養素はビタミンB群(B12・B1・B2・B9)と銅である。これらはミトコンドリアの酸化リン酸化に不可欠な補因子である。
歴史的には飢饉や戦争時に集団発生が報告されてきた。
ストラチャン症候群(1880年代) :ジャマイカのサトウキビ労働者に多発した栄養欠乏性神経症。熱帯性弱視 :ナイジェリアをはじめとしたサブサハラアフリカで報告。戦時捕虜の視神経症 :第二次世界大戦中の日本人捕虜に発生。キューバ流行性視神経症(1991〜1993年) :約5万人が罹患した現代最大の集団発生例。タンザニア流行性視神経症 :類似の集団発生が報告されている。
現代では、肥満外科手術(Bariatric surgery;BS)後の患者や制限食・ヴィーガン食の実践者が新たなリスク群となっている。BS後の患者で神経学的合併症を発症するのは約4.6%であり、内訳は末梢神経障害52%・Wernicke脳症9%・夜盲 症2.8%とされる2) 。
小児においても発症が報告されており、文献レビュー25例中88%が男児、68%が自閉症合併例であった。ビタミンAとB12欠乏が最多の原因であった5) 。
Q 栄養性視神経症はどれくらい珍しい疾患か?
A まれだが見逃されやすい疾患である。歴史的には戦争・飢饉時に多発した。現代では肥満外科手術後患者やヴィーガン食実践者において新たな発症が報告されており、増加傾向にある。
????????????????? Liveta Sereikaite, Alvita Vilkeviciute, Brigita Glebauskiene et al. First Case in Lithuania of an Autosomal Recessive Mutation in the DNAJC30 Gene as a Cause of Leber’s Hereditary Optic Neuropathy. Genes. 2025 Aug 23; 16(9):993. Figure 5. PMCID: PMC12470238. License: CC BY.
???????????????????????????????????????????????????????????
視力低下 :亜急性かつ進行性。両眼性・対称性で無痛性である。色覚障害(dyschromatopsia) :赤色が以前より鮮やかに見えないなどの訴えとして現れる。コントラスト感度 の低下中心暗点 :「見ようとする部位での霧視 」として自覚される。その後、進行性の視力低下へと移行する。
視神経乳頭所見 は病期によって変化する。
初期 :正常、または充血(チアミン欠乏では乳頭浮腫 を生じることがある)中期 :乳頭耳側蒼白(temporal pallor)後期 :びまん性視神経乳頭蒼白(視神経萎縮 )
その他の所見は以下の通りである。
RAPD (相対的瞳孔求心路障害)対光反応 :保たれていることが多い。対光反応に関与するγ細胞が保存されるためである。視野 :中心暗点または盲点中心暗点(centrocecal scotoma)。乳頭黄斑 線維束の選択的障害による。VEP OCT 所見RNFL (網膜神経線維層)正常。乳頭黄斑線維束(耳側)から菲薄化が始まり、全象限に拡大する。RNFL菲薄化は発症3か月以降に検出される6) 。一方、GCL(網膜神経節細胞 層)はRNFL変化に先行してびまん性菲薄化を認めることがある1) 4) 。
Q OCTで異常がなくても栄養性視神経症の可能性はあるか?
A ある。RNFLの菲薄化は発症後3か月以降に検出されるため、初期ではOCTが正常でも視機能障害が生じている可能性がある6) 。GCL解析ではRNFLに先行して異常を検出できる可能性があり1) 4) 、VEPは機能的な視路障害をより早期に捉えられる場合がある。
ビタミンB群
ビタミンB12(コバラミン) :栄養欠乏性視神経症の最重要原因。悪性貧血・亜急性連合性脊髄変性症・末梢神経障害を伴うことがある。
ビタミンB1(チアミン) :糖質代謝に関与。欠乏で脚気、Wernicke脳症(意識障害・記憶障害・眼球運動障害 )を生じる。
ビタミンB6(ピリドキシン) :神経伝達物質の生合成に関与。抗結核薬イソニアジドがB6代謝に拮抗し、欠乏を惹起する。
ビタミンB9(葉酸) :プリン・ピリミジン合成の補酵素。欠乏で巨赤芽球症と感覚障害優位のポリニューロパチーを生じる。
銅
銅(Copper) :酸化リン酸化・細胞代謝の補因子。銅依存性酵素(酸化還元酵素・モノオキシゲナーゼ)の機能不全を招く。
胃バイパス手術後患者の10〜20%で神経症の原因となる。欠乏症は術後3年以上を経て発症することが多いが、栄養不良を合併した例では術後18か月での発症も報告されている6) 。
肥満外科手術(Bariatric surgery) :Roux-en-Y胃バイパス・胆膵路転換術など。術後1.5〜3年での発症が多い。B1・B6・A欠乏では術後7か月での発症例もある2) 。厳格なヴィーガン・ベジタリアン食 :B12・B1・B9欠乏のリスクが高い。偏食・ARFID(回避・制限性食物摂取症) :小児での重要なリスク因子。COVID-19パンデミック後、正常発達児のNONが増加している5) 。アルコール依存症 :直接の原因ではないが、B12・B9欠乏を高頻度に伴う。炎症性腸疾患(IBD)・セリアック病 :B12・葉酸の吸収不良を来す。悪性貧血 :内因子欠乏によるB12吸収不良。消化管手術歴 :Whipple手術・結腸切除などの既往4) 。不適切な経静脈栄養 :ビタミン補給なしの場合、急性チアミン欠乏のリスクがある。
バランスのとれた食事が最良の予防策です。
肥満外科手術を受けた方は、術後も生涯にわたるビタミン・微量元素のモニタリングと補充が必要です。定期的な採血検査を欠かさないようにしてください。
ヴィーガン食を実践している方は、ビタミンB12のサプリメントが必須です。
偏食のあるお子さんは、定期的な栄養状態の評価をかかりつけ医に相談してください。
Q 肥満外科手術後はどのくらいの期間で視神経症が発症するのか?
A 一般的には術後1.5〜3年での発症が多い。銅欠乏は通常3年以上を経てから発症するが、栄養不良を合併した症例では術後18か月での発症も報告されている6) 。複数の栄養素が欠乏する例では、より早期に発症する可能性がある2) 。
スネレン視力検査
対座法視野検査
石原式色覚検査またはFarnsworth D15テスト(色覚異常 の確認)
アムスラー格子
視神経・網膜 の直像鏡検査
スウィンギング・フラッシュライト・テスト(RAPD確認)
視野検査(HVF) :中心暗点または盲点中心暗点を確認する。VEP :振幅減少・潜時ほぼ正常。OCTが正常でも機能的障害を検出できる6) 。OCT(RNFL・GCL解析) :RNFLは初期正常。GCL解析はRNFL変化に先行して異常を検出できる可能性があり、早期診断・経過モニタリングに有用である1) 4) 。網膜電図 MRI(脳・眼窩 ) :圧迫性・脱髄性疾患を除外するために必須である。
CBC・末梢血塗抹標本・総合代謝パネル
血清ビタミンB12・葉酸
ホモシステイン・メチルマロン酸(MMA):B12低値〜境界値の場合に追加する。MMAはB12欠乏でのみ上昇し、葉酸欠乏では正常であるため鑑別に有用である。
血清銅・セルロプラスミン
血清チアミン(B1)・ピリドキシン(B6)
以下の疾患との鑑別が重要である。
疾患 主な鑑別ポイント Leber遺伝性視神経症(LHON ) 母系遺伝・mtDNA変異検索 常染色体優性視神経萎縮(ADOA) RNFLとGCLが初期から同時障害 中毒性視神経症 エタンブトール・メタノールなどの薬剤歴 圧迫性視神経症 頭部画像診断で除外(見逃し厳禁) 視神経炎 眼球運動時痛の有無が重要な鑑別点 黄斑症 蛍光眼底造影 ・局所網膜電図で鑑別
なお、LHONは喫煙が発症に関与するとする報告もあり、ATP不足というミトコンドリア機能障害の共通機序を持つ点でNONとの類似性が認識されている。
Zainuddinら(2025)が引用するSpinazziの診断基準は以下の3項目からなる6) 。
代替診断(炎症性・非炎症性視神経症)の除外
視神経症を引き起こすことが知られる微量栄養素欠乏の生化学的検出
補充療法に対する臨床的・検査的反応の改善
原因となる栄養素欠乏の是正が治療の柱となる。多職種アプローチ(眼科・消化器内科・臨床心理・栄養士・生化学)が推奨されている6) 。
経口投与(可逆的原因) :1,000μg/日を少なくとも1か月継続し、以後同量を維持する。軽度欠乏では100〜500μg/日に減量してもよい。筋注(不可逆的原因・重症例) :1,000μg/日×1週間→1,000μg/週×1か月→維持量1,000μg/月を無期限継続する。投与経路は経口・経鼻・舌下・皮下・筋注から選択できる。
1〜5mg/日を投与する。治療は欠乏の原因が是正されるまで3〜6か月継続する。
Wernicke脳症では100〜1,000mgを投与する。BS後の欠乏例では経口100mg×3回/日×3日後に100mg/日を継続した報告がある2) 。
経口ピリドキシン100mg/日を投与する2) 。イソニアジド内服中の患者ではB6補充が特に重要である。
経口銅グルコン酸を用いる。Moseniaら(2024)の報告では、4mg×2回/日×1か月の後に維持量2mg×2回/日で継続した4) 。同報告では6か月で血清銅レベルが正常化し、2年後に視力が手動弁→20/25 OD・20/40 OSに改善した。
**完全静脈栄養(TPN)**と銅補充を組み合わせる6) 。
重度栄養欠乏が持続する場合、胃バイパス術の正常解剖への再建(revision surgery)も選択肢となる6) 。
術式によって推奨補充内容が異なる。
胃バンディング術 :葉酸・鉄・カルシウム・チアミン・ビタミンDを含むマルチビタミンを継続する。その他のBS術式 :上記にビタミンB12とミネラルを追加する。
中毒性視神経症(エタンブトール視神経症 など)では、原因薬剤の中止が原則である。EB中止後も3か月は症状が進行しうるため、ビタミンB12内服・亜鉛製剤・マグネシウム製剤で回復を待つ。
喫煙は視神経症に対する相加的悪影響があるため、禁煙を指導する。
高血圧・糖尿病など血流に影響する基礎疾患の管理も考慮する。
Q ビタミン補充で視力は回復するか?
A 早期発見・早期治療であれば良好な回復が期待できる。銅欠乏の例では補充開始から2年後に視力が大幅に回復した報告がある4) 。一方、診断が遅れた慢性例では視力回復が限定的となることがある3) 。3か月以内の治療開始が良好な転帰につながる可能性が高い。
ビタミンB群・銅はATP産生に関与するミトコンドリアの酸化リン酸化に不可欠である。これらが欠乏すると、電子伝達系が遮断されてATPが減少するとともに、遊離基(スーパーオキシドアニオン)が蓄積して酸化ストレス が増大する。
乳頭黄斑線維束が選択的に障害されるのは、この線維束を構成するparvocellular RGC(小細胞型網膜神経節細胞)のミトコンドリア予備能が限定的であり、アポトーシス 閾値が低いためとされる4) 6) 。タバコ・アルコール視神経症の機序も同様で、p細胞のATP消費が激しいために優位に障害される。
中毒性・栄養性視神経症ではGCL(網膜神経節細胞層)がRNFL(網膜神経線維層)に先行してびまん性に菲薄化することが、複数の症例報告で確認されている1) 。RGC死にはミトコンドリア機能障害・カスパーゼ活性(特にcaspase-7)・ニューロトロフィン欠乏が関与する1) 。
遺伝性視神経症(ADOA)ではRNFLとGCLが初期から同時に障害される点が、NONとの対照的な違いとなる1) 。
Sriramら(2021)は中毒性・栄養性視神経症5例においてRNFLは比較的保たれる一方、GCLがびまん性に菲薄化することを報告した1) 。エタンブトールはRGCに対し興奮毒性(excitotoxicity)を示し、内因性グルタミン酸を介してRGC層を選択的に障害することも明らかとなった。
ビタミンB9・B12欠乏 :プリン合成に蟻酸を使用する反応の補因子として機能する。欠乏すると蟻酸が蓄積し、電子伝達系を阻害してミトコンドリア機能が抑制され、ATP枯渇へと至る3) 。
銅欠乏 :銅依存性酵素(酸化還元酵素・モノオキシゲナーゼ)の機能不全を引き起こす。神経伝達物質変換障害・酸化リン酸化障害・遊離基除去障害が複合的に生じる。
複数の症例報告で、RNFLが正常でもGCLが早期に菲薄化することが確認されつつある1) 4) 。緑内障 領域のデータからは、GCL解析は早期段階でRNFLよりも高感度である可能性が示唆されている4) 。今後、NONの重症度評価・経過モニタリングにGCL解析が標準的に組み込まれることが期待される。
Tengら(2025)は発達正常の小児3例(13〜15歳男児)で選択的偏食(ARFID含む)によるB12欠乏が主因のNONを報告した5) 。文献レビューでは小児NON 25例中68%が自閉症合併、88%が男児であり、自閉症以外のリスク因子(トラウマ性食体験・複数食物アレルギー・ARFID)への認識が重要であると指摘された。
COVID-19パンデミック後に小児の摂食障害が増加しており、発達正常児でのNON報告が新たな課題として注目されている。
Moseniaら(2024)は消化管手術後に銅欠乏性視神経症を発症した1例に銅グルコン酸を補充し、2年後に視力が手動弁(CF )から20/25 OD・20/40 OSに改善したと報告した4) 。RNFLが正常でもGCL菲薄化を検出した点も注目される。
長期の未治療例では回復が限定的であるため、消化管手術後患者への定期的な銅モニタリングの普及が求められる。
Zainuddinら(2025)は胃バイパス後の銅欠乏性NON例で、TPN・銅補充・マルチビタミン投与に加えて正常解剖への胃バイパス再建術を施行し、視力が6/6・N5に改善したと報告した6) 。ただし中心暗点は18か月後も残存した。
再建術は吸収不良を根本的に解決する選択肢として注目されるが、対象症例の選択基準や長期成績の検討が今後の課題である。
Sriram A, Miao Y, Subramanian P, Schultz JS, Zhang C. A differential loss of nerve fiber layer thickness and retinal ganglion cell complex in toxic and nutritional optic neuropathy. Adv Ophthalmol Pract Res. 2021;1:100026.
Khalid MJ, Ayub MA, Kataria S, Hebert M, Parvathaneni A. Concomitant occurrence of peripheral neuropathy and vision loss due to multivitamin deficiency after bariatric surgery. Cureus. 2024;16(5):e59959.
Othman I, Tai E, Kuganasan S, Abu N. Vision loss as a presenting symptom of vitamin B12 deficiency. Cureus. 2024;16(5):e60113.
Mosenia A, Khan S, Aung MH. Visual recovery in a patient with optic neuropathy secondary to copper deficiency. Am J Ophthalmol Case Rep. 2024;36:102197.
Teng RW, Heidary G, Gise RA. Selective diet induced nutritional optic neuropathy in developmentally normal children. Am J Ophthalmol Case Rep. 2025;37:102234.
Zainuddin MZA, Che Hamzah J, Nik Mahmood NRK, Cheng TC, Bastion MLC. Nutritional optic neuropathy: bariatric surgery gone wrong. Cureus. 2025;17(5):e84548.
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト) してください