非動脈炎性前部虚血性視神経症(éåèçæ§åé¨èè¡æ§è¦ç¥çµç)は、視神経乳頭 への血流障害による急性の無痛性片眼性視力 低下を特徴とする。
50歳以上の急性視神経症として最も頻度が高く、米国では年間約6,000人が新規発症する。
小さい視神経乳頭陥凹 (disc at risk)が最大の解剖学的リスク因子であり、患者の最大97%に認める。
高血圧・糖尿病・閉塞性睡眠時無呼吸・夜間低血圧が主要な全身性リスク因子である。
確立された有効な治療法は存在せず、修正可能なリスク因子の管理が現在の中心的アプローチである。
5年以内に15〜30%が反対側の眼にも発症する。
視力・視野の障害は多くの場合永続し、40〜50%が患眼で重度の視覚障害に至る。
非動脈炎性前部虚血性視神経症(Non-Arteritic Anterior Ischemic Optic Neuropathy; éåèçæ§åé¨èè¡æ§è¦ç¥çµç)は、視神経乳頭(optic nerve head; ONH)への血流障害によって生じる非炎症性の視神経症である。急性の無痛性視力低下と視神経乳頭浮腫を主な特徴とする。
虚血性視神経症(ION)は、視神経乳頭から視交叉 後方までのいずれかが侵される疾患群である。部位によって前部(AION)と後部(PION)に分類され、成因によって動脈炎性(A-AION)と非動脈炎性(NA-AION)に分けられる。éåèçæ§åé¨èè¡æ§è¦ç¥çµçは全AIIONの9割以上を占める。
50歳以上の急性視神経症のなかで最も頻度が高い疾患である。米国では年間発症率が10万人あたり2.3〜10.2人、年間約6,000人の新規症例が報告されている。欧州系に多く、黒人・アジア人では低い傾向がある。男女差はほぼなく、平均発症年齢は57〜65歳である。50歳未満の発症は7.5〜25%とされ、この年代ではdisc at risk(小さい視神経乳頭陥凹)のほか視神経乳頭ドルーゼン が重要な背景因子となる。
歴史的には、1817年にJean-Pierre Saint-Yvesが最初の記載を行い、1935年にC. Miller Fisherが詳細な臨床的記述を行った。1970年代初頭にSohan Singh Hayreh が “anterior ischemic optic neuropathy” の用語を提唱した。
Q éåèçæ§åé¨èè¡æ§è¦ç¥çµçは反対側の目にも発症するか?
A 5年以内に15〜30%の患者が対側眼にも発症し、中央値は発症後7〜12ヶ月とされている。対側眼にdisc at risk(C/D比0.2未満)を持つ患者は特にリスクが高い。リスク因子の管理が対側眼発症の予防において重要である。
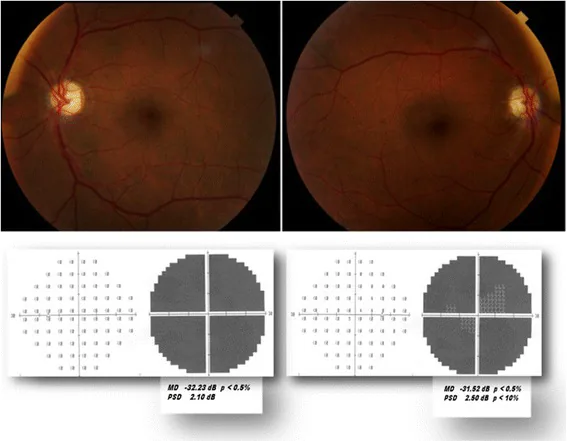
???????????????????????? A Niro, G Sborgia, A Sborgia et al. Hyperhomocysteinemia in bilateral anterior ischemic optic neuropathy after conventional coronary artery bypass graft: a case report. Journal of Medical Case Reports. 2018 Jan 17; 12:11. Figure 1. PMCID: PMC5771151. License: CC BY.
??????????????8?????????????????NAION???????????????????????
急性の無痛性片眼性視力低下が主訴となる。以下の特徴がある。
無痛性 : 眼痛や眼球運動時の痛みは原則としてない。8〜12%で頭痛・眼窩 周囲痛を訴える例があるが、視神経炎 とは異なる。起床時発症 : 70%以上が朝起床時に気づく。夜間低血圧との関連が示唆される。視力の幅 : 光覚なしから1.0以上まで幅広い。Ischemic Optic Neuropathy Decompression Trial(IONDT)では、49%が初期視力20/64(0.3)以上、66%が20/200(0.1)以上であった。視野欠損 色覚異常 羞明
急性期と慢性期では乳頭所見が大きく異なる。
急性期
視神経乳頭浮腫 :急性期に必発。びまん性または分節性(上方・下方いずれかのみ腫脹する水平性が多い)。通常は充血性(発赤腫脹)。蒼白浮腫はまれで、動脈炎性AIIONを示唆する。6〜11週で消失する。
乳頭周囲線状出血 :約75%に認める。浮腫に隣接した線状・炎状の出血である。
RAPD (相対的瞳孔 求心性障害)
僚眼のdisc at risk :対側眼のC/D比が0.2未満の小乳頭陥凹を80〜90%に認める。これはéåèçæ§åé¨èè¡æ§è¦ç¥çµç発症のリスク因子であると同時に、診断を支持する重要な所見である。
慢性期
視神経乳頭の蒼白化 :発症後1〜2ヶ月で乳頭浮腫 が消失し、ゆっくりと視神経萎縮 (乳頭蒼白)に移行する。
網膜神経線維層 菲薄化光干渉断層計 (OCT)で乳頭周囲の網膜神経線維層が菲薄化する。2〜3ヶ月から網膜神経線維層欠損が明確となり、6ヶ月でプラトーに達する。
視野欠損の固定 :急性期を過ぎると視野欠損はほぼ固定する。安定期以降の視力低下の進行は非常にまれである。
視野欠損は水平半盲(特に下方)が最多で、弓状暗点や中心暗点 (約25%)も認める。乳頭周囲網膜 細動脈の狭小化が約2/3に認められる。
Incipient 非動脈炎性前部虚血性視神経症 :無症候性の乳頭浮腫で自然消退することもあるが、25〜45%が顕性éåèçæ§åé¨èè¡æ§è¦ç¥çµçに進行する。偽Foster Kennedy症候群 :片眼にéåèçæ§åé¨èè¡æ§è¦ç¥çµç急性期の乳頭浮腫、対側眼に既発症の視神経萎縮が同時にみられる状態。頭蓋内腫瘍に伴う真のFoster Kennedy症候群との鑑別が必要である。 Q なぜéåèçæ§åé¨èè¡æ§è¦ç¥çµçでは下方の視野が欠けやすいのか?
A 視神経乳頭を養う短後毛様体 動脈(SPCA)が輪状構造をとり、上下で血流が解剖学的に分離されているためである。この血流の分節性により、虚血が上下いずれかの半側に偏りやすく、水平性の半盲・弓状暗点として視野欠損が出現する。
éåèçæ§åé¨èè¡æ§è¦ç¥çµçの大部分は特発性であり、血栓塞栓ではなく一過性の灌流障害(虚血)が主な病因とされる。発症には解剖学的素因と全身・局所の血管的リスク因子が重なって生じると考えられている。
以下の3つの主要リスク因子の頻度・関連度をまとめる。
リスク因子 頻度・関連度 備考 Disc at risk(C/D < 0.2) éåèçæ§åé¨èè¡æ§è¦ç¥çµç患者の最大97% 最大の解剖学的リスク因子 高血圧 IONDT患者の47% 最も多い全身性リスク因子 閉塞性睡眠時無呼吸(OSA) éåèçæ§åé¨èè¡æ§è¦ç¥çµç患者の最大89% リスク比1.7〜3.8倍
Disc at risk(小乳頭陥凹) : C/D比0.2未満、乳頭径1.5mm未満の小さい視神経乳頭。篩状板 で軸索が物理的に圧迫され、軸索輸送障害から浮腫・循環障害の悪循環が生じる。視神経乳頭ドルーゼン : 乳頭内の石灰化沈着。乳頭の混雑を悪化させ、特に50歳未満の若年者でリスクとなる。
高血圧 : IONDT患者の47%に合併。夜間の過度な血圧低下(降圧薬の就寝前内服など)が発症誘因となる。糖尿病 : IONDT患者の24%に合併。IONDT全体の60%に少なくとも1つの血管障害リスク因子が認められた。夜間低血圧 : 70%以上が起床時に症状を自覚し、生理的夜間降圧の過剰や降圧薬の就寝前内服が発症と関連する。閉塞性睡眠時無呼吸(OSA) : éåèçæ§åé¨èè¡æ§è¦ç¥çµç患者の最大89%にOSAが合併し、リスクは1.7〜3.8倍に上昇する。対側眼発症のリスク因子にもなる。CPAPによる予防効果については現時点で確実なエビデンスはない。片頭痛
降圧薬の過剰投与 : 就寝前服用による夜間低血圧が最大の懸念となる。PDE5阻害薬(シルデナフィルなど) : 夜間低血圧を増幅する可能性があり、disc at riskを持つ患者でONH虚血のリスクとなりうる。ただしメタ解析では有意な関連は確認されていない。インターフェロンα : 免疫複合体による乳頭循環への影響が仮説として挙げられているが、因果関係は未確立。GLP-1受容体作動薬(セマグルチドなど) : 後述のセクション7に詳細を記載する。血液透析 : 末期腎不全(ESRD)患者はéåèçæ§åé¨èè¡æ§è¦ç¥çµç発症リスクが3.1倍に上昇する。透析中の低血圧(IDH)が主な発症機序とされている。2)
悪性腫瘍に伴う全身性炎症がまれにéåèçæ§åé¨èè¡æ§è¦ç¥çµçの誘因となりうることが報告されている。炎症性サイトカインによる内皮障害・血栓促進が機序として推定されている。3)
Q 睡眠時無呼吸症候群はéåèçæ§åé¨èè¡æ§è¦ç¥çµçとどう関連するか?
A éåèçæ§åé¨èè¡æ§è¦ç¥çµç患者の最大89%に閉塞性睡眠時無呼吸(OSA)が合併しており、OSAはéåèçæ§åé¨èè¡æ§è¦ç¥çµçのリスクを1.7〜3.8倍高める。睡眠中の間欠的低酸素とONH血流の自己調節障害が発症機序として考えられている。CPAPによる対側眼éåèçæ§åé¨èè¡æ§è¦ç¥çµçの予防効果は現時点では確立されていないが、OSAの治療はリスク管理として推奨されている。
éåèçæ§åé¨èè¡æ§è¦ç¥çµçの診断は主に臨床的に行う。単一の決定的所見はなく、所見の積み重ねで疑いを強め、経過観察を通じて確認する。
以下の所見が揃う場合にéåèçæ§åé¨èè¡æ§è¦ç¥çµçを強く疑う。
急性片眼性の無痛性視力低下
患側にRAPD陽性
視神経乳頭浮腫(充血性・分節性または びまん性)
乳頭周囲線状出血
弓状または水平半盲の視野欠損
僚眼のdisc at risk(C/D比 < 0.2)
視野欠損は最も重要な診断検査である。視力低下が軽度または欠如する場合でも、視野欠損は必ず存在する。
視野検査 (ゴールドマン・ハンフリー自動視野計)血液検査 : 50歳以上では巨細胞性動脈炎 (GCA)除外のためESR・CRP ・血小板を測定する。50歳未満で早期血栓症の既往があれば凝固亢進スクリーニングを考慮する。OCT(光干渉断層計) : 急性期に乳頭周囲RNFLの著明な肥厚を認める。発症後2〜3ヶ月でRNFL欠損が明確となり、6ヶ月でプラトーに達する。disc at riskや視神経乳頭ドルーゼンの同定にも有用である。耳側象限厚128µm以下は良好な視力転帰(20/25以上)と関連し、鼻側象限肥厚105µm未満は良好な視野転帰(VFI 90%以上)と関連するとの報告がある。OCTA (光干渉断層血管撮影)脈絡膜 毛細血管は急性期の一過性低下後に対照レベルへ回復することが報告されている。1) 蛍光眼底造影 (FAG)VEP (視覚誘発電位)MRI : 典型例には不要。痛みが強い場合・経過が非典型的な場合に視神経炎や圧迫性病変の除外のために実施する。éåèçæ§åé¨èè¡æ§è¦ç¥çµçでは視神経の造影効果はない。造影効果がある場合は視神経炎や巨細胞動脈炎関連血管炎を示唆する。
éåèçæ§åé¨èè¡æ§è¦ç¥çµçとAAION(動脈炎性)および視神経炎の主な鑑別点を以下に示す。
鑑別疾患 特徴的な鑑別点 AAION(動脈炎性) 蒼白な乳頭浮腫、顎跛行・頭痛などの巨細胞動脈炎症状、ESR・CRP著明亢進 視神経炎 眼球運動時の眼痛、若年(30〜40代)、MRI造影効果、VEPでP100潜時延長 圧迫性視神経症 緩徐な進行、MRIで腫瘤性病変
その他の鑑別として、鼻性視神経症・浸潤性視神経症・急性乳頭浮腫(頭蓋内圧亢進)なども念頭におく。
確立された有効な治療法は現時点では存在しない。試みられた各治療法のいずれも、有意な視力・視野改善を証明することができていない。
効果未確立の治療
ステロイド 内服眼圧 上昇、肺塞栓)のリスクもある。
アスピリン :初期・最終視力に差なし。
視神経鞘減圧術 (ONSD)
硝子体 内トリアムシノロン
現在の治療戦略
修正可能なリスク因子の管理 :高血圧・糖尿病・脂質異常症のコントロール。
睡眠時無呼吸の治療 :OSAが確認されれば積極的に治療する。
夜間低血圧の回避 :就寝前の降圧薬服用を見直し、過度な夜間血圧低下を防ぐ。
抗凝固・血管拡張薬 :科学的根拠は確立しておらず、一般的には推奨されない。
航空機旅行との関連 :客室内の低酸素環境(高度8,000フィート相当)が血管障害を持つ個人でéåèçæ§åé¨èè¡æ§è¦ç¥çµç発症の誘因となりうることが症例報告から示唆さ��ている。片眼éåèçæ§åé¨èè¡æ§è¦ç¥çµç既往者では長距離飛行前に眼科医への相談が推奨される。
現時点で視力・視野を確実に回復させる治療法は存在しない。
ステロイド内服は最終視力の改善を示せておらず、副作用のリスクも存在する。
同眼での再発率は3〜8%であるが、安定期以降の視力低下の進行は非常にまれである。
対側眼への発症リスク(5年で15〜30%)が高いため、リスク因子管理を継続することが重要である。
透析関連非動脈炎性前部虚血性視神経症 : 血液透析患者では透析セッションの最適化が推奨される。具体的には、週の透析回数の増加、セッション延長、透析液温度の低下(35〜36°C)、透析液カルシウム濃度の増加、透析中の食事回避などが挙げられる。2)
患眼の視力 : 40〜50%が患眼で重度視覚障害または法的盲に至る。同眼再発 : 3〜8%僚眼発症 : 5年以内に15〜30%(中央値7〜12ヶ月)
Q éåèçæ§åé¨èè¡æ§è¦ç¥çµçに有効な治療法はあるか?
A 現時点では確立された有効な治療法は存在しない。ステロイド内服・アスピリン・視神経鞘減圧術などが試みられてきたが、いずれも視力・視野の有意な改善を証明できていない。現在の中心的なアプローチは、高血圧・糖尿病・睡眠時無呼吸・夜間低血圧などの修正可能なリスク因子を管理することで、対側眼への発症を防ぐことにある。
éåèçæ§åé¨èè¡æ§è¦ç¥çµçの発症機序を理解するには、視神経乳頭(ONH)の血管解剖が重要である。
ONHは眼動脈の終末枝である短後毛様体動脈(SPCA)の枝によって主に栄養される。SPCAは眼球後面で10〜20本に分枝する終動脈であり、側副血行路をもたない。各部位の血管支配は以下の通りである。
篩状板前方部 : SPCAの枝と網膜循環由来の毛細血管が混在する篩状板部 : SPCAが直接または Zinn-Haller 動脈輪を形成して栄養する篩状板後方部 : 軟膜血管が担う
発症の主要な機序は血栓塞栓ではなく、一過性の非灌流または低灌流とされている(組織学的にSPCA動脈には加齢性変化のみで明確な塞栓・血栓は認めないことが多い)。
一過性の低灌流 : SPCAによるONH血流の一過性低灌流。眼灌流圧(平均全身動脈圧 − 眼圧)が自己調節能の閾値を下回る。血液脳関門の早期破綻 : 毛細血管透過性亢進により乳頭浮腫が発生する。コンパートメント症候群 : disc at riskで篩状板の非拡張性スペース内に浮腫が蓄積し、組織圧が上昇する。二次的炎症 : グリア・軸索への追加障害が生じる。網膜神経節細胞 のアポトーシス
ONHの血流自己調節には血管内皮からのエンドセリン-1・一酸化窒素(NO)の放出が重要な役割を担っている。加齢、動脈性高血圧・低血圧、糖尿病、脂質異常症、OSA、血管作動薬などがこの自己調節能を障害することで、ONHは全身血圧の変動に対して脆弱になる。
一部の研究者(Levinら)は、éåèçæ§åé¨èè¡æ§è¦ç¥çµçが動脈閉塞ではなく視神経毛細血管の分枝静脈閉塞による可能性を提唱している。éåèçæ§åé¨èè¡æ§è¦ç¥çµçに蒼白浮腫や高度陥凹が乏しい点が根拠として挙げられている。
Phuljheleら(2023)はéåèçæ§åé¨èè¡æ§è¦ç¥çµç患者15眼を対象としたスイープソースOCTA(SS-OCTA)による前向き縦断研究で、乳頭周囲・黄斑部 の微小血管密度を6ヶ月間追跡した。乳頭周囲表層血管密度(wiSPD)は急性期(42.49±5.28)から対照(46.36±2.09、P=0.015)と比較して有意に低下し、6ヶ月でさらに35.66へ進行性低下した。脈絡膜毛細血管層密度(wiPCC)は急性期に有意低下(55.23±4.51 vs 対照60.60±3.17、P<0.001)したのち、3〜6ヶ月で対照レベルに回復した。黄斑の表層・深層血管密度は急性期から有意に低下し6ヶ月まで安定して低値を維持した。6ヶ月時点の視力はwiSPD(R=0.6824、P=0.0002)およびwiRPC (R=0.6217、P=0.0012)と有意に相関した。1)
この所見は、乳頭周囲の微小血管が神経萎縮に伴い進行性に失われる一方、脈絡膜毛細血管の急性期変化は一過性の低灌流または浮腫による信号アーチファクトを反映している可能性を示唆している。黄斑の二次的変化は、視神経萎縮に伴う網膜神経節細胞層の萎縮を反映していると考えられる。
2型糖尿病および過体重患者におけるセマグルチド使用とéåèçæ§åé¨èè¡æ§è¦ç¥çµçリスクの関連が報告され、注目を集めている。
16,827人のマッチドコホート研究(Kaiser Permanente)では、2型糖尿病群においてセマグルチド使用者でのéåèçæ§åé¨èè¡æ§è¦ç¥çµç累積発症率が6.7%であったのに対し、非GLP-1群では0.8%であった。過体重群でも同様のシグナルが観察された。ただし、現時点でAAO (米国眼科学会)およびNANOS(神経眼科学会)はセマグルチドの服薬中止を推奨していない。視機能障害のある患者では主治医への相談が促されている。
OCTAは急性期のONH・乳頭周囲血管密度の変化を定量的に捉えることができ、重症度や視力予後との相関が報告されている。しかし研究間で結果に不一致があり、臨床への応用にはさらなる検証が必要である。1)
Ferreira Sacramentoら(2025)は、糖尿病・高血圧・末梢動脈疾患・両側頸動脈狭窄を持つ67歳男性でéåèçæ§åé¨èè¡æ§è¦ç¥çµç発症後にPET-CTで結腸腺癌(T1N0M0)を発見し、切除後に炎症マーカー(ESR>140 mm/h、CRP 11 mg/dL)の改善とともに視機能が徐々に回復したことを報告した。IL-6・TNF -αなどの炎症性サイトカインによる内皮障害と微小血栓形成が機序として推定されている。3)
悪性腫瘍に伴う全身性炎症がéåèçæ§åé¨èè¡æ§è¦ç¥çµçの誘因となりうることを示唆する症例報告であり、特発性éåèçæ§åé¨èè¡æ§è¦ç¥çµçの一部に腫瘍性背景が潜んでいる可能性を示している。ただし単一の症例報告であり、一般化には慎重な解釈が必要である。
Phuljhele S, Sharma S, Chawla R, Saxena R, Sharma P. Evaluation of optical coherence tomography angiography (OCTA) changes in nonarteritic anterior ischemic optic neuropathy (NAION). Indian J Ophthalmol. 2023;71(5):2020-2026.
Eshtiaghi A, Micieli JA. Hemodialysis-related vision loss from anterior ischemic optic neuropathy. Case Rep Nephrol Dial. 2022;12(1):57-62.
Ferreira Sacramento G, Brito S, Mesquita T. Anterior ischemic optic neuropathy as a paraneoplastic manifestation of colorectal cancer. Cureus. 2025;17(12):e100070.
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト) してください