前眼部病変

結節性多発動脈炎(PAN)の神経眼科的徴候
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. 結節性多発動脈炎(PAN)の神経眼科的徴候とは
Section titled “1. 結節性多発動脈炎(PAN)の神経眼科的徴候とは”結節性多発動脈炎(Polyarteritis Nodosa; PAN)は、中型動脈を主体に侵す全身性壊死性血管炎である。動脈壁の全層に炎症と血管周囲への炎症性細胞浸潤をきたし、フィブリノイド壊死を生じる。
発生率は生検確認例で10万人あたり年間0.7人、有病率は10万人あたり6.3人と稀な疾患である。フランスの多民族集団の報告では100万人あたりの有病率33人、発症率0〜1.6人/年と報告されている1)。通常40〜60歳に発症し、男性にやや多い(男女比1.5:1)1)。日本の教科書では40〜50歳代に好発し性差はないとされる。
全身症状の中で神経症状は頻度が高く、Pagnoux 2010の348例では79%に認められた1)。眼病変は9〜20%に生じ、脈絡膜血管炎・網膜血管閉塞・虚血性視神経症・脳神経麻痺など多彩な神経眼科的徴候を呈する。肺病変は原則としてみられないことが本疾患の特徴の一つである。
B型肝炎ウイルス(HBV)との関連があり、現在HBV関連PANは全体の7〜10%を占める。HBVワクチン普及前は36%を占めていたが普及後に低下した。
眼病変は10〜20%の患者にみられる。脈絡膜血管炎が最も一般的な眼所見であり、脈絡膜毛細血管板の多局性急性虚血は血管炎を強く示唆する。神経眼科的所見(脳神経麻痺、同名半盲など)を含めると影響の頻度はさらに高い。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”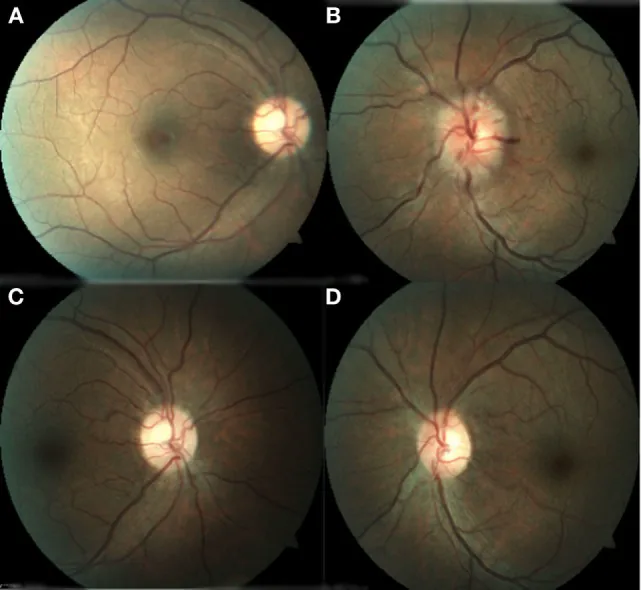
初発症状として全身症状が先行することが多い。
- 発熱・体重減少・全身倦怠感:PANの初発に多く、38℃以上の発熱が2週間以上続くことがある。
- 筋痛・関節痛:半数以上にみられる。
- 精巣痛:PANを強く示唆する症状であり、約20%に認められる5)。
- 末梢神経障害:症例の50〜75%に認められ、手足のしびれや脱力として自覚される。
眼の自覚症状は以下の通りである。
- 視力低下:虚血性視神経症や網膜血管閉塞による急激なものから、慢性的なものまで幅がある。
- 一過性視力障害:網膜血管の一過性虚血により生じる。
- 視野異常:同名半盲など、中枢神経系(CNS)血管炎の部位に応じた視野欠損が生じる。
- 複視:外眼筋麻痺や脳神経麻痺による。
眼病変は多彩であり、前眼部・後眼部・神経眼科的所見に分類される。
後眼部・神経眼科的所見
全身臓器の主な有病率を以下に示す。
| 臓器 | 主な症候 | 有病率(%) |
|---|---|---|
| 末梢神経 | 多発単神経炎 | 50〜70 |
| 腎臓 | 蛋白尿・高血圧・腎不全 | 70 |
| 皮膚 | 紫斑・潰瘍・網状青斑・壊疽 | 50 |
| 筋肉 | 筋肉痛 | 50〜60 |
| 消化管 | 腹痛・消化管出血 | 30〜35 |
| 関節 | 関節炎 | 20 |
| 生殖器 | 精巣梗塞 | 20 |
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”PANの病態生理は完全には解明されていない。環境刺激による遺伝的素因の関与が推定されている。
基本的な病態は、免疫複合体が中型動脈の血管壁に沈着し、壊死をもたらすものである。小動脈および中等大の動脈にフィブリノイド壊死を生じる。
主なリスク・関連因子は以下の通りである。
- HBV感染:PANとの強い関連があり、感染から6か月以内に発症することが多い。血清免疫複合体沈着と補体消費が機序として関与する。HBVワクチン普及後、HBV関連PANは1970年代の36%から7%まで低下した。
- HCV感染:HBVほど強くはないが、関連が報告されている。
- CECR1変異(DADA2):アデノシンデアミナーゼ2(ADA2)欠損症を来し、より若年発症(多くは10歳まで)で脳卒中の頻度が高い。
- 薬剤:ミノサイクリンの3年以上の長期服用で腎PANの発症が報告されている。薬剤中止のみで動脈瘤が消失した症例がある3)。
- COVID-19 mRNAワクチン:接種後7〜28日以内の発症が4例報告されている5)。
- その他:パルボウイルスB19、CMV、EBV、HIV感染、有毛細胞白血病、VEXAS症候群との関連も報告されている1)。
4. 診断と検査方法
Section titled “4. 診断と検査方法”PANを確定する単一の検査は存在しない。臨床所見・検査所見・画像所見・病理所見を組み合わせて診断する。
日本の診断基準
Section titled “日本の診断基準”厚生省難治性血管炎調査研究班(1998年)の基準では、以下10項目の主要症候のうち2項目以上を認め、血管造影所見または血管炎の病理所見があれば確実例とする。
- 発熱(38℃以上、2週間以上)と体重減少(6か月以内に6kg以上)
- 高血圧
- 進行性の腎不全
- 脳梗塞(出血)
- 虚血性心疾患、心膜炎または心不全
- 胸膜炎
- 消化器出血または腸閉塞
- 多発性単神経炎
- 皮膚症状(皮下結節、皮膚潰瘍、壊疽、紫斑)
- 多関節炎または筋炎(筋痛、筋力低下)
血管造影・病理所見がなくても、(1)を含む6項目以上を満たせば疑い例とする。
ACR 1990分類基準
Section titled “ACR 1990分類基準”以下10項目中3項目以上で分類する1)。
体重減少4kg超、網状青斑、精巣痛、びまん性筋痛、単/多発神経障害、拡張期血圧90mmHg超、腎不全、HBV陽性、血管造影異常(動脈瘤・閉塞)、生検で動脈壁に好中球浸潤。
臨床・血液検査
Section titled “臨床・血液検査”- 炎症マーカー:ESR亢進、CRP上昇、軽度白血球増多、血小板増多、慢性貧血。
- ANCA:古典的PANは通常陰性。10%でMPO-ANCA陽性の場合があるが、陽性例は顕微鏡的多発血管炎(MPA)を考慮する。ANCA高値はPANの可能性を大幅に低下させる。
- ウイルス検査:HBV・HCV・HIV血清学を確認する。
- IL-6:活動性と相関し、高値例は関節痛・皮膚潰瘍が多い傾向がある2)。
PANを確定する単一の検査はない。ESR・CRP亢進などの非特異的炎症所見が認められる一方、ANCA・クリオグロブリンは通常陰性であることが手がかりになる。HBV・HCV・HIV血清学の確認も必須である。確定診断には血管造影または組織生検が必要となる。
- 中型動脈の斑状の全層性フィブリノイド壊死、好中球主体の炎症が特徴的である。
- 慢性病変ではリンパ球・マクロファージへの移行と血管新生を認める。
- 壊死と線維化の組み合わせ、隣接する微小動脈瘤と血栓症が典型像である。
- 筋肉・神経の併用生検では、症状のあるPAN患者の80%で血管炎の証拠が得られる(筋肉単独では65%)。
- 生検で肉芽腫・巨細胞を認めた場合はPAN以外の血管炎(GPA・GCAなど)を考慮する。
眼科的・画像検査
Section titled “眼科的・画像検査”- 蛍光眼底造影(FA):脈絡膜毛細血管板の多局性急性虚血の描出に有用。腕網膜循環時間・網膜内循環時間の延長が認められる。
- 頭部MRI:皮質・皮質下の多発性散在病変(灰白質・白質)。ガドリニウム造影・FLAIR画像で小出血性病変と多発性梗塞の併存を確認できる。
- MRA/CTA:腸間膜・腎・肝動脈に多発性微小動脈瘤(1〜5mm)と共存狭窄病変を描出する。動脈狭窄と動脈瘤拡張の交互出現が特徴的な所見である6)。
- 内臓血管造影:生検陰性時や内臓症状主体の場合に施行。メセンテリック・肝・腎の局所性分節性動脈瘤が最大90%で確認される1)。
5. 標準的な治療法
Section titled “5. 標準的な治療法”PANは生命にかかわる疾患であり、診断後は速やかに膠原病専門医と連携して治療を開始する。
全身治療(日本の標準)
Section titled “全身治療(日本の標準)”治療の基本はステロイドパルス療法→経口ステロイド内服→シクロホスファミド点滴の組み合わせである。
- ステロイドパルス療法:急性期の強力な炎症抑制を目的に施行する。
- 経口ステロイド内服:パルス後に開始し、漸減して5〜10mg/日程度で維持する。
- シクロホスファミド(エンドキサン®)点滴:ステロイドと同時進行で施行し、寛解導入を図る。一般的に1〜3回の点滴静注で寛解導入する。
- 維持療法:寛解後はメトトレキサートまたはアザチオプリン(イムラン®)に切り替える。禁忌の場合はミコフェノール酸モフェチルを使用する。
病型別の治療選択も重要である。
- HBV-PAN:抗ウイルス薬+血漿交換(免疫複合体除去)が基本となる。
- DADA2-PAN:TNF阻害薬が有効である。
- 薬剤誘発性PAN(ミノサイクリンなど):原因薬剤の中止のみで寛解が得られる可能性がある3)。
眼病変の種類に応じて以下の治療を行う。
- 乾性角結膜炎:ヒアレイン点眼液(0.1%)1日4〜6回。
- 上強膜炎・ぶどう膜炎:リンデロン点眼液(0.1%)1日2〜6回。
- 前眼部病変全般:ステロイドまたは人工涙液点眼などの対症療法。
- 活動性の網膜血管炎:ステロイド全身投与。ステロイド抵抗性には免疫抑制薬を追加。
- 進行性の網膜血管閉塞:抗凝固療法(ワーファリン2〜5mg/日、PT-INR 1.5〜2目標)。
- 網膜新生血管:網膜光凝固術を速やかに施行する。広範な網膜血管閉塞に対しては予防的にも施行する。
- 増殖性硝子体網膜症:硝子体手術を検討する。
免疫抑制療法中のCMV網膜炎などの日和見感染、ステロイド性中心性漿液性網脈絡膜症、網膜無灌流領域からの新生血管出現に注意が必要である。定期的な蛍光眼底造影を含む眼底検査が推奨される。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”PANの基本病変は中型動脈の壁の全層炎である。
炎症カスケードは以下のように進行すると考えられている。
- 内皮損傷の開始:環境刺激(感染・薬剤など)を契機に直接損傷またはサイトカイン・抗体介在性の内皮障害が生じる。
- 炎症性サイトカインの放出:IL-2・IL-8・IFN-γが高値となり、白血球が動脈中膜に動員される。
- 内弾性板の破壊:好中球浸潤が内弾性板を破壊し、内膜肥厚・浮腫・血栓症を引き起こす。
- 動脈閉塞・動脈瘤形成:血栓症による閉塞と、動脈壁の脆弱化による動脈瘤形成が混在する。血管造影での両者の混在がPANの典型的所見である。
HBV関連PANでは免疫複合体の沈着と補体消費が動脈炎の主要機序となる。
CNS動脈の脆弱化により動脈瘤が形成され、破裂による出血性梗塞が生じることがある。慢性炎症は狭窄と血栓症を招き、虚血性病変の原因となる。眼においては脈絡膜・網膜・視神経への血流障害がさまざまな眼所見を生じさせる。
DADA2(CECR1変異)では、ADA2欠損によりM1型マクロファージが過活性化し、血管壁の炎症と破壊が促進されると考えられている。
Boistaultら(2021)の報告では、難治性PAN小児例でIL-6が106.43 pg/mL(正常0〜4.3 pg/mL)と著明高値であった2)。IL-6高値群は男性に多く、関節痛・皮膚潰瘍が有意に多い傾向を示した。
7. 最新の研究と今後の展望(研究段階の報告)
Section titled “7. 最新の研究と今後の展望(研究段階の報告)”トシリズマブ(IL-6受容体阻害薬)
Section titled “トシリズマブ(IL-6受容体阻害薬)”IL-6受容体阻害薬であるトシリズマブ(TCZ)の難治性PANへの応用が報告されている。
Boistaultら(2021)は11例の難治性PAN(中央値35歳、IQR 23.5〜57.5歳、5例女性)にTCZを投与した報告をまとめた2)。用量はTCZ 8mg/kg 2〜4週ごとの点滴静注、またはTCZ 162mg毎週皮下注射であり、ほとんどの症例で寛解が達成された。
小児PANの1例では、高用量ステロイド+シクロホスファミドに不応の4歳女児にTCZ 8mg/kg 2週ごとを開始したところ、数日で臨床的・生物学的改善が得られ、21か月後も完全寛解が持続した2)。TCZ選択の根拠として、IL-6高値がTNF-αに比して相対的に高かったことが挙げられた。
COVID-19ワクチン関連PAN
Section titled “COVID-19ワクチン関連PAN”COVID-19 mRNAワクチン接種後のPAN発症が4例報告されている。
Ohkuboら(2022)は、ワクチン接種後7〜28日以内のPAN発症症例をまとめた5)。初回接種後の発症が多く、全例がステロイド・免疫抑制薬で改善した。発症機序として、脂質ナノ粒子(LNP)注射による炎症反応→好中球浸潤・炎症性サイトカイン産生が推察されている。
因果関係はいまだ確立されておらず、ワクチンの有益性はリスクを大幅に上回ると考えられている。
薬剤誘発性PANへの非免疫抑制的管理
Section titled “薬剤誘発性PANへの非免疫抑制的管理”Yokotaら(2022)は、ミノサイクリン3年以上服用後に腎PANを発症した症例において、薬剤中止のみで機能的・形態的寛解が得られたことを英語文献で初めて報告した3)。7.5年後の再造影で腎動脈瘤の消失が確認され、ステロイド・免疫抑制薬を使用せずに管理できた。
薬剤誘発性PANでは原因薬剤の中止が最優先であり、免疫抑制療法なしの寛解達成の可能性を示した重要な知見である。
8. 参考文献
Section titled “8. 参考文献”- Ambrogetti R, Taha O, Awan B, et al. Pericarditis of Polyarteritis Nodosa. Cureus. 2023;15(10):e46717.
- Boistault M, Lopez Corbeto M, Quartier P, et al. A young girl with severe polyarteritis nodosa successfully treated with tocilizumab: a case report. Pediatr Rheumatol Online J. 2021;19:168.
- Yokota K, Kurihara I, Nakamura T, et al. Remission of Angiographically Confirmed Minocycline-induced Renal Polyarteritis Nodosa: A Case Report and Literature Review. Intern Med. 2022;61:103-110.
- Waisayarat J, Niyasom C, Vilaiyuk S, et al. Polyarteritis Nodosa with Cytomegalovirus Enteritis and Jejunoileal Perforation: Report of a Case with a Literature Review. Vasc Health Risk Manag. 2022;18:595-601.
- Ohkubo Y, Ohmura S, Ishihara R, et al. Possible case of polyarteritis nodosa with epididymitis following COVID-19 vaccination: A case report and review of the literature. Mod Rheumatol Case Rep. 2022;(epub).
- Robinson C, Yasin Z, Patel P, et al. A Rare Presentation of Polyarteritis Nodosa. Cureus. 2022;14(2):e21925.
