視神経系

COVID-19の神経眼科的徴候
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. COVID-19の神経眼科的徴候とは
Section titled “1. COVID-19の神経眼科的徴候とは”COVID-19の神経眼科的徴候とは、SARS-CoV-2感染(COVID-19)に伴い、視神経・脳神経・視路・瞳孔経路などの神経眼科系が障害される多様な臨床徴候の総称である。
SARS-CoV-2は2019年に中国武漢で最初の症例が報告され、2020年3月にWHOがパンデミックを宣言した。その後223カ国以上に拡大し、7億7,000万人以上の確定症例と約700万人の死亡(WHO)をもたらした。2020年には米国において心疾患・癌に次ぐ3番目の死因となった。重症COVID-19患者の約4%に神経学的合併症が報告されており1)、重症化リスクは60歳以上で基礎疾患を有する者で最も高い。
重症COVID-19の約4%に神経学的合併症が報告されている1)。頭痛はSARS-CoV-2陽性者の最大71%、眼痛は34%に認められる。視神経炎や脳神経麻痺などの神経眼科的徴候は感染中または回復後に出現しうる。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”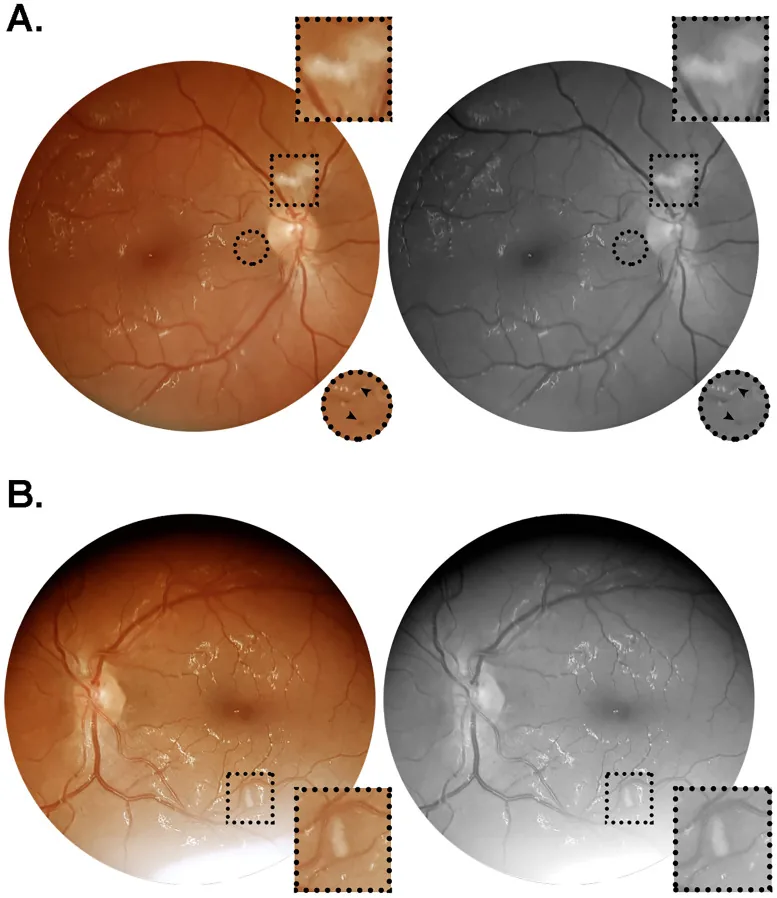
- 頭痛:SARS-CoV-2陽性者の最大71%が報告する。
- 眼痛:34%に認められる。
- 視力低下:視神経炎・視神経梗塞・後可逆性脳症症候群(PRES)などに伴う急性視力低下。
- 複視:第3・4・6脳神経麻痺に伴う。
- 視揺視(oscillopsia):免疫介在性脳炎に伴う症状。
COVID-19に関連する神経眼科的徴候は多岐にわたる。主要カテゴリを以下に示す。
脳神経・眼球運動系
視路・その他
視路障害:脳卒中による同名半盲、皮質盲、読書困難。PRES(後可逆性脳症症候群)による一過性皮質視覚喪失・幻覚性反復視。
特発性頭蓋内圧亢進症(IIH):MIS-Cにより小児で多く報告。
二次感染(ROCM):鼻・眼窩・脳ムコール症。87%にステロイド投与歴あり、78%が糖尿病。
COVID-19後の複視は、主に第3・4・6脳神経麻痺によって生じる。フィッシャー症候群(眼筋麻痺・運動失調・腱反射消失を三主徴とする)、ギラン・バレー症候群、重症筋無力症の文脈で発症することもある。脳静脈洞血栓症(CVST)に伴う場合も報告されている。
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”SARS-CoV-2の特性と神経組織への侵入
Section titled “SARS-CoV-2の特性と神経組織への侵入”SARS-CoV-2はコロナウイルス科に属する、エンベロープを持つ正鎖単鎖RNAウイルスである。スパイク(S)タンパク質がACE2受容体に結合し、宿主細胞に侵入する。ACE2受容体は呼吸器上皮のほか、脳のニューロンやグリア細胞にも発現している。
神経組織への侵入経路として以下が考えられている。
- 嗅神経経路:嗅神経を介した直接的な中枢神経侵入。
- 髄膜・脈絡叢経路:血液脳関門を介さない侵入。
- 血行性経路:ウイルス血症による全身循環を介した侵入。
- 直接的神経損傷:ウイルスによる神経細胞への直接侵襲。
- サイトカインストーム:単球・好中球・Tリンパ球の免疫活性化により局所・全身炎症が惹起され、血管透過性が亢進する。
- 異常な自己抗体産生:抗MOG抗体の陽性化など、免疫介在性の神経損傷。
- 血液高凝固状態:炎症促進状態による脳静脈洞血栓症(CVST)・脳卒中のリスク増大。
- 60歳以上・基礎疾患(高血圧、糖尿病など)の保有
- 重症COVID-19(多臓器不全)
- 高用量ステロイド投与(ムコール症発症リスク)
NA-AIONとの関連
Section titled “NA-AIONとの関連”SARS-CoV-2感染が非動脈炎性前部虚血性視神経症(NA-AION)のリスク因子として報告されている。2)発症機序として、炎症性・自己免疫性の血栓性微小血管障害が推定されている。COVID-19ワクチン接種後にもNA-AIONが報告されている。2)
4. 診断と検査方法
Section titled “4. 診断と検査方法”COVID-19の確定診断
Section titled “COVID-19の確定診断”COVID-19の診断方法を以下に示す。
| 検査法 | 特徴 | 適用時期 |
|---|---|---|
| PCR(鼻咽頭スワブ) | ゴールドスタンダード | 感染第1週 |
| 血清学的検査 | ウイルス抗原に対する抗体検出 | 感染2週目以降 |
感度は完全ではなく、臨床データ・疫学的履歴も併用して診断する。
神経眼科的評価
Section titled “神経眼科的評価”診察では以下の所見を確認する。
視野・電気生理学的検査
Section titled “視野・電気生理学的検査”- 視野検査:視神経炎では(傍)中心暗点、虚血性視神経症(AION)では水平半盲が典型的。
- 視覚誘発電位(VEP):脱髄性疾患では潜時延長、虚血性では振幅低下のみを示す。
- 光干渉断層計(OCT):視神経障害の定量的評価に有用。
- 眼窩部MRI:視神経炎に関連する異常増強効果の同定に有用。冠状断脂肪抑制STIR画像・造影T1強調画像が特に有用。
- FLAIR画像:脱髄病変の評価(MS合併評価)に使用する。
- DWI(拡散強調像):脳卒中・視神経虚血の評価に有用。
視神経炎の鑑別では、虚血性・圧迫性・腫瘍性・鼻性・中毒性・遺伝性の視神経症を除外する。非典型的視神経炎の特徴として以下が挙げられる。
- 15〜45歳以外での発症
- 両眼発症
- 発症後2週間以降の進行
- ステロイド依存性
- 全身症状の合併
抗AQP4抗体・抗MOG抗体の評価も鑑別に重要である。NA-AIONとの鑑別には、年齢・疼痛の有無・視野パターン・VEP所見を参考にする。2)
5. 標準的な治療法
Section titled “5. 標準的な治療法”COVID-19の全身管理には、抗SARS-CoV-2モノクローナル抗体・抗ウイルス薬・免疫調節薬・副腎皮質ステロイドが用いられる。呼吸不全に対してはパルスオキシメトリによる監視と酸素飽和度92〜96%の維持が基本となる。
デキサメタゾンまたはレムデシビルは、脳卒中・けいれん・髄膜炎を含む神経学的合併症の頻度低下と関連することが報告されている。両薬剤の併用では相乗効果が見られ、非低酸素性COVID-19においてもデキサメタゾンが神経学的合併症リスクを低下させた。1)
視神経炎の治療
Section titled “視神経炎の治療”視神経炎の治療は以下の通りである。
| 病型 | 第一選択 | 備考 |
|---|---|---|
| 典型的視神経炎 | ステロイドパルス療法 | 視力回復を早める(最終視力への影響は限定的) |
| 非典型的視神経炎 | ステロイドパルス療法 | 必須適応。NMO・膠原病疑いでは専門科連携 |
- ステロイドパルス療法:メチルプレドニゾロン1,000mg/日を3日間点滴静注する。
- パルス療法後のプレドニゾロン内服は行わない(ONTTの知見に基づく)。
- NMO・膠原病・血管炎症候群が疑われる場合は神経内科等との連携が必要である。
虚血性視神経症(AION)の治療
Section titled “虚血性視神経症(AION)の治療”- 動脈炎性AION(GCA関連):大量副腎皮質ステロイド点滴1g/日×3〜5日間、その後プレドニゾロン内服1mg/kg/日を4〜6ヶ月かけて漸減する。
- 非動脈炎性AION(NA-AION):急性期の視機能障害改善・僚眼発症予防ともに、現時点で明らかな効果のある治療はない。
神経眼科的徴候全般の管理
Section titled “神経眼科的徴候全般の管理”炎症・虚血・高凝固状態・全身異常(高血圧・低酸素症)への対応が基本となる。脳卒中関連では、治療的抗凝固療法・静注血栓溶解療法・機械的血栓回収術が選択肢となる。免疫抑制薬は、活動性感染例では感染合併症リスクに注意して使用する。なお、標準的スクリーニングや確立された意思決定アルゴリズムは現時点で存在しない。
視神経炎の基本治療はステロイドパルス療法(メチルプレドニゾロン1,000mg/日×3日間点滴静注)である。非典型的視神経炎(両眼性・ステロイド依存性・全身合併症など)ではこの治療が必須適応となる。NMOスペクトラム障害や膠原病が疑われる場合は神経内科等との連携が必要である。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”SARS-CoV-2のスパイク(S)タンパク質はACE2受容体に結合して宿主細胞に侵入する。ACE2受容体は呼吸器上皮・食道・心筋細胞・膀胱尿路上皮・腎近位尿細管・脳(ニューロン・グリア細胞)に広く分布している。
神経眼科的徴候の発症機序として、以下の経路が複合的に関与すると考えられている。
- 直接的神経損傷:ウイルスが嗅神経・髄膜・脈絡叢・血行性経路を介して中枢神経に侵入し、ニューロンやグリア細胞を直接障害する。
- サイトカインストーム:単球・好中球・Tリンパ球の活性化により局所・全身炎症が惹起され、血管透過性亢進と肺水腫が生じる。この全身炎症が神経組織の二次的障害につながる。
- 免疫介在性機序:異常な自己抗体産生(抗MOG抗体など)が誘導され、視神経炎やNMOスペクトラム障害を引き起こす。
- 血液高凝固状態:炎症促進状態が持続することで、脳静脈洞血栓症(CVST)や脳卒中のリスクが増大する。
神経眼科的徴候は全身症状と同時、または数日〜数週間後に出現する。
NA-AIONの推定機序として、SARS-CoV-2感染による炎症性・自己免疫性の血栓性微小血管障害が考えられている。2)ワクチン関連神経眼科的合併症では、脈絡膜毛細血管の微小血管虚血による急性黄斑神経網膜症(AMN)が報告されている。
ロングCOVIDにおける神経眼科的症状は、慢性炎症とサイトカイン産生の持続増加によって維持されると推定されている。
7. 最新の研究と今後の展望(研究段階の報告)
Section titled “7. 最新の研究と今後の展望(研究段階の報告)”抗ウイルス薬による神経学的合併症予防
Section titled “抗ウイルス薬による神経学的合併症予防”Grundmannら(2022)は、重症COVID-19患者を対象とした解析で、デキサメタゾンまたはレムデシビルによる治療が脳卒中・けいれん・髄膜炎を含む神経学的合併症の頻度低下と関連することを報告した1)。両薬剤の併用では相乗効果が見られ、非低酸素性COVID-19においてもデキサメタゾンが神経学的合併症リスクを低下させた。神経学的合併症の予防という観点からの両薬剤の位置づけは、今後さらなる検討が必要である。
ワクチン接種後の神経眼科的合併症
Section titled “ワクチン接種後の神経眼科的合併症”COVID-19ワクチン接種後に神経眼科的合併症が報告されている。
- 頭蓋内出血・脳静脈血栓症
- 脳神経症・瞳孔異常(ホルネル症候群、ホームズ・アディー瞳孔、縮瞳、散瞳)
- 両側性AION・急性虚血性脳卒中
- 視神経炎・BPPV
- 急性黄斑神経網膜症(AMN):感染またはワクチン接種との直接関連の可能性
ロングCOVIDの神経眼科症状
Section titled “ロングCOVIDの神経眼科症状”COVID-19回復後も神経眼科的症状が持続するロングCOVIDにおいて、以下が報告されている。
- 頭痛・視神経炎の持続
- 角膜神経損傷
- 眼球運動の変化
- 視神経乳頭静脈炎
- 炎症性網膜血管閉塞
巨細胞性動脈炎(GCA)との関連
Section titled “巨細胞性動脈炎(GCA)との関連”COVID-19感染およびワクチン接種の両方と巨細胞性動脈炎(GCA)の関連が報告されており、今後のエビデンス蓄積が期待される。
8. 参考文献
Section titled “8. 参考文献”- Grundmann A, et al. Fewer COVID-19 neurological complications with dexamethasone and remdesivir. Ann Neurol. 2022. doi:10.1002/ana.26536
- Salvetat ML, et al. Non-Arteritic Anterior Ischemic Optic Neuropathy. Vision. 2023;7:72.
