口腔顔面浮腫
発現頻度:症例の80〜100%と最も高頻度。
典型的性状:片側性・無痛性・非圧痕性。上唇に好発。
経過:初期は一過性・断続性だが、後に持続性となることがある。組織の線維化に至る可能性がある。
鑑別:血管性浮腫と類似するが、MRSはより持続的で抗ヒスタミン薬に不応。補体価は正常。

メルカーソン・ローゼンタール症候群(Melkersson-Rosenthal Syndrome; MRS)は、非乾酪性慢性肉芽腫性神経皮膚疾患である。口腔および顔面の浮腫を呈し、生検では肉芽腫性炎症が認められる。「口腔顔面肉芽腫症(orofacial granulomatosis)」と呼ばれる疾患群に属する。
本症の歴史的記述は以下の通りである。1928年にErnst Melkersson が再発性顔面神経麻痺と浮腫の存在を初めて詳細に報告した。1931年にCurt Rosenthalが溝状舌(lingua plicata)を追加記載し、1949年にLüscherが「Melkersson-Rosenthal症候群」の名称を初めて使用した3)。
疫学的には、一般人口の0.08%に発生すると推定される2)。20〜30代で最も頻繁に見られ、発症時の平均年齢は39歳(範囲:8〜79歳)である。女性優位(約3倍)とされる。
古典的三徴は以下の3つである。
3つすべての症状が揃うのは症例の8〜25%に過ぎない。多くは1〜2症状のみを呈し、単一症状型は肉芽腫性口唇炎(Miescher口唇炎)として記述されることがある1)。
一部の研究者は本症がサルコイドーシスやクローン病の症状の一つである可能性を示唆しており、独立疾患か否かは未解決のままである。
古典的三徴がすべて揃うのは症例の8〜25%に過ぎない。病歴と身体診察で1〜2症状が確認できた場合、または生検で肉芽腫性口唇炎が認められた場合でも診断は可能である。確定診断が得られることは稀であり、長期的な経過観察が必要となる。
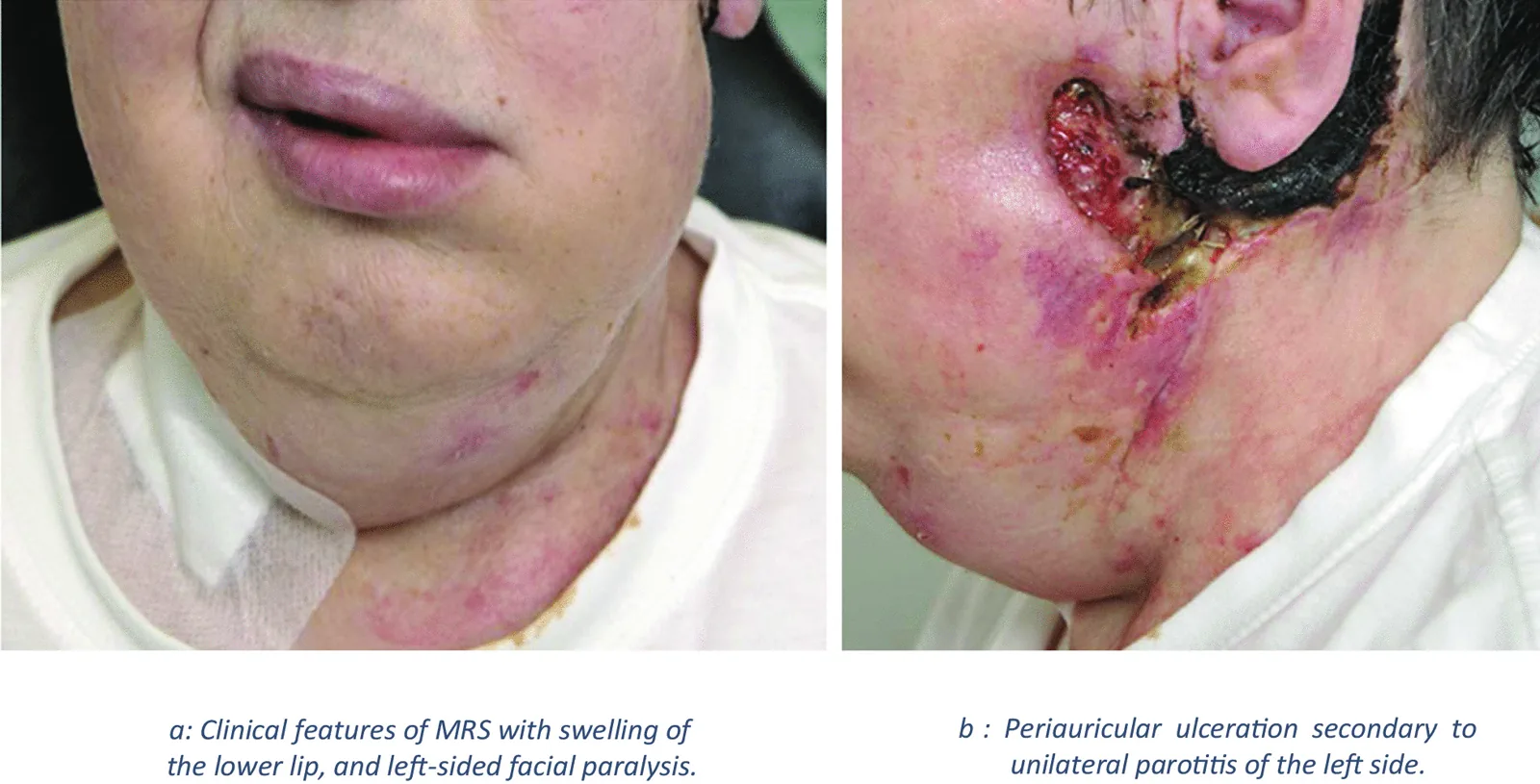
患者が自覚する症状は多岐にわたる。
三徴の各要素は発現頻度と特徴が大きく異なる。
口腔顔面浮腫
発現頻度:症例の80〜100%と最も高頻度。
典型的性状:片側性・無痛性・非圧痕性。上唇に好発。
経過:初期は一過性・断続性だが、後に持続性となることがある。組織の線維化に至る可能性がある。
鑑別:血管性浮腫と類似するが、MRSはより持続的で抗ヒスタミン薬に不応。補体価は正常。
顔面神経麻痺
発現頻度:症例の47〜60%(最大90%)。片側性または両側性。
経過:初回は回復することが多いが、再発するにつれ持続期間が延長し永続的となることがある。再発率は3〜11%。
浮腫との関係:口腔顔面浮腫の数年前または数年後に出現しうる。罹患者の13〜50%で浮腫と顔面神経麻痺が合併する。
疫学:MRS関連顔面神経麻痺の発生率は10万人あたり0.36人/年5)。
溝状舌
発現頻度:症例の30〜35%。
性状:深さ約2mm、長さ約15mmの溝。先天性の場合もある。
診断的意義:正常人口の5%にも認められるため、単独では診断根拠にならない。
眼科的所見として、眼瞼浮腫のみを呈する単一症状型MRSも報告されている3)。その他の眼科的随伴所見として、球後視神経炎・角膜混濁・乾性角結膜炎・眼瞼弛緩症(blepharochalasis)が挙げられる3)。全身合併症として憩室炎やぶどう膜炎が報告されており、クローン病やサルコイドーシスとの関連が示唆されている。
ベル麻痺には口腔顔面浮腫を伴わない。一方MRSでは口腔顔面浮腫が症例の80〜100%に認められる。再発性の顔面神経麻痺を口腔顔面浮腫が伴う場合、MRSを積極的に疑うべきである。
病因は不明である。以下の因子が関与していると考えられているが、MRSの原因を説明する強力な関連性は見つかっていない。
誘因・リスク因子は以下のように分類される。
| 分類 | 主な因子 |
|---|---|
| 遺伝的要因 | 常染色体優性遺伝(9p11)、FATP1/SLC27A1遺伝子変異 |
| 感染・免疫 | EBV、VZV、CMV、HSV、COVID-19、Th1型細胞性免疫応答 |
| アレルゲン | 食品添加物、グルテン、金・水銀・コバルト、歯科用アマルガム |
| 薬剤 | ACE阻害薬、カルシウム拮抗薬 |
| その他 | ストレス、ホルモン変化、UV-B過敏症、アトピー |
遺伝的要因については、第9染色体短腕(9p11)に原因遺伝子を持つ常染色体優性遺伝が報告されている。ATP1(FATP1)遺伝子変異が中国の家系で報告され、ヘテロ接合性SLC27A1(FATP1)変異も報告されているが確定には至っていない3)。家族性MRSの報告例では、患者の兄・息子・母・姉に溝状舌が認められた5)。
感染症については、ウイルス感染(EBV, VZV, CMV, HSV)が誘因となりうる。COVID-19感染を契機とした4年ぶりの再発例が報告されており、マスト細胞の活性化がCOVID-19の炎症反応とMRSの病態に共通して関与している可能性が示唆されている2)。
免疫学的にはTh1型細胞性免疫応答の関与が考えられている1)。アレルゲンとしては、グルテン含有食品・チョコレート・シナモン・食品添加物(グルタミン酸ナトリウム)・歯磨き粉、金属(金・水銀・コバルト・亜鉛)、歯科用アマルガムなどが挙げられる1)。
関連疾患としてクローン病・サルコイドーシスとの重複が議論されている。なおサルコイドーシスの診断においてMRSは除外すべき「他の肉芽腫性皮膚疾患」の一つとして挙げられており、両者の鑑別が求められる。
MRSでは常染色体優性遺伝が示唆されており、家族内に溝状舌や顔面神経麻痺を持つ例が報告されている5)。ただし疾患の臨床的・遺伝的多様性は大きく、遺伝的原因の確定には至っていない3)。
病歴と身体診察に基づく臨床診断が基本である。三徴のうち2つ以上が認められるか、または生検で肉芽腫性口唇炎が確認されれば診断に十分とされる5)。確定診断が得られることは稀であり、長期的な経過観察が必要である。
診断確定に必須ではないが有用である。特徴的な組織所見は以下の通りである。
感染症除外のため周辺虹彩前癒着染色・Ziehl-Neelsen染色・Grocott銀染色などを施行する1)4)。
鑑別診断のために以下の検査を行う。
なおサルコイドーシスを眼所見から疑う場合には、血液検査(血清ACE、血清可溶性IL-2受容体)と胸部X線を施行し、必要に応じて呼吸器内科・皮膚科へ紹介すべきである。
MRSには多くの鑑別診断があり、臨床症状がより一般的な疾患と重複するため見逃されることがある。
| 鑑別疾患 | 鑑別のポイント |
|---|---|
| 血管性浮腫 | MRSはより持続的、抗ヒスタミン薬に不応、補体価正常 |
| サルコイドーシス | 肺門リンパ節腫脹・ACE高値・sIL-2R高値で鑑別 |
| クローン病 | 消化器症状の有無、便潜血、大腸内視鏡4) |
| ベル麻痺 | 口腔顔面浮腫を伴わない |
| 眼瞼浮腫の鑑別 | 腫瘍、偽腫瘍、リンパ増殖性疾患、甲状腺眼症3) |
その他の鑑別疾患として甲状腺機能低下症・上大静脈症候群・リンパ管腫・丹毒・リンパ腫がある。診断には眼科・皮膚科・免疫科・消化器科などの多職種連携が必要な場合がある。
根治療法は存在せず、再発は避けられない。自然寛解も報告されているが、治療が行われない場合は症状エピソードがより頻繁かつ長期化する可能性がある。標準的な治療法は未確立であり、以下の段階的アプローチが報告されている。
第一選択
病変内ステロイド注射:トリアムシノロンアセトニド 10〜40 mg/mL。全身投与と同等の有効性が示されている1)3)。
経口ステロイド:プレドニゾン(1 mg/kg/日、10日間後漸減)。寛解率は高いが再発する5)。
NSAIDs・抗ヒスタミン薬:初期治療として用いる。
第二選択以降
抗ウイルス薬(アシクロビル400 mg 4時間毎)は顔面神経麻痺に対してステロイドと併用されることがある5)。
保存的治療に抵抗する顔面神経麻痺には顔面神経減圧術が有効な選択肢となる。重度麻痺(House-Brackmann Grade VI)からGrade IIへの劇的な改善例が報告されており5)、将来の再発予防効果も示唆されている。保存的治療との比較対照試験は未実施であるが、Grade IV以上の持続性麻痺では手術を検討すべきとされる。
MRSの基本病態は、非乾酪性上皮細胞肉芽腫を主体とする慢性肉芽腫性炎症である。組織学的には多核ランゲルハンス型巨細胞・血管周囲単核球性炎症浸潤・リンパ浮腫・線維化を伴う。
免疫学的機序としてはTh1型細胞性免疫応答の関与が示されている1)。マスト細胞の活性化がサイトカイン(IL-1、IL-6)放出を促し、局所の肉芽腫性炎症や浮腫を惹起すると考えられている2)。
顔面神経麻痺の機序は、肉芽腫性浸潤と浮腫による神経組織への圧迫である。再発するたびに神経が進行性に損傷されるため、麻痺の持続期間が延長していく5)。
遺伝学的基盤としては9p11領域、FATP1(SLC27A1)遺伝子変異が示唆されているが、疾患の臨床的・遺伝的多様性が大きく確定的結論には至っていない3)。
MRS・肉芽腫性口唇炎・サルコイドーシス・クローン病が連続的スペクトラムを構成する可能性が議論されている1)。これらの疾患はいずれもTh1型免疫応答による非乾酪性肉芽腫を特徴とし、臨床的・組織病理学的な類似性を持つ。
Talidere ら(2021)は、COVID-19感染を契機に4年ぶりにMRSが再発した51歳女性を報告した2)。口唇浮腫・右顔面神経麻痺・溝状舌の古典的三徴すべてを呈し、ヒドロキシクロロキン・アジスロマイシン・ステロイド療法で軽快した。マスト細胞がCOVID-19とMRSの炎症反応において共通の役割を担う可能性が考察され、COVID-19感染がMRS再発の誘因となりうることが初めて報告された。
Estacia ら(2022)は、右眼瞼浮腫のみを呈した単一症状型MRS(59歳女性)において、病変内トリアムシノロン注射5回(1年間)および経口プレドニゾンに不応であった症例に対し、タクロリムス0.03%軟膏を適用し改善を報告した3)。ステロイド不応性の眼瞼浮腫に対する新たな局所療法として注目されている。
Alencar ら(2023)は、家族性MRS(38歳女性)の3回目発作(左側Grade VI麻痺)に対して顔面神経減圧術を施行し、術後8か月でGrade IIへの著明な改善を報告した5)。患者の兄・息子・母・姉に溝状舌、兄に顔面神経麻痺の既往があり、常染色体優性遺伝のパターンを示した。保存的治療(プレドニゾン60 mg/日・アシクロビル400 mg)では改善が得られなかった症例であり、遅延減圧術の有効性と将来の再発予防効果が示唆された。
MRSの原因遺伝子候補としてSLC27A1(FATP1)のヘテロ接合変異が報告されているが、臨床的・遺伝的多様性が大きく、単一遺伝子変異で疾患全体を説明することは困難である3)。遺伝子研究の進展により、MRSの病態解明と治療標的の同定が期待されている。