眼所見
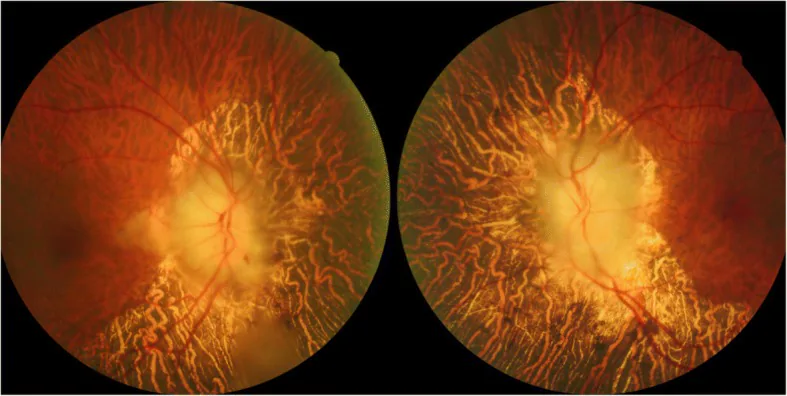
視神経乳頭の蒼白浮腫(pallid swelling):動脈炎性前部虚血性視神経症(A-AION)の典型所見。
RAPD(相対的求心性瞳孔反応)陽性:患側で陽性となる。
乳頭周囲出血・軟性白斑:網膜所見として認められる場合がある。
蛍光眼底造影:視神経乳頭への充盈遅延、乳頭周囲脈絡膜の充盈遅延・欠損を認める。

巨細胞性動脈炎(Giant Cell Arteritis; GCA)は、中〜大型血管を侵す全身性肉芽腫性血管炎である。側頭動脈炎(temporal arteritis)とも呼ばれる。50歳以上に好発し、中央値は75歳である。
10世紀バグダッドのAli Ibn Isa al-Kahhalによる記述が最古とされる。1890年にHutchinsonが頭部の「痛みを伴う赤い筋」を記述した。1932年にBayard Hortonが初めて側頭動脈生検を実施し、肉芽腫性血管炎として記載した。1941年にGilmourが巨細胞を初めて記述した。
発症率は50歳以上で年間10万人あたり18〜29例と報告されている3)。年齢とともに増加し、60歳代で10万人あたり2.3例、90歳代で44.7例とされる。
性差として、女性は男性の2〜6倍の頻度で発症する。人種差が顕著であり、北欧系白人で最も多く、ノルウェーでは10万人あたり約30人に達する。一方、日本での発症率は10万人あたり1.47人と欧米に比べてきわめてまれである。欧州では50歳以上の原発性全身性血管炎の中で最も多い疾患で、毎年100万人あたり32〜290人の発症が報告されている。
日本での発症率は10万人あたり1.47人と欧米に比べてまれだが、発症は報告されている。日本では高安動脈炎が多く、巨細胞動脈炎は相対的に少ない傾向がある。アジア人でも発症しうる疾患であり、典型的な症状がある場合は積極的に疑うことが重要である。
恒久的視力喪失の約30%で前駆症状として認められ、平均8.5日前に出現する。一過性黒内障を生じた場合は緊急に眼科を受診し、巨細胞動脈炎を積極的に鑑別すべきである。早期にステロイド治療を開始することで恒久的視力喪失を予防できる可能性がある。
眼所見
視神経乳頭の蒼白浮腫(pallid swelling):動脈炎性前部虚血性視神経症(A-AION)の典型所見。
RAPD(相対的求心性瞳孔反応)陽性:患側で陽性となる。
乳頭周囲出血・軟性白斑:網膜所見として認められる場合がある。
蛍光眼底造影:視神経乳頭への充盈遅延、乳頭周囲脈絡膜の充盈遅延・欠損を認める。
全身所見
側頭動脈の異常:怒張、結節、圧痛、拍動の減弱または消失。
眼球運動制限:脳神経麻痺による複視と眼球運動制限を生じることがある。
Horner症候群:まれに巨細胞動脈炎診断時に認められる。部分的眼瞼下垂と縮瞳を呈する6)。
巨細胞動脈炎の病因は複合的であり、遺伝的要因と環境因子が免疫反応を誘発すると考えられている。
HLA DRB1*04、DRW6、DR3が感受性増加と関連する。TNF-α遺伝子座やIL-10プロモーターの多型もリスク増大と相関する。
クラミジア・ニューモニエ、水痘帯状疱疹ウイルス、パルボウイルスB19の関与が示唆されているが、相反する報告も存在する。水痘帯状疱疹ウイルスとの関連を示唆する特徴が報告されている。
内弾性板・エラスチン・細胞外マトリックスの石灰化が年齢特異的発現を説明する可能性がある。
巨細胞動脈炎の診断には臨床所見、血液検査、画像検査、側頭動脈生検を組み合わせる。
1990年ACR(米国リウマチ学会)分類基準では以下の5項目中3項目以上で診断する。
| 項目 | 基準 |
|---|---|
| 1. 発症年齢 | 50歳以上 |
| 2. 新たな頭痛 | 新発の頭痛 |
| 3. 側頭動脈異常 | 圧痛または脈拍減弱 |
| 4. 赤血球沈降速度 | ≥50 mm/h |
| 5. 動脈生検 | 単核細胞浸潤または肉芽腫性炎症 |
2022年ACR/EULAR分類基準ではCRP≥10 mg/Lが追加され、より包括的な診断が可能になった3)。
確定診断のゴールドスタンダードであり、感度・特異度ともに95%以上とされる。検体はできるだけ大きく採取し、スキップ病変(skip lesion)があるため通常2cm以上の採取が推奨される。巨細胞は確定診断に必須ではないが、内弾性板の破壊が重要な所見である。
偽陰性率は最大61%との報告もあり、生検陰性でも巨細胞動脈炎を否定できない3)。
非侵襲的で反復可能な検査であり、欧州では巨細胞動脈炎早期診断の主要画像ツールとして普及している。感度77%、特異度96%と報告されている2)。
特徴的な超音波所見を以下に示す。
スキップ病変のため、両側かつ多領域の動脈を包括的に検索することが重要である4)。
結節性多発性動脈炎、多発血管炎性肉芽腫症(Wegener)、全身性エリテマトーデス(SLE)などの他の血管炎と鑑別する。巨細胞動脈炎では肺や腎臓が侵されないことが重要な鑑別点である。全身症状を欠き視力障害のみを呈する「オカルト巨細胞動脈炎」が約20%に存在することも念頭に置く。
スキップ病変のために偽陰性率が最大61%との報告があり3)、生検陰性のみで巨細胞動脈炎を否定することはできない。臨床所見・血液検査・超音波所見を総合的に判断する必要がある。生検が陰性でも臨床的に強く疑われる場合は治療継続が考慮される。
巨細胞動脈炎は視力喪失のリスクがある眼科的救急疾患であり、確定診断を待たずに早急な治療開始が必要である。
視覚障害を伴うA-AIONに対しては、入院でのステロイド大量点滴療法(パルス療法)を行う。
発症眼の視力回復は非常に困難であり、治療後も最終視力が0.1以下となる症例が多い。無治療では短期間で高頻度に僚眼にも発症し、15〜40%が両眼性となる。治療の主目的は僚眼への進展防止である。
海外の報告では以下の漸減スケジュールが用いられた症例がある3)。
| 投与量 | 期間 |
|---|---|
| プレドニゾン60 mg | 2週間 |
| プレドニゾン50 mg | 2週間 |
| プレドニゾン40 mg | 2週間 |
| プレドニゾン30 mg | 1週間 |
| プレドニゾン20 mg | 1週間 |
| プレドニゾン10 mg | 1週間 |
日本の教科書では全身状態・ESR・CRPを指標として漸減速度を個別に調整することが強調されている。
視覚障害を含む頭蓋虚血症状がある場合は、IV メチルプレドニゾロン500〜1,000 mgを3日間投与してから経口に切り替える方法も報告されている5)。
再発時はステロイドを増量し、メトトレキサートの併用が推奨される場合がある5)。
発症眼の視力回復は困難であり、治療後も最終視力が0.1以下となる症例が多い。治療の主目的は発症眼の回復ではなく、僚眼への進展防止にある。無治療では15〜40%が両眼性の視力喪失に至るため、早期にステロイド治療を開始することが極めて重要である。
巨細胞動脈炎の病態は2つの免疫反応機序からなる。
全身性炎症反応
IL-6媒介の自然免疫反応:循環マクロファージ・好中球・単球がIL-6を産生する。
急性期反応の過剰活性化:CRP、ハプトグロビン、フィブリノーゲン、補体の上昇と相関する。
全身症状の原因:発熱・倦怠感・体重減少などを引き起こす。
抗原特異的反応
動脈壁への侵入:外膜の栄養血管(vasa vasorum)を利用してマクロファージとT細胞が侵入する。
免疫カスケード:活性化T細胞→樹状細胞成熟→CD4+ T細胞動員→Th1/Th17分極→IFN-γ/IL-17産生→単球動員→マクロファージ分化→巨細胞形成。
血管壁破壊:メタロプロテアーゼと活性酸素中間体による内弾性板の破壊が生じる。
断裂した内弾性板と全層にわたる細胞浸潤が特徴的である。巨細胞は断裂した内弾性板の近くに位置する。急性期はリンパ球浸潤が主体であり、慢性期には線維化が生じる。なお、B細胞の関与は確認されておらず、ANCA関連血管炎との重要な鑑別点となる。
炎症に対する治癒反応として内膜肥厚・筋線維芽細胞増殖・細胞外マトリックス沈着が生じ、血管狭窄・閉塞をきたす。内腔側は血流速度が速いため通常影響を受けにくい。
短後毛様動脈(SPC動脈)の閉塞が主な原因である。SPC動脈の閉塞→視神経乳頭の篩板前部・篩板部への血流遮断→動脈炎性前部虚血性視神経症(A-AION)という経路をたどる。巨細胞動脈炎症例の約20%でSPC動脈の血栓性閉塞が関与する7)。
IL-6受容体拮抗薬であるトシリズマブはランダム化比較試験(RCT)で巨細胞動脈炎に対するグルココルチコイド(GC)スペアリング効果と寛解達成の有効性が証明されている5)。GCの長期投与に伴う毒性を軽減する代替療法として注目されている。
超音波を活用した巨細胞動脈炎迅速診断経路が欧州で普及しつつある。
Piccusらの総説(2022)によれば、fast-track pathwayの導入により視力喪失の減少、過剰治療の抑制、費用対効果の改善がもたらされることが示されている5)。超音波検査は非侵襲的かつ反復可能であり、多数の動脈領域を一度に評価できるため、欧州では早期診断の主要ツールとして位置づけられている。
巨細胞動脈炎診断時にHorner症候群(部分的眼瞼下垂・縮瞳)を合併する症例が報告されている6)。栄養血管の血管炎による交感神経線維の虚血性損傷が推定メカニズムである。
Sverdlichenkoら(2022)は巨細胞動脈炎合併Horner症候群の症例シリーズを報告し、眼周囲領域の交感神経線維の虚血性損傷がメカニズムである可能性を示唆した6)。
巨細胞動脈炎と亜急性甲状腺炎の合併は非常にまれな病態である。超音波検査が両疾患の鑑別に有用とされる4)。
2022年ACR/EULAR基準でCRP≥10 mg/Lが追加されたことにより、より包括的な診断が可能になった3)。今後も画像診断技術の進歩とバイオマーカー研究により診断精度の向上が期待される。